13.短周期元素的离子:aW3+、bX+、cY2-、dZ-具有相同的电子层结构,下列关系中不正确的是( )
| A. | 半径:Y2->Z->X+>W3+ | B. | 还原性:Y2->Z- | ||
| C. | 氧化性:W3+>X+ | D. | 质子数:c>d>b>a |
12.下列关于物质性质变化的比较,不正确的是( )
| A. | 稳定性:HI>HBr>HCl>HF | B. | 原子半径大小:Na>S>O | ||
| C. | 碱性强弱:KOH>NaOH>LiOH | D. | 还原性强弱:Cl-<Br-<I- |
11.将14Si的电子排布式写成1S22S22P63S23P2X,它违背了( )
| A. | 构造原理 | B. | 泡利原理 | C. | 洪特规则 | D. | 能量守恒原理 |
10.下列有关电池的说法不正确的是( )
| A. | 铅蓄电池属于二次电池 | |
| B. | 锂离子电池是一种一次性电池 | |
| C. | 氢氧燃料电池可把化学能转化为电能 | |
| D. | 镍镉电池中,Cd为负极,NiO(OH)为正极 |
9.下列分子中所有原子都满足最外层为8电子结构的是( )
| A. | CCl4 | B. | HClO | C. | PCl5 | D. | NH3 |
7.下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是Ar(填具体元素符号,下同),原子结构示意图为 ;元素⑩名称为Br.
;元素⑩名称为Br.
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,碱性最强的化合物的电子式是: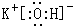 .
.
(3)元素⑤与⑦形成化合物的化学式为AlCl3;实验测得,当此化合物在液态或固态时不导电,溶解于水时能导电,由此判断该化合物属于共价化合物.
(4)元素③、⑥、⑦形成的气态氢化物中,沸点最高的物质的化学式是H2O,原因是H2O分子间含有氢键.
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是S2->Cl->O2-.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 ;元素⑩名称为Br.
;元素⑩名称为Br.(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,碱性最强的化合物的电子式是:
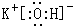 .
.(3)元素⑤与⑦形成化合物的化学式为AlCl3;实验测得,当此化合物在液态或固态时不导电,溶解于水时能导电,由此判断该化合物属于共价化合物.
(4)元素③、⑥、⑦形成的气态氢化物中,沸点最高的物质的化学式是H2O,原因是H2O分子间含有氢键.
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是S2->Cl->O2-.
6.某短周期元素的气态氢化物与该元素最高价氧化物对应的水化物反应生成盐.下列说法正确的是( )
0 154983 154991 154997 155001 155007 155009 155013 155019 155021 155027 155033 155037 155039 155043 155049 155051 155057 155061 155063 155067 155069 155073 155075 155077 155078 155079 155081 155082 155083 155085 155087 155091 155093 155097 155099 155103 155109 155111 155117 155121 155123 155127 155133 155139 155141 155147 155151 155153 155159 155163 155169 155177 203614
| A. | 该元素位于元素周期表的第三周期ⅦA族 | |
| B. | 生成的盐含有的化学键既有离子键又有共价键 | |
| C. | 该元素的常见化合价有:-1、0、+1、+3、+5、+7等 | |
| D. | 该元素的氢化物的稳定性比PH3、H2S弱 |
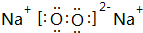 ,其中含有的化学键为离子键和共价键.
,其中含有的化学键为离子键和共价键.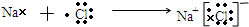 .
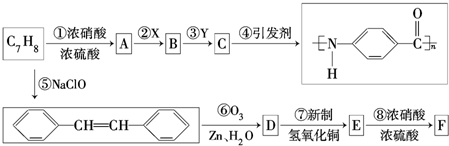
. 
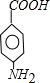 .
.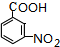 .
.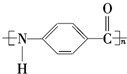 +n H2O、
+n H2O、 +2Cu(OH)2$\stackrel{△}{→}$Cu2O↓+2H2O+
+2Cu(OH)2$\stackrel{△}{→}$Cu2O↓+2H2O+ 、
、