13.下列各组晶体中化学键类型和晶体类型均相同的是( )
| A. | 二氧化硅和二氧化碳 | B. | 金刚石和石墨 | ||
| C. | 氯化钠和过氧化钠 | D. | 铁和铜 |
12.下列说法正确的是( )
| A. | 钾(K)原子基态的原子结构示意图为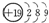 | |
| B. | Ca2+电子排布式为1s22s22p63s23p64s2 | |
| C. | 原子核内有10个中子的氧原子可表示为${\;}_{8}^{16}$O | |
| D. | H2O分子的电子式为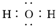 |
11.符号为M的能层所含的能级有几种( )
| A. | 2 | B. | 3 | C. | 8 | D. | 18 |
8.图为元素周期表中短周期的一部分, 四种元素中只有一种是金属,下列说法错误的是( )
四种元素中只有一种是金属,下列说法错误的是( )
 四种元素中只有一种是金属,下列说法错误的是( )
四种元素中只有一种是金属,下列说法错误的是( )| A. | 气态氢化物稳定性:R>Q | |
| B. | 元素T的离子结构示意图为 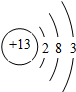 | |
| C. | 与W同主族的某元素形成的18电子的氢化物分子中既有极性键又有非极性键 | |
| D. | Q的一种同位素可用于测定文物的年代 |
7.下列离子中半径最大的是( )
| A. | O2? | B. | F- | C. | Mg2+ | D. | Al3+ |
5.用FeCl3酸性溶液脱除H2S后的废液,通过控制电压电解得以再生.某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol/L的FeCl2溶液,研究废液再生机理.记录如下(a、b、c代表电压数值):
(1)用FeCl3酸性溶液脱除H2S的离子方程式为2Fe3++H2S═S↓+2Fe2++2H+
(2)用KSCN检验出Fe3+的离子方程式为Fe3++3SCN-═Fe(SCN)3.
(3)Ⅰ中,Fe3+产生的原因可能是:Cl-在阳极放电(或Cl-失电子生成Cl2),生成的Cl2将Fe2+氧化.
(4)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有还原性.
(5)Ⅱ中虽未检验出Cl2,但Cl-在阳极是否放电仍需进一步验证.电解pH=1的NaCl溶液做对照实验,记录如下:
①NaCl的浓度是0.2mol/L
②Ⅳ中检测Cl2的实验方法湿润的淀粉碘化钾检验生成气体,试纸变蓝.
③与Ⅱ对比,得出的结论(写出两点):通过控制电压,证实了产生Fe3+的两种原因,通过控制电压,验证了Fe2+先于Cl-放电.
0 154981 154989 154995 154999 155005 155007 155011 155017 155019 155025 155031 155035 155037 155041 155047 155049 155055 155059 155061 155065 155067 155071 155073 155075 155076 155077 155079 155080 155081 155083 155085 155089 155091 155095 155097 155101 155107 155109 155115 155119 155121 155125 155131 155137 155139 155145 155149 155151 155157 155161 155167 155175 203614
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅰ | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| Ⅱ | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| Ⅲ | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
(2)用KSCN检验出Fe3+的离子方程式为Fe3++3SCN-═Fe(SCN)3.
(3)Ⅰ中,Fe3+产生的原因可能是:Cl-在阳极放电(或Cl-失电子生成Cl2),生成的Cl2将Fe2+氧化.
(4)由Ⅱ推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有还原性.
(5)Ⅱ中虽未检验出Cl2,但Cl-在阳极是否放电仍需进一步验证.电解pH=1的NaCl溶液做对照实验,记录如下:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅳ | a>x≥c | 无明显变化 | 有Cl2 |
| Ⅴ | c>x≥b | 无明显变化 | 无Cl2 |
②Ⅳ中检测Cl2的实验方法湿润的淀粉碘化钾检验生成气体,试纸变蓝.
③与Ⅱ对比,得出的结论(写出两点):通过控制电压,证实了产生Fe3+的两种原因,通过控制电压,验证了Fe2+先于Cl-放电.
 .
.
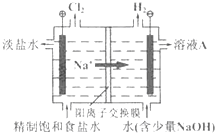 氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.完成下列填空:
氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.完成下列填空: