13.下列离子能大量共在的是( )
| A. | Ba2+、Na+、OH-、SO42- | B. | H+、Na+、I-、Cl- | ||
| C. | HCO3-、K+、NO3-、OH- | D. | H+、Fe2+、SO42-、NO3- |
12.下列说法中,正确的是( )
| A. | 硅是不活泼的非金属元素,在自然界中可以以游离态的形式存在 | |
| B. | 传统无机非金属材料和新型无机非金属材料的主要成分都是硅酸盐 | |
| C. | 铝制品在空气中有很强的抗腐蚀性是因为铝的化学性质不活泼 | |
| D. | 铝合金比纯铝的硬度更大、熔点更低 |
11.下列元素的原子在形成不同物质时,既能形成离子键,又能形成共价键的是( )
| A. | K | B. | Ca | C. | Cl | D. | Ar |
10.向一个2L容密闭容器中充入3.6molN2和10.8molH2,一定的条件下反应生成NH3,10min后测得N2的浓度是0.8mol•L-1,则在这10min内NH3的平均反应速率是( )
| A. | 0.1 mol•L-1•min-1 | B. | 0.2 mol•L-1•min-1 | ||
| C. | 0.3 mol•L-1•min-1 | D. | 0.6 mol•L-1•min-1 |
9.由于地球引力的存在,人在地球上生活而不能自动脱离地球.同理,原子之间能自动结合是因为它们之间存在着强烈的相互作用--化学键,由于有化学键才使得100多种元素构成了世界万物.下列有关化学键的叙述,正确的是( )
| A. | 离子化合物中一定含有离子键,可能含共价键,共价化合物中只含共价键绝不含有离子键 | |
| B. | 单质分子中均存在化学键,且只含有共价键,不可能含有离子键 | |
| C. | 共价化合物中可能含非极性共价键,离子化物中不可能含非极性共价键 | |
| D. | 共价化合物中可能含离子键,离子化合物中只含离子键 |
8.一种一元强酸HA溶液中加入一种碱MOH反应后,溶液呈中性,下列判断中正确的是( )
| A. | 若为强碱,则需加入的碱过量 | |
| B. | 混合前酸与碱中溶质的物质的量相等 | |
| C. | 生成的盐不发生水解 | |
| D. | 反应溶液中c(A-)、c(M+)相等 |
7.已知各破坏1mol N≡N键、H-H键和N-H键分别需要吸收的能量为946kJ、436kJ、391kJ.计算1mol N2(g)和3mol H2(g)完全转化为NH3(g)的能量变化为( )
| A. | 吸收92KJ | B. | 放出92kJ | C. | 吸收184kJ | D. | 放出184KJ |
6.下列化学用语或模型表示正确的是( )
| A. | 氚原子符号:H | B. | H2O2分子结构式:H-O-O-H | ||
| C. | Mg2+结构示意图: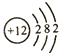 | D. | HF的形成过程 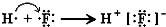 |
5.下列关系正确的是( )
| A. | 熔点:正戊烷>2,2一二甲基戊烷>2,3一二甲基丁烷>丙烷 | |
| B. | 密度:CCl4>H2O>苯 | |
| C. | 同质量的物质燃烧耗O2量:丙炔>乙烷>乙烯>乙炔>甲烷 | |
| D. | 同物质的量物质燃烧耗O2量:已烷>环已烷>苯>苯甲酸 |
4.下列图象正确的是( )
0 154973 154981 154987 154991 154997 154999 155003 155009 155011 155017 155023 155027 155029 155033 155039 155041 155047 155051 155053 155057 155059 155063 155065 155067 155068 155069 155071 155072 155073 155075 155077 155081 155083 155087 155089 155093 155099 155101 155107 155111 155113 155117 155123 155129 155131 155137 155141 155143 155149 155153 155159 155167 203614
| A. | 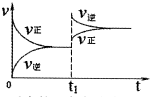 反应的正方向放热(t1时升温) | |
| B. | 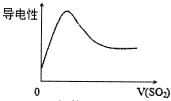 SO2气体通入氯水中 | |
| C. | 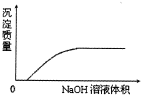 NaOH溶液滴加Ca(HCO3)2溶液中 | |
| D. | 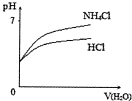 将PH相同的NH4Cl溶液和稀盐酸稀释时PH的变化 |