11.不能说明金属性Na>Mg>Al的是( )
| A. | 碱性NaOH>Mg(OH)2>Al (OH)3 | |
| B. | 原子半径Na>Mg>Al | |
| C. | 阳离子的氧化性Na+<Mg2+<Al3+ | |
| D. | Na与冷水剧烈反应,Mg与冷水反应微弱;镁粉与铝粉分别与同浓度稀HCl反应,镁粉比铝粉反应剧烈 |
10.下列说法正确的是( )
| A. | ${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、${\;}_{1}^{3}$H三种核素的性质不同 | |
| B. | 16O2、18O2彼此是同位素 | |
| C. | 14N、14C两种核素的中子数相同,质子数不同 | |
| D. | 白磷与红磷是磷元素的两种同素异形体 |
9.下列化学用语正确的是( )
| A. | 氯离子结构示意图 | B. | HCl的电子式  | ||
| C. | CO2的结构式 O=C=O | D. | 作为相对原子质量标准的原子614C |
8.关于目前常用元素周期表的说法中正确的是( )
| A. | 第ⅢB族元素种类最多 | |
| B. | 只有第3列到第12列全部是金属元素 | |
| C. | 周期数大于或等于族的序数时,一定是金属元素 | |
| D. | 是按原子的质量数由小到大的顺序编制的 |
7.部分难溶物的颜色和常温下的Ksp如下表所示:
某研究性学习小组对电解食盐水进行了如下探究: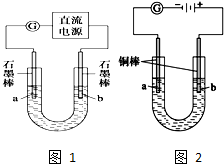
实验Ⅰ:装置如图所示,接通电源后,发现a、b电极上均有气泡产生.
(1)电解过程中的总离子反应方程式为2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑.
(2)为了确定电源的正、负极,下列操作一定行之有效的是BD.
A.观察两极产生气体的颜色
B.往U形管两端分别滴入数滴酚酞试液
C.用燃着的木条靠近U形管口
D.在U形管口置一张湿润的淀粉KI试纸
实验Ⅱ:把上述电解装置的石墨棒换成铜棒,用直流电源进行电解,装置如图所示.
观察到的现象如下所示:
①开始无明显现象,随后液面以下的铜棒表面逐渐变暗;
②5min后,b极附近开始出现白色沉淀,并逐渐增多,且向a极扩散;
③10min后,最靠近a极的白色沉淀开始变成红色;
④12min后,b极附近的白色沉淀开始变成黄色,然后逐渐变成橙黄色;
⑤a极一直有大量气泡产生;
⑥停止电解,将U形管中悬浊液静置一段时间后,上层溶液呈无色,没有出现蓝色,下层沉淀全部显砖红色.
(3)a极发生的电极反应方程式为:2H++2e-=H2↑(或2H2O+2e-═2OH-+H2↑).
(4)电解5min后,b极发生的电极反应方程式为:Cu+Cl--e-═CuCl↓.
(5)12min后,b极附近出现的橙黄色沉淀的成分是CuOH和Cu2O,原因是Ksp(CuOH)<Ksp(CuCl),CuCl转化为黄色的CuOH沉淀,CuOH不稳定分解生成Cu2O,所以橙黄色沉淀的成分为CuOH和Cu2O的混合物.
| Cu(OH)2 | CuOH | CuCl | Cu2O | |
| 颜色 | 蓝色 | 黄色 | 白色 | 砖红色 |
| Ksp(25℃) | 1.6×10-19 | 1.0×10-14 | 1.2×10-6 | - |

实验Ⅰ:装置如图所示,接通电源后,发现a、b电极上均有气泡产生.
(1)电解过程中的总离子反应方程式为2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑.
(2)为了确定电源的正、负极,下列操作一定行之有效的是BD.
A.观察两极产生气体的颜色
B.往U形管两端分别滴入数滴酚酞试液
C.用燃着的木条靠近U形管口
D.在U形管口置一张湿润的淀粉KI试纸
实验Ⅱ:把上述电解装置的石墨棒换成铜棒,用直流电源进行电解,装置如图所示.
观察到的现象如下所示:
①开始无明显现象,随后液面以下的铜棒表面逐渐变暗;
②5min后,b极附近开始出现白色沉淀,并逐渐增多,且向a极扩散;
③10min后,最靠近a极的白色沉淀开始变成红色;
④12min后,b极附近的白色沉淀开始变成黄色,然后逐渐变成橙黄色;
⑤a极一直有大量气泡产生;
⑥停止电解,将U形管中悬浊液静置一段时间后,上层溶液呈无色,没有出现蓝色,下层沉淀全部显砖红色.
(3)a极发生的电极反应方程式为:2H++2e-=H2↑(或2H2O+2e-═2OH-+H2↑).
(4)电解5min后,b极发生的电极反应方程式为:Cu+Cl--e-═CuCl↓.
(5)12min后,b极附近出现的橙黄色沉淀的成分是CuOH和Cu2O,原因是Ksp(CuOH)<Ksp(CuCl),CuCl转化为黄色的CuOH沉淀,CuOH不稳定分解生成Cu2O,所以橙黄色沉淀的成分为CuOH和Cu2O的混合物.
6.铜及其化合物在工农业生产及日常生活中应用非常广泛.某研究小组用粗铜(含杂质铁)制备氯化铜晶体(CuCl2•2H2O )的流程如下.

已知常温下,Cu2+、Fe3+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
请回答下列问题:
(1)溶液I中加入试剂X可以调节溶液pH,从而除去Fe3+且不引入杂质.
①试剂X可选用下列物质中的bd(填代号).
a.CuO b.NaOH c.Cu d..Cu(OH)2
②调节溶液pH时,理论上可选择pH最大范围是3.2≤pH<4.7.
(2)由溶液Ⅱ制备CuCl2•2H2O的操作依次为:边滴加浓盐酸边加热浓缩、冷却结晶(填操作名称)、过滤、洗涤干燥.
(3)向溶液Ⅱ中通入H2S气体,溶液变浑浊,pH减小,用离子方程式解释其原因:H2S+Cu2+=CuS↓+2H+.
(4)某学习小组用碘量法测定CuCl2•2H2O样品的纯度(杂质不与发生反应).实验如下:
a.准确称取CuCl.•2H2O样品mg于小烧杯中,加入适量蒸馏水和足量的碘化钾,再滴
入适量的稀硫酸,充分反应后,将所得混合液配成250mL待测溶液.
(已知:2Cu2++4I-=2CuI↓+I2)
b.移取25.00mL待测溶液于锥形瓶中,加几滴指示剂,用c mol•L-1Na2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为V mL.
(已知:I2+2S2O32-=2I-+S4O62-)
①实验中使用的指示剂名称为淀粉溶液.
②达到滴定终点时,仰视滴定管读数将使测定结果偏高(填“偏高”、“偏低”或“无影响”).
③该样品中CuCl2•2H2O 的质量分数为$\frac{171cV×1{0}^{-3}×10}{m}$×100%(用含m、c、V的代数式表示,不用化简).

已知常温下,Cu2+、Fe3+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
| 金属离子 | Fe3+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 1.9 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 6.7 |
(1)溶液I中加入试剂X可以调节溶液pH,从而除去Fe3+且不引入杂质.
①试剂X可选用下列物质中的bd(填代号).
a.CuO b.NaOH c.Cu d..Cu(OH)2
②调节溶液pH时,理论上可选择pH最大范围是3.2≤pH<4.7.
(2)由溶液Ⅱ制备CuCl2•2H2O的操作依次为:边滴加浓盐酸边加热浓缩、冷却结晶(填操作名称)、过滤、洗涤干燥.
(3)向溶液Ⅱ中通入H2S气体,溶液变浑浊,pH减小,用离子方程式解释其原因:H2S+Cu2+=CuS↓+2H+.
(4)某学习小组用碘量法测定CuCl2•2H2O样品的纯度(杂质不与发生反应).实验如下:
a.准确称取CuCl.•2H2O样品mg于小烧杯中,加入适量蒸馏水和足量的碘化钾,再滴
入适量的稀硫酸,充分反应后,将所得混合液配成250mL待测溶液.
(已知:2Cu2++4I-=2CuI↓+I2)
b.移取25.00mL待测溶液于锥形瓶中,加几滴指示剂,用c mol•L-1Na2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为V mL.
(已知:I2+2S2O32-=2I-+S4O62-)
①实验中使用的指示剂名称为淀粉溶液.
②达到滴定终点时,仰视滴定管读数将使测定结果偏高(填“偏高”、“偏低”或“无影响”).
③该样品中CuCl2•2H2O 的质量分数为$\frac{171cV×1{0}^{-3}×10}{m}$×100%(用含m、c、V的代数式表示,不用化简).
4.下列对分子及其性质的解释中,不正确的是( )
| A. | 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 | |
| B. | 乳酸[CH3CH(OH)COOH]中存在一个手性碳原子 | |
| C. | 许多过渡金属离子对多种配体具有很强的结合力,因而,只有过渡金属才能形成配合物 | |
| D. | 已知酸性:H3PO4>HClO,是因为H3PO4分子中有1个非羟基氧原子而HClO为0 |
3.现有四种元素的基态原子的电子排布式如下:①[Ne]3s23p4;②1s22s22p63s23p3;③1s22s22p5.则下列有关比较中正确的是( )
0 154959 154967 154973 154977 154983 154985 154989 154995 154997 155003 155009 155013 155015 155019 155025 155027 155033 155037 155039 155043 155045 155049 155051 155053 155054 155055 155057 155058 155059 155061 155063 155067 155069 155073 155075 155079 155085 155087 155093 155097 155099 155103 155109 155115 155117 155123 155127 155129 155135 155139 155145 155153 203614
| A. | 最高正化合价:③>②>① | B. | 单质氧化性:③>①>② | ||
| C. | 电负性:③>②>① | D. | 原子半径:③>②>① |