11.X、Y、Z、W是元素周期表前四周期中常见的元素,其相关信息如下表:
(1)W位于元素周期表第四周期第Ⅷ族.
(2)X的电负性比Y的小(填“大”或“小”);
(3)X 和Y的气态氢化物中,熔沸点较高的是H2O(写化学式).原因:H2O分子间形成氢键
(4)写出Z2Y2与XY2反应的化学方程式,并标出电子转移的方向和数目: .
.
| 元素 | 相关信息 |
| X | X的基态原子L层电子数是K层电子数的2倍 |
| Y | Y的基态原子最外层电子排布式为:nsnnpn+2 |
| Z | Z存在质量数为23,中子数为12的核素 |
| W | W有多种化合价,其白色氢氧化合物在空气中会迅速变成灰绿色,最后变成红褐色 |
(2)X的电负性比Y的小(填“大”或“小”);
(3)X 和Y的气态氢化物中,熔沸点较高的是H2O(写化学式).原因:H2O分子间形成氢键
(4)写出Z2Y2与XY2反应的化学方程式,并标出电子转移的方向和数目:
 .
.
10.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4L二氯甲烷的分子数约为NA个 | |
| B. | 1mol冰中有2mol氢键 | |
| C. | 17.6g丙烷中所含的极性共价键为3.2NA个 | |
| D. | 1molH3O+含有11mol电子 |
9.下列叙述中能肯定说明金属A比金属B的活泼性强的是( )
| A. | A原子最外层电子数比B原子的最外层电子数少 | |
| B. | 将A、B组成原电池时,A为正极 | |
| C. | 1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多 | |
| D. | 将A和B用导线相连接,一同放入CuSO4溶液中,B的表面有红色的铜析出 |
8.在下列各组化合物中,化学键类型相同的是( )
| A. | HCl和MgCl2 | B. | H2O和CO2 | C. | CO2和NaCl | D. | F2和NaF |
7.维生素A对人体,特别是对人的视力有重大作用,其结构简式如图所示: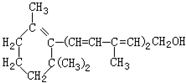
下列关于该化合物的说法正确的是( )

下列关于该化合物的说法正确的是( )
| A. | 维生素A的分子式为C16H25O | |
| B. | 维生素A含有苯环结构 | |
| C. | 维生素A的一个分子中有3个双键 | |
| D. | 维生素A的分子中含有两种官能团 (维生素A的结构简式) |
5.微型钮扣电池在现代生活中有广泛应用.有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为:Zn+2OH--2e-=ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH-
根据上述反应式,判断下列叙述中正确的是( )
根据上述反应式,判断下列叙述中正确的是( )
| A. | 在使用过程中,电池负极区溶液的pH增大 | |
| B. | 使用过程中,电子由Ag2O极经外电路流向Zn极 | |
| C. | Zn是负极,Ag2O是正极 | |
| D. | Zn电极发生还原反应,Ag2O电极发生氧化反应 |
4.日本福岛第一核电站发生严重的核辐射泄漏,日本政府向福岛核电站附近居民发放碘片(12753I),以降低放射性碘对人体的伤害.已知核辐射中放射性碘(碘13153I)的核电荷数为53,则下列说法正确的是( )
| A. | 核裂变是一种化学变化 | |
| B. | 12753I的质量数为127,原子序数为53,核内有74个中子 | |
| C. | 碘12753I和放射性碘13153I属于同素异形体 | |
| D. | 12753I与13153I是同一种核素 |
3.关于反应N2+3H2$?_{△}^{催化剂}$2NH3的说法错误的是( )
0 154955 154963 154969 154973 154979 154981 154985 154991 154993 154999 155005 155009 155011 155015 155021 155023 155029 155033 155035 155039 155041 155045 155047 155049 155050 155051 155053 155054 155055 155057 155059 155063 155065 155069 155071 155075 155081 155083 155089 155093 155095 155099 155105 155111 155113 155119 155123 155125 155131 155135 155141 155149 203614
| A. | 外界条件可以改变平衡状态 | B. | 达到平衡时正、逆反应速率相等 | ||
| C. | 平衡时各组分的含量也在不断变化 | D. | 该反应所建立的平衡是动态平衡 |
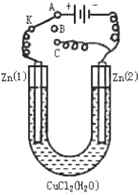 在一个U形管里盛有氯化铜溶液,并插入两块锌片作电极,按如图连接:
在一个U形管里盛有氯化铜溶液,并插入两块锌片作电极,按如图连接: