18.下表是元素周期表的一部分,表中序号分别代表某一元素.请回答下列问题.
(1)①-⑩中,最活泼的金属元素是Na(写元素符号,下同);最不活泼的元素是Ar;可作半导体材料的元素是Si;某元素的气态氢化物与其最高价氧化物的水化物可直接 化合生成一种盐,该元素是N.
(2)④、⑤的简单离子,其半径更大的是F-(写离子符号).
(3)⑧、⑨的气态氢化物,更稳定的是HCl(填化学式).
(4)元素的非金属性:①>⑦(填“>”或“<”).
(5)①-⑨的最高价氧化物的水化物中:酸性最强的是HClO4(填化学式);碱性最强的是NaOH(填化学式),它与⑨的最高价氧化物的水化 物反应的化学方程式为HClO4+NaOH=NaClO4+H2O.
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)④、⑤的简单离子,其半径更大的是F-(写离子符号).
(3)⑧、⑨的气态氢化物,更稳定的是HCl(填化学式).
(4)元素的非金属性:①>⑦(填“>”或“<”).
(5)①-⑨的最高价氧化物的水化物中:酸性最强的是HClO4(填化学式);碱性最强的是NaOH(填化学式),它与⑨的最高价氧化物的水化 物反应的化学方程式为HClO4+NaOH=NaClO4+H2O.
17.硫黄制酸在我国的工业发展进程中具有重要地位,其工业流程示意图如下.已知硫磺的燃烧热△H=-297kJ•mol-1.下列说法正确的是( )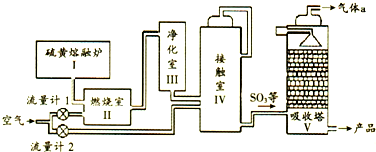

| A. | Ⅱ中主要反应的热化学方程式:S(s)+O2(g)?SO3(g)△H=-297kJ•mol-1S(s)+O2(s)=SO2(g)△H=-297kJ•mol-1 | |
| B. | Ⅳ中主要反应的化学方程式:2SO2+O2(s) $?_{△}^{催化剂}$SO3 | |
| C. | Ⅳ中使用催化剂可提高化学反应速率和平衡转化率 | |
| D. | Ⅴ中气体a 可以直接排放到大气中 |
16.利用下列实验装置能完成相应实验的是( )
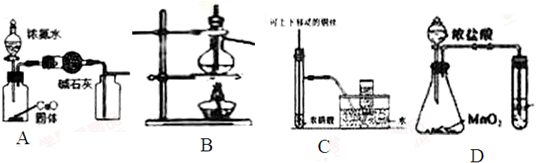

| A. | 制取并收集干燥纯净的NH3 | B. | 分离Br2和CCl4的混合物 | ||
| C. | 用于制备并收集少量NO | D. | 比较MnO2、Cl2、S 的氧化性 |
14.下表是元素周期表的一部分,回答下列问题:
(1)写出①、③两种元素形成的化合物有两种,其化学式分别为:CO,CO2.
(2)写出①元素最高价氧化物的电子式和结构式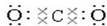 ,O=C=O.
,O=C=O.
(3)这些元素的最高价氧化物的对应水化物中HClO4酸性最强;NaOH碱性最强;能形成两性氢氧化物的元素是Al.
(4)序号④⑤⑪的元素组成的化合物为NaClO,写出电子式 .
.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | O |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(2)写出①元素最高价氧化物的电子式和结构式
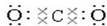 ,O=C=O.
,O=C=O.(3)这些元素的最高价氧化物的对应水化物中HClO4酸性最强;NaOH碱性最强;能形成两性氢氧化物的元素是Al.
(4)序号④⑤⑪的元素组成的化合物为NaClO,写出电子式
 .
.
10.下列说法错误的是( )
| A. | 金属的冶炼方法有4种,其中铝热反应属于热分解法 | |
| B. | 海带中碘元素的检验原理:2H++2I-+H2O2=I2+2H2O | |
| C. | 石油的分馏,裂化,裂解,催化重整中裂化是物理变化 | |
| D. | 铝热反应中铝做还原剂 |
9.下列有机反应中,不属于取代反应的是( )
0 154936 154944 154950 154954 154960 154962 154966 154972 154974 154980 154986 154990 154992 154996 155002 155004 155010 155014 155016 155020 155022 155026 155028 155030 155031 155032 155034 155035 155036 155038 155040 155044 155046 155050 155052 155056 155062 155064 155070 155074 155076 155080 155086 155092 155094 155100 155104 155106 155112 155116 155122 155130 203614
| A. | 乙醇与乙酸的反应 | |
| B. | 蛋白质的水解反应 | |
| C. | 苯和浓硝酸、浓硫酸混合液在50-60℃水浴中发生的反应 | |
| D. | 乙烯使溴水褪色 |
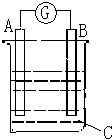 请根据如图所示回答:甲装置是由铜、锌和硫酸铜组成的原电池,
请根据如图所示回答:甲装置是由铜、锌和硫酸铜组成的原电池,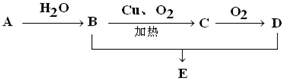 如图所示,已知A的产量是一个国家石油化工水平的标志,D具有酸性.E是具有香味的不溶于水的液体.
如图所示,已知A的产量是一个国家石油化工水平的标志,D具有酸性.E是具有香味的不溶于水的液体. 2,3,4-三甲基己烷,
2,3,4-三甲基己烷, 3-甲基-3-乙基己烷,
3-甲基-3-乙基己烷, 3,3-二甲基-4-乙基-3-己烯,
3,3-二甲基-4-乙基-3-己烯, 2,3-二甲基-2-丁烯.
2,3-二甲基-2-丁烯.