8.下列叙述中正确的是( )
| A. | 共价化合物分子中的化学键可能含有离子键 | |
| B. | 含有金属元素的化合物-定是离子化合物 | |
| C. | 需要加热才能发生的反应是吸热反应 | |
| D. | 反应是吸热还是放热必须看旧键断裂时吸收的能量和新键生成时释放的能量的大小 |
7.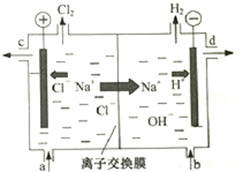 氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.
氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.
完成下列填空:
(1)写出电解饱和食盐水的离子方程式2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑.
(2)精制饱和食盐水从图中a位置补充,氢氧化钠溶液从图中d位置流出.(选填“a”、“b”、“c”或“d”)
(3)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质.写出该反应的化学方程式2KClO3+H2C2O4+2H2SO4=2ClO2+2CO2+2KHSO4+2H2O.
(4)已知室温下几种弱酸的平衡常数:
则0.1mol/L NaClO溶液的pH>0.1mol/L Na2SO3溶液的pH.(选填“大于”、“小于”或“等于”).浓度均为0.1mol/L的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3- 浓度从大到小的顺序为c(SO32-)>c(CO32-)c(HCO3-)>c(HSO3-).
 氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.
氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品.如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过.完成下列填空:
(1)写出电解饱和食盐水的离子方程式2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑.
(2)精制饱和食盐水从图中a位置补充,氢氧化钠溶液从图中d位置流出.(选填“a”、“b”、“c”或“d”)
(3)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质.写出该反应的化学方程式2KClO3+H2C2O4+2H2SO4=2ClO2+2CO2+2KHSO4+2H2O.
(4)已知室温下几种弱酸的平衡常数:
| K1 | K2 | |
| H2SO3 | 1.54x 10-2 | 1.02x 10-7 |
| HClO | 2.95x 10-8 | |
| H2CO3 | 4.3x 10-7 | 5.6x 10-11 |
2.25℃时,在10mL浓度均为0.1mol/L NaOH和NH3•H2O混合溶液中,滴加0.1mol/L的盐酸,下列有关溶液中粒子浓度关系正确的是( )
| A. | 未加盐酸时,c (Na+)+c(OH-)=c(NH3•H2O) | |
| B. | 加入10mL盐酸时,c(NH4+)+c(H+)=c(OH-) | |
| C. | 加入盐酸至溶液pH=7时:c(Cl-)=c (Na+) | |
| D. | 加入20mL盐酸时,c(Cl-)=c(NH4+)+c (Na+) |
1.25℃时,将0.05mol Na2CO3固体溶于水配成100mL溶液,向溶液中加入下列物质.有关结论正确的是
( )
( )
| 加入的物质 | 结论 | |
| A | 50mL 1mol/L H2SO4 | 反应结束后,c(Na+)=c(SO42-) |
| B | 0.5mol CaO | 若反应完全后溶液的体积仍为100mL,则溶液的pH约为14 |
| C | 50mL H2O | c(Na+)=2[c(CO32-)+c(HCO3-)] |
| D | 0.1mol NaHSO4 | 反应完全后,溶液pH减小,c (Na+)不变 |
| A. | A | B. | B | C. | C | D. | D |
20.25℃时,用如图所示装置除去含CN-、Cl-废水中CN-时,控制pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是( )

| A. | 可用石墨做阳极,铁做阴极 | |
| B. | 阳极的电极反应式:Cl-+2OH--2e-=ClO-+H2O | |
| C. | 若铁做阴极,则电解过程中溶液中的阳离子向铁电极运动 | |
| D. | 除去CN-的反应,2CN-+5ClO-+2H+=N2↑+2CO2↑+5Cl-+H2O |
19.25℃时,水的电离达到平衡,H2O?H++OH-△H>0,下列说法正确的是( )
0 154935 154943 154949 154953 154959 154961 154965 154971 154973 154979 154985 154989 154991 154995 155001 155003 155009 155013 155015 155019 155021 155025 155027 155029 155030 155031 155033 155034 155035 155037 155039 155043 155045 155049 155051 155055 155061 155063 155069 155073 155075 155079 155085 155091 155093 155099 155103 155105 155111 155115 155121 155129 203614
| A. | 向水中加入稀氨水,水的电离平衡逆向移动,c(OH-)减小 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变 | |
| C. | 向水中加入少量固体CH3COO Na,水的电离平衡逆向移动,c(H+)减小 | |
| D. | 将水加热,KW增大,pH不变 |
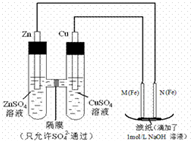 某课外小组分别用如图所示装置对原电池和电解原理进行实验探究.
某课外小组分别用如图所示装置对原电池和电解原理进行实验探究.