8.设NA为阿伏伽德罗常数,根据Cu+4NNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,则下列叙述正确的是( )
| A. | 22.4LNO2含电子总数为23NA | |
| B. | 3.6gH2O中含有共价键的总数为0.2NA | |
| C. | 若生成的硝酸铜浓度为2mol/L,则1L该溶液中含有的Cu2+数为2N | |
| D. | 若有2molCu参与反应,则有4molHNO3被还原 |
7.关于明矾的叙述正确的是( )
| A. | 明矾投入水中的电离方程式为:KAI(SO4)2•12H2O=K++Al3++2SO42-+12H20,说明明矾是一种混合物 | |
| B. | 净水时Al3+发生水解生成的是Al(OH)3沉淀 | |
| C. | 明矾净水的原理是杀菌消毒 | |
| D. | 硫酸铁可以代替明矾进行净水 |
6.下列叙述正确的是( )
| A. | 乙醛和甲酸两者都能发生银镜反应,所以它们互为同系物 | |
| B. | 营养物质中的多糖、油脂、蛋白质在一定条件下都可以发生水解 | |
| C. | 氨基酸和氯乙烯都能通过加聚反应生成高分子化合物 | |
| D. | 通过对煤的分馏,可以提高煤的利用率 |
3.要证明CuSO4溶液显蓝色不是由于SO42-造成的,下列实验无意义的是( )
| A. | 观察K2SO4溶液的颜色 | |
| B. | 加水稀释CuSO4溶液,溶液颜色变浅 | |
| C. | 向CuSO4溶液中滴加过量NaOH溶液,振荡后静置,溶液变成无色 | |
| D. | 向CuSO4溶液中滴加过量Ba(NO3)2溶液,振荡后静置,溶液未变成无色 |
2.某同学用如图所示的装置及药品进行比较酸性强弱的实验,一段时间后试管②中有胶冻状物质生成.下列说法正确的是( )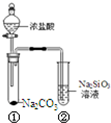

| A. | 向Na2SiO3溶液中滴入酚酞溶液无明显现象 | |
| B. | 试管①中反应的离子方程式是:Na2CO3+2H+═2Na++CO2↑+H2O | |
| C. | 该实验可以证明酸性:盐酸>碳酸>硅酸 | |
| D. | 若将盐酸换成硫酸,能证明酸性:硫酸>碳酸>硅酸 |
1.下列实验事实得出的结论不正确的是( )
| 选项 | 实验事实 | 结论 |
| A | H2可在Cl2中燃烧产生苍白色的火焰 | 燃烧不一定有氧气参加 |
| B | 铝箔在酒精灯火焰上加热融化但不滴落 | 氧化铝熔点高于铝 |
| C | 将SO2通入酸性KMnO4溶液中,酸性KMnO4溶液褪色 | SO2具有漂白性 |
| D | 去黄豆粒大小的钠与水反应,钠熔化成闪亮的小球,浮在水面,不断游动,嘶嘶作响,最后消失 | 钠熔点低、密度比水小,放热,具有强还原性 |
| A. | A | B. | B | C. | C | D. | D |
20.能在溶液中大量共存的一组离子是( )
| A. | Cu2+、SO42-、OH-、K+ | B. | Fe3+、SCN-、Cl-、H+ | ||
| C. | K+、CO32-、Cl-、H+ | D. | H+、Na+、Cl-、SO42- |
19.解释下列事实的方程式不正确的是( )
0 154929 154937 154943 154947 154953 154955 154959 154965 154967 154973 154979 154983 154985 154989 154995 154997 155003 155007 155009 155013 155015 155019 155021 155023 155024 155025 155027 155028 155029 155031 155033 155037 155039 155043 155045 155049 155055 155057 155063 155067 155069 155073 155079 155085 155087 155093 155097 155099 155105 155109 155115 155123 203614
| A. | Al溶于NaOH溶液:2Al+2H2O+2NaOH═2NaAlO2+3H2↑ | |
| B. | 盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH-═SiO32-+H2O | |
| C. | 向FeCl3溶液中滴加淀粉碘化钾溶液,溶液变蓝:2Fe3++2I-═2Fe2++I2 | |
| D. | 红热的Fe丝与水接触,表面形成蓝黑色保护层:2Fe+3H2O(g) $\frac{\underline{\;\;△\;\;}}{\;}$ Fe2O3+3H2↑ |
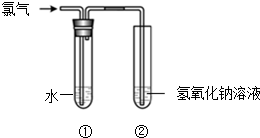 某同学用如图所示装置制取氯水并进行相关实验.
某同学用如图所示装置制取氯水并进行相关实验.