8. 自然界中存在大量的金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用.
自然界中存在大量的金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用.
(1)请写出Fe的基态原子核外电子排布式1s22s22p63s23p63d64s2或[Ar]3d64s2.
(2)金属A的原子只有3个电子层,其第一至第四电离能如表:
则A原子的价电子排布式为3s2.
(3)合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气体中的CO(Ac-代表CH3COO-),其反应是:[Cu(NH3)2]Ac+CO+NH3?[Cu(NH3)3CO]Ac[醋酸羰基三安合铜(I)]△H<0
①C、N、O三种元素的第一电离能由小到大的顺序为C<O<N
②配合物[Cu(NH3)3CO]Ac中心原子的配位数为4
③在一定条件下NH3与CO2能合成尿素[CO(NH2)2],尿素中C原子核N原子轨道的杂化类型分别为sp2、sp3;1mol尿素分子中,σ键的数目为7NA.
(4)NaCl和MgO都属于离子化合物,NaCl的熔点为801.3℃,MgO的熔点高达2800℃.造成两种晶体熔点差距的主要原因是MgO晶体所含离子半径小,电荷数多,晶格能大.
(5)(NH4)2SO4、NH4NO3等颗粒物及扬尘等易引起雾霾.其中NH4-的空间构型是正四面体(用文字描述),与NO3-互为等电子体的分子是SO3或者BF3.(填化学式)
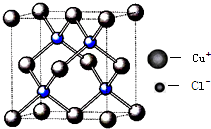
(6)铜的化合物种类很多,如图是氢化亚铜的晶胞结构,已知晶胞的棱长为acm,则氢化亚铜密度的计算式为ρ=$\frac{260}{{a}^{3}•{N}_{A}}$g/cm3.(用NA表示阿佛加德罗常数)
 自然界中存在大量的金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用.
自然界中存在大量的金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用.(1)请写出Fe的基态原子核外电子排布式1s22s22p63s23p63d64s2或[Ar]3d64s2.
(2)金属A的原子只有3个电子层,其第一至第四电离能如表:
| 电离能(KJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
(3)合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气体中的CO(Ac-代表CH3COO-),其反应是:[Cu(NH3)2]Ac+CO+NH3?[Cu(NH3)3CO]Ac[醋酸羰基三安合铜(I)]△H<0
①C、N、O三种元素的第一电离能由小到大的顺序为C<O<N
②配合物[Cu(NH3)3CO]Ac中心原子的配位数为4
③在一定条件下NH3与CO2能合成尿素[CO(NH2)2],尿素中C原子核N原子轨道的杂化类型分别为sp2、sp3;1mol尿素分子中,σ键的数目为7NA.
(4)NaCl和MgO都属于离子化合物,NaCl的熔点为801.3℃,MgO的熔点高达2800℃.造成两种晶体熔点差距的主要原因是MgO晶体所含离子半径小,电荷数多,晶格能大.
(5)(NH4)2SO4、NH4NO3等颗粒物及扬尘等易引起雾霾.其中NH4-的空间构型是正四面体(用文字描述),与NO3-互为等电子体的分子是SO3或者BF3.(填化学式)
(6)铜的化合物种类很多,如图是氢化亚铜的晶胞结构,已知晶胞的棱长为acm,则氢化亚铜密度的计算式为ρ=$\frac{260}{{a}^{3}•{N}_{A}}$g/cm3.(用NA表示阿佛加德罗常数)
7. 亚硝酸钠是一种工业盐,外观与食盐非常相似,毒性较强.某化学兴趣小组对食盐与亚硝酸钠进行多角度探究:
亚硝酸钠是一种工业盐,外观与食盐非常相似,毒性较强.某化学兴趣小组对食盐与亚硝酸钠进行多角度探究:
(一)鉴别NaCl和NaNO2
甲同学用沉淀分析法:
经查:常温下Ksp(AgNO2)=2×10-8,Ksp(AgCl)=1.8×10-10.分别向盛有5mL 0.0001mol/L两种盐溶液的试合中同时逐滴滴加0.0001mol/L硝酸银溶液,先生成沉淀的是装有NaCl溶液的试管.
乙同学侧定溶液pH:
用pH试纸分别测定0.1mol/L两种盐溶液的pH,测得NaNO2溶液呈碱性.该溶液呈碱性的原因是NO2-+H2O?HNO2+OH-(用离子方程式解释).
(二)该小组用如图装置(略去夹持仪器)制备亚硝酸钠
已知:①2NO+Na2O2=2NaNO2;
②酸性条件下,NO和NO2都能与MnO4一反应生成NO3一和Mn2+•
(1)使用铜丝的优点是可以控制反应的发生与停止.
(2)装置A中反应方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O.
装置C 中盛放的药品是C;(填字母代号)
A.浓硫酸 B.NaOH 溶液 C.水 D.四氯化碳
仪器F的作用防止水蒸气进入.
(3)该小组称取5.000g制取的样品溶于水配成250.0mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol/L酸性KMnO4溶液进行滴定,实验所得数据如表所示:
①第一次实验数据出现异常,造成这种异常的原因可能是bc(填字母代号).
a.锥形瓶洗净后未干燥
b.酸式滴定管用蒸馏水洗净后未用标准液润洗
c.滴定终点时仰视读数
②酸性KMnO4溶液滴定亚硝酸钠溶液的离子方程式为2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O.
③该样品中亚硝酸钠的质量分数为69.0%.
 亚硝酸钠是一种工业盐,外观与食盐非常相似,毒性较强.某化学兴趣小组对食盐与亚硝酸钠进行多角度探究:
亚硝酸钠是一种工业盐,外观与食盐非常相似,毒性较强.某化学兴趣小组对食盐与亚硝酸钠进行多角度探究:(一)鉴别NaCl和NaNO2
甲同学用沉淀分析法:
经查:常温下Ksp(AgNO2)=2×10-8,Ksp(AgCl)=1.8×10-10.分别向盛有5mL 0.0001mol/L两种盐溶液的试合中同时逐滴滴加0.0001mol/L硝酸银溶液,先生成沉淀的是装有NaCl溶液的试管.
乙同学侧定溶液pH:
用pH试纸分别测定0.1mol/L两种盐溶液的pH,测得NaNO2溶液呈碱性.该溶液呈碱性的原因是NO2-+H2O?HNO2+OH-(用离子方程式解释).
(二)该小组用如图装置(略去夹持仪器)制备亚硝酸钠
已知:①2NO+Na2O2=2NaNO2;
②酸性条件下,NO和NO2都能与MnO4一反应生成NO3一和Mn2+•
(1)使用铜丝的优点是可以控制反应的发生与停止.
(2)装置A中反应方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O.
装置C 中盛放的药品是C;(填字母代号)
A.浓硫酸 B.NaOH 溶液 C.水 D.四氯化碳
仪器F的作用防止水蒸气进入.
(3)该小组称取5.000g制取的样品溶于水配成250.0mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol/L酸性KMnO4溶液进行滴定,实验所得数据如表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| 消耗KMnO4溶液体积/mL | 20.70 | 20.12 | 20.00 | 19.88 |
a.锥形瓶洗净后未干燥
b.酸式滴定管用蒸馏水洗净后未用标准液润洗
c.滴定终点时仰视读数
②酸性KMnO4溶液滴定亚硝酸钠溶液的离子方程式为2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O.
③该样品中亚硝酸钠的质量分数为69.0%.
6.化学与社会、生活密切相关,下列说法中正确的是( )
| A. | “歼-20”飞机上使用的碳纤维是一种新型的有机高分子材料 | |
| B. | 燃料电池中燃料都在负极发生氧化反应 | |
| C. | Fe3O4俗称铁红,常作红色油漆和涂料 | |
| D. | 工业上通常用电解Na、Mg、Al对应的氯化物制取该三种金属单质 |
5. 常温下,向20.00mL0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol•L-1的NaOH溶液,pH随NaOH溶液体积的变化如图所示.下列说法不正确的是( )
常温下,向20.00mL0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol•L-1的NaOH溶液,pH随NaOH溶液体积的变化如图所示.下列说法不正确的是( )
 常温下,向20.00mL0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol•L-1的NaOH溶液,pH随NaOH溶液体积的变化如图所示.下列说法不正确的是( )
常温下,向20.00mL0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol•L-1的NaOH溶液,pH随NaOH溶液体积的变化如图所示.下列说法不正确的是( )| A. | 在反应过程中,c(Na+)+c(H+)=c(CH3COO-)+c(OH-) | |
| B. | pH=5时,c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| C. | pH=6时,c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1000 mol•Lˉ1 | |
| D. | pH=7时,消耗NaOH溶液的体积小于20.00mL |
4.用NA表示阿伏德罗常数,下列叙述正确的是( )
| A. | 标准状况下,22.4L H2O含有的分子数为 NA | |
| B. | 通常状况下,NA 个CO2分子占有的体积为22.4L | |
| C. | 将等物质的量的SO3和SO2溶于水,所得溶液中H+数目相等 | |
| D. | 常温常压下,1.06g Na2CO3溶于水形成的溶液中含有Na+离子数为0.02 NA |
3.下列气体中不属于大气污染物的是( )
| A. | O3 | B. | SO2 | C. | CO | D. | N2 |
2.下列物质的颜色不是黑色的是( )
| A. | 还原Fe粉 | B. | FeO | C. | Fe3O4 | D. | Fe2O3 |
1.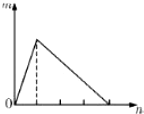 将溶液(或气体)X逐渐加入(或通入)到一定量Y溶液中,产生沉淀的量m与加入X的物质的量n的关系如图所示,符合图中情况的一组物质是( )
将溶液(或气体)X逐渐加入(或通入)到一定量Y溶液中,产生沉淀的量m与加入X的物质的量n的关系如图所示,符合图中情况的一组物质是( )
 将溶液(或气体)X逐渐加入(或通入)到一定量Y溶液中,产生沉淀的量m与加入X的物质的量n的关系如图所示,符合图中情况的一组物质是( )
将溶液(或气体)X逐渐加入(或通入)到一定量Y溶液中,产生沉淀的量m与加入X的物质的量n的关系如图所示,符合图中情况的一组物质是( )| A | B | C | D | |
| X | Ba(OH)2 | NaOH | NH3 | HCl |
| Y | 明矾 | AlCl3 | MgSO4 | NaAlO2 |
| A. | A | B. | B | C. | C | D. | D |
20.下列物质不是黄色或淡黄色的是( )
| A. | 单质硫 | B. | 过氧化钠 | C. | 氢氧化铁胶体 | D. | 三氯化铁稀溶液 |
19.密度为0.910g/cm3的氨水,质量分数为25.0%,该氨水用等体积的水稀释后,所得溶液的质量分数为( )
0 154923 154931 154937 154941 154947 154949 154953 154959 154961 154967 154973 154977 154979 154983 154989 154991 154997 155001 155003 155007 155009 155013 155015 155017 155018 155019 155021 155022 155023 155025 155027 155031 155033 155037 155039 155043 155049 155051 155057 155061 155063 155067 155073 155079 155081 155087 155091 155093 155099 155103 155109 155117 203614
| A. | 等于12.5% | B. | 大于12.5% | C. | 小于12.5% | D. | 无法确定 |