20.在1L溶液中含有Fe(NO3)3和H2SO4两种溶质,其浓度分别为0.2mol/L和1.5mol/L,现向该溶液中加入39.2g铁粉使其充分反应.下列有关说法正确的是( )
| A. | 反应后溶液中H+剩余 1.8mol | |
| B. | 由于氧化性Fe3+>H+,故反应中先没有气体产生后产生气体 | |
| C. | 反应后产生13.44L H2(标准状况) | |
| D. | 反应后溶液中Fe2+和Fe3+物质的量之和为0.9mol |
19.标准状况下,某同学向100mLH2S饱和溶液中通入SO2,所得溶液pH变化如图所示,下列分析中,正确的是( )
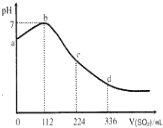

| A. | b 点对应的溶液导电性最强 | |
| B. | 亚硫酸是比氧硫酸更弱的酸 | |
| C. | 原H2S溶液的物质的量浓度为0.05mol•L-1 | |
| D. | ab段反应是:SO2+2H2S═3S↓+2H2O |
18.下列说法正确的是( )
| A. | 足量Cu与浓硫酸反应后,向溶液中加入NaNO3,无任何现象 | |
| B. | 实验室检验氨气是将湿润的蓝色石蕊试纸靠近瓶口或管口,观察试纸是否呈红色 | |
| C. | 灼热的铂丝与NH3、O2混合气接触,铂丝持续红热,说明氮的氧化反应是放热反应 | |
| D. | 大气污染气体很难处理,是因为NO等在空气中都能稳定存在 |
17.25℃时,在某物质的溶液中,由水电离出的c(H+)=1×10-amol/L,下列说法正确的是( )
| A. | a<7时,水的电离受到抑制 | B. | a>7时,水的电离受到抑制 | ||
| C. | a<7时,溶液的pH一定为a | D. | a>7时,溶液的pH一定为14-a |
14.对于常温下pH均为4的三种溶液:①盐酸,②CH3COOH溶液,③NH4Cl溶液,下列说法中正确的是( )
| A. | 溶液中由水电离出的c(H+):②>③ | |
| B. | 稀释100倍后溶液的pH:①<③ | |
| C. | 中和相同体积的上述溶液消耗NaOH溶液的体积:①<② | |
| D. | ②和③等体积混合后的溶液:c(CH3COO-)+c(Cl-)=c(NH4+) |
13.下列物质属于可溶性的是( )
| A. | Fe(OH)3 | B. | Cu(OH)2 | C. | Al(OH)3 | D. | Ba(OH)2 |
12.下列电离方程式正确的是( )
| A. | NH4Cl=NH4++Cl- | B. | NaHSO4=Na++HSO42- | ||
| C. | H2CO3=2H++CO32- | D. | CH3COOH→CH3++COOH- |
11.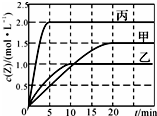 向甲、乙、丙三个容积固定不变的密闭容器中充入一定量的X和Y,一定条件下发生反应 X(g)+aY(g)?2Z(g).各容器的反应温度、反应物起始量、反应过程中Z的浓度随时间变化分别以如图和下表来表示.下列说法不正确的是( )
向甲、乙、丙三个容积固定不变的密闭容器中充入一定量的X和Y,一定条件下发生反应 X(g)+aY(g)?2Z(g).各容器的反应温度、反应物起始量、反应过程中Z的浓度随时间变化分别以如图和下表来表示.下列说法不正确的是( )
0 154872 154880 154886 154890 154896 154898 154902 154908 154910 154916 154922 154926 154928 154932 154938 154940 154946 154950 154952 154956 154958 154962 154964 154966 154967 154968 154970 154971 154972 154974 154976 154980 154982 154986 154988 154992 154998 155000 155006 155010 155012 155016 155022 155028 155030 155036 155040 155042 155048 155052 155058 155066 203614
 向甲、乙、丙三个容积固定不变的密闭容器中充入一定量的X和Y,一定条件下发生反应 X(g)+aY(g)?2Z(g).各容器的反应温度、反应物起始量、反应过程中Z的浓度随时间变化分别以如图和下表来表示.下列说法不正确的是( )
向甲、乙、丙三个容积固定不变的密闭容器中充入一定量的X和Y,一定条件下发生反应 X(g)+aY(g)?2Z(g).各容器的反应温度、反应物起始量、反应过程中Z的浓度随时间变化分别以如图和下表来表示.下列说法不正确的是( ) | 容器 | 甲 | 乙 | 丙 | |
| 容积/L | 0.5 | 0.5 | 1.0 | |
| 温度/℃ | T1 | T2 | T2 | |
| 反应物起始量 | 1.0 mol X 0.5 mol Y | 1.0 mol X 0.5 mol Y | 4.0 mol X 2.0 mol Y |
| A. | 该反应温度升高,平衡常数减小 | |
| B. | 20 min内甲容器中反应的平均速率:v(X)=0.0375mol•(L•min)-1 | |
| C. | 10 min时,其他条件不变,向乙容器中再加入2 mol Z,平衡向逆反应方向移动 | |
| D. | 其他条件不变,若缩小乙的体积,Y的转化率增大 |
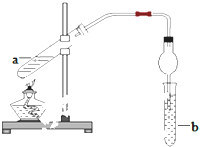 如图,在试管a中先加入2mL95%的乙醇,再加入3mL无水醋酸,边摇边缓缓加入2mL浓H2SO4,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入5mL饱和碳酸钠溶液.连接好装置.用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.
如图,在试管a中先加入2mL95%的乙醇,再加入3mL无水醋酸,边摇边缓缓加入2mL浓H2SO4,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入5mL饱和碳酸钠溶液.连接好装置.用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验. CH3COOC2H5+H2O.
CH3COOC2H5+H2O.