10.下列说法不正确的是( )
| A. | 由于Ksp(ZnS)>Ksp(CuS),所以ZnS沉淀在一定条件下可转化为CuS沉淀 | |
| B. | Ksp只与难溶电解质的性质和温度有关 | |
| C. | 其他条件不变,离子浓度改变时,Ksp不变 | |
| D. | 两种难溶电解质,Ksp小的,溶解度一定小 |
9.(1)实验室要使AlCl3溶液中的Al3-全部沉淀出来,最适宜用方法是(用离子方程式表示)Al3++3NH3•H2O═Al(OH)3↓+3NH4+;
(2)现有如下两个反应:
A:2NaOH+H2SO4=Na2SO4+2H2O B:CH4+2O2=CO2+2H2O
根据反应的本质,两个反应都为放热反应(填“放热”或“吸热”);
(3)下列各项分别与哪个影响化学反应速率因素的关系最为密切?
①夏天的食品易变霉,在冬天不易发生该现象:温度;
②双氧水中加入MnO2放出气泡更快:催化剂;
③同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气体有快有慢:反应物本身性质;
④黄铁矿煅烧时要粉碎成细小的矿粒:固体表面积;
(4)已知Na2S2O3+H2SO4=Na2SO4+S↓+SO2+H2O,甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响,设计如下实验(所取溶液体积均为10mL)
其他条件不变时:探究浓度对化学反应速率的影响,应选择①②和③④(填试验编号),探究温度对化学反应速率的影响,应选择①④(填试验编号);
(5)某元素的同位素R形成的最高价氧化物的化学式是RO2,其气态氢化合物中含氢25%,且已知R原子核内的质子数等于中子数.则:R的质数量为12,质子数为6.
(2)现有如下两个反应:
A:2NaOH+H2SO4=Na2SO4+2H2O B:CH4+2O2=CO2+2H2O
根据反应的本质,两个反应都为放热反应(填“放热”或“吸热”);
(3)下列各项分别与哪个影响化学反应速率因素的关系最为密切?
①夏天的食品易变霉,在冬天不易发生该现象:温度;
②双氧水中加入MnO2放出气泡更快:催化剂;
③同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气体有快有慢:反应物本身性质;
④黄铁矿煅烧时要粉碎成细小的矿粒:固体表面积;
(4)已知Na2S2O3+H2SO4=Na2SO4+S↓+SO2+H2O,甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响,设计如下实验(所取溶液体积均为10mL)
| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol•L-1 | c(H2SO4)/mol•L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.1 | 0.2 |
| ③ | 50 | 0.2 | 0.1 |
| ④ | 50 | 0.1 | 0.1 |
(5)某元素的同位素R形成的最高价氧化物的化学式是RO2,其气态氢化合物中含氢25%,且已知R原子核内的质子数等于中子数.则:R的质数量为12,质子数为6.
7.阿伏加德罗常数约为6.02×1023 mol-1,下列叙述正确的是( )
| A. | 2.24 L CO2中含有的原子数为0.3×6.02×1023 | |
| B. | 0.1 mol F- 中含有的电子数等于0.9×6.02×1023 | |
| C. | 5.6 g铁粉与硝酸反应失去的电子数一定为0.3×6.02×1023 | |
| D. | 电解饱和食盐水若产生2 g氢气,则转移的电子数目为2×6.02×1023 |
6.已知四种主族元素的离子aWm+、bXn+、cYm-、dZn-具有相同的电子层结构,下列说法正确的是( )
| A. | 若m>n,金属性W>X | |
| B. | 若m>n,气态氢化物的稳定性HmY>HnZ | |
| C. | 若m<n,氧化性Xn+>Wm+ | |
| D. | 若m<n,原子序数a>b>c>d |
5.已知aA+、bB2+、cC-、dD2-四种离子均具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是( )
| A. | 原子半径:A>B>C>D | B. | 原子序数:b>a>c>d | ||
| C. | 离子半径:D>C>B>A | D. | a+1=d-2 |
4.只用胶头滴管和试管,不能区别的溶液是( )
| A. | CaCl2和Na2CO3 | B. | 稀盐酸和Na[Al(OH)4] | C. | 稀盐酸和Na2CO3 | D. | NaOH和AlCl3 |
3.下列说法不正确的是( )
①质子数相同的粒子一定属于同种元素
②同位素的物理性质有较大差别而化学性质几乎相同
③元素种类由质子数决定,核素种类由质子数和中子数共同决定,元素主要化学性质 由最外层电子数决定
④电子数相同的粒子不一定是同一种元素
⑤每种元素都有两种或两种以上的核素.
①质子数相同的粒子一定属于同种元素
②同位素的物理性质有较大差别而化学性质几乎相同
③元素种类由质子数决定,核素种类由质子数和中子数共同决定,元素主要化学性质 由最外层电子数决定
④电子数相同的粒子不一定是同一种元素
⑤每种元素都有两种或两种以上的核素.
| A. | ①②④ | B. | ③④⑤ | C. | ②③⑤ | D. | ①⑤ |
2.有机物X的蒸气相对氢气的密度为51,X中氧元素的质量分数为31.7%,则能在碱性溶液中发生反应的X的同分异构体有(不考虑立体异构)( )
| A. | 4种 | B. | 9种 | C. | 13种 | D. | 15种 |
1.某元素R原子的质量数为127,已知R的离子中含有72个中子,54个电子,该原子最高价某化合物的化学式正确的是( )
0 154871 154879 154885 154889 154895 154897 154901 154907 154909 154915 154921 154925 154927 154931 154937 154939 154945 154949 154951 154955 154957 154961 154963 154965 154966 154967 154969 154970 154971 154973 154975 154979 154981 154985 154987 154991 154997 154999 155005 155009 155011 155015 155021 155027 155029 155035 155039 155041 155047 155051 155057 155065 203614
| A. | ROH | B. | R2O7 | C. | HRO3 | D. | NaR |
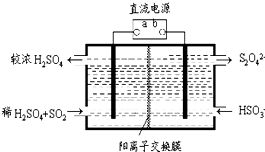 氮和硫的氧化物有多种,其中SO2和NOx都是大气污染物,对它们的研究有助于空气的净化.
氮和硫的氧化物有多种,其中SO2和NOx都是大气污染物,对它们的研究有助于空气的净化.