12.一定量的稀硫酸与足量的铝粉反应时,为了减缓反应速率,且不影响生成氢气的总量,应向稀硫酸中加入适量的( )
| A. | NaOH(固体) | B. | CH3COOH | C. | NaCl(固体) | D. | CH3COONa(固体) |
9.下列反应中不可能设计成原电池的是( )
| A. | NaOH+HCl═NaCl+H2O | B. | 2Fe3++Fe═3Fe2+ | ||
| C. | Zn+2HCl═ZnCl2+H2↑ | D. | 4Al+3O2+6H2O═4Al(OH)3↓ |
8.A、B、C、D、E、F、G为由七种短周期元素构成的粒子,它们都 有10个电子,其结构特点如下表:
其中,B的离子半径大于E的离子半径;D是由极性键构成的4原子分子;C常用作F的检验(加热).请填写下列空白:
(1)F粒子的电子式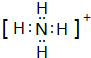 .
.
(2)比较BC和EC2的碱性强弱BC>EC2(填<、>、=).
(3)F与C加热时反应的离子方程式NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
| 粒子代号 | A | B | C | D | E | F | G |
| 原子核数 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
| 电荷数 | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
(1)F粒子的电子式
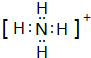 .
.(2)比较BC和EC2的碱性强弱BC>EC2(填<、>、=).
(3)F与C加热时反应的离子方程式NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
7.下表是元素周期表的一部分,请回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为 .
.
(2)表中能形成两性氢氧化物的元素在周期表中的位置是第三周期第ⅢA族,写出该元素的最高价氧化物对应的水化物与⑨最高价氧化物的水化物反应的化学方程式KOH+Al(OH)3═KAlO2+2H2O.
(3)用电子式表示④元素与⑦元素形成化合物的过程 .
.
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是HClO4(填酸的化学式).
(5)④⑤两元素相比较,金属性较强的是镁(填名称),可以验证该结论的实验是bc.(填编号)
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将形状、大小相同的这两种元素的单质分别和同浓度的盐酸反应
(c)将形状、大小相同两种元素的单质分别和热水作用,并滴入酚酞
(d)比较这两种元素的气态氢化物的稳定性
(6)⑥和⑦阴离子还原性较强的是(填微粒符号):S2-用一个置换反应证实这一结论(写化学方程式)Cl2+Na2S═2NaCl+S↓
(7)③⑦⑩三种元素的气态氢化物沸点由高到低的顺序为HF>HBr>HCl(写化学式),氢化物酸性由弱到强的顺序为HF<HCl<HBr(写化学式)
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .
.(2)表中能形成两性氢氧化物的元素在周期表中的位置是第三周期第ⅢA族,写出该元素的最高价氧化物对应的水化物与⑨最高价氧化物的水化物反应的化学方程式KOH+Al(OH)3═KAlO2+2H2O.
(3)用电子式表示④元素与⑦元素形成化合物的过程
 .
.(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是HClO4(填酸的化学式).
(5)④⑤两元素相比较,金属性较强的是镁(填名称),可以验证该结论的实验是bc.(填编号)
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将形状、大小相同的这两种元素的单质分别和同浓度的盐酸反应
(c)将形状、大小相同两种元素的单质分别和热水作用,并滴入酚酞
(d)比较这两种元素的气态氢化物的稳定性
(6)⑥和⑦阴离子还原性较强的是(填微粒符号):S2-用一个置换反应证实这一结论(写化学方程式)Cl2+Na2S═2NaCl+S↓
(7)③⑦⑩三种元素的气态氢化物沸点由高到低的顺序为HF>HBr>HCl(写化学式),氢化物酸性由弱到强的顺序为HF<HCl<HBr(写化学式)
6.微量元素硒(Se)对人体有保健作用,已知硒为第四周期第ⅥA族元素,根据它在周期表中的位置推测,下列对硒元素性质的描述不正确的是( )
| A. | 硒化氢不稳定 | |
| B. | 酸性强弱顺序:HClO4>H3AsO4>H2SeO4 | |
| C. | 硒与铁反应可生成FeSe | |
| D. | 最高氧化物的化学式是SeO3 |
5.有某温度下KCl饱和溶液m1g,溶质质量分数为ω1%.对其蒸发结晶或降温结晶,若析出KCl的质量、所得母液质量及溶质质量分数用m g、m2g和ω2%表示,分析正确的是( )
| A. | 原条件下KCl的溶解度小于ω1g | B. | m1?ω1%-m=m2?ω2% | ||
| C. | ω1一定大于ω2 | D. | m1-m2≤m |
4.氢核磁共振谱是根据不同化学环境的氢原子在谱中给出的信号不同来确定有机物分子中氢原子种类的.下列有机物分子中,在氢核磁共振谱中只给出一种信号的是( )
| A. | 丙烷 | B. | 新戊烷 | C. | 正丁烷 | D. | 异丁烷 |
3.对有关NaClO和NaCl混合溶液的叙述正确的是( )
0 154842 154850 154856 154860 154866 154868 154872 154878 154880 154886 154892 154896 154898 154902 154908 154910 154916 154920 154922 154926 154928 154932 154934 154936 154937 154938 154940 154941 154942 154944 154946 154950 154952 154956 154958 154962 154968 154970 154976 154980 154982 154986 154992 154998 155000 155006 155010 155012 155018 155022 155028 155036 203614
| A. | 该溶液中,H+、NH4+、SO42-、Br-可以大量共存 | |
| B. | 该溶液中,K+、OH-、S2-、NO3-能大量共存 | |
| C. | 向该溶液中滴入少量FeSO4溶液,离子方程式为:2Fe2++ClO-+2H+→Cl-+2Fe3++H2O | |
| D. | 向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023个 |
 原子序数小于36的X、Y、Z、W四种元素,其中X是宇宙中最丰富的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.
原子序数小于36的X、Y、Z、W四种元素,其中X是宇宙中最丰富的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29. (1)电子表所用的某种钮扣电池的电极材料为Zn和Ag2O,电解质溶液为KOH,其电极反应式分别为Zn+2OH--2e-=ZnO+H2O Ag2O+H2O+2e-=2Ag+2OH-
(1)电子表所用的某种钮扣电池的电极材料为Zn和Ag2O,电解质溶液为KOH,其电极反应式分别为Zn+2OH--2e-=ZnO+H2O Ag2O+H2O+2e-=2Ag+2OH-