12.几种短周期元素的原子半径及某些化合价见表
分析判断下列说法正确的是( )
| 元素代号 | A | B | D | E | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | -1 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.143 | 0.160 | 0.186 |
| A. | A的单质能将E从HE的溶液中置换出来 | |
| B. | 气态氢化物的稳定性:D>A>B | |
| C. | 离子半径由大到小的顺序是A>J>H | |
| D. | 最高价氧化物的水化物的碱性:H>I>J |
11.下列结论正确的是( )
| A. | 微粒半径:K+>Al3+>S2->Cl- | B. | 离子的还原性:S2->Cl->Br->I- | ||
| C. | 酸性:HClO>H2SO4>H3PO4>H2CO3 | D. | 金属性:K>Ca>Mg>Be |
10.应用元素周期表和元素周期律的有关知识,可以预测我们不知道的一些元素及其化合物的性质.下列说法中正确的是( )
| A. | 第六周期第ⅢA族的元素Tl,其氢氧化物的碱性比Al(OH)3弱 | |
| B. | 卤族元素At的单质为有色固体,AgAt可能不溶于水也不溶于稀硝酸 | |
| C. | Li与水反应比钠与水反应剧烈 | |
| D. | H2Se是无色,有毒,比H2S稳定的气体 |
9.下列说法正确的是( )
| A. | 有的共价化合物在液态时也能导电 | |
| B. | 含有离子键的化合物中,也可能还含有共价键 | |
| C. | 形成离子键的微粒必须是金属阳离子与阴离子 | |
| D. | 非金属元素形成的化合物一定不存在离子键 |
6.下列各组离子在指定的溶液中能大量共存的是( )
| A. | 酸性溶液中:K+、MnO4+、SO42-Cl- | |
| B. | 能使甲基橙显红色的溶液:Fe2+,NO3-,Na+,SO42- | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=l0-12的水溶液中:NH4+、Al3+、NO3-、Cl- | |
| D. | 酸性透明溶液中:Cu2+、Al3+、SO42-、NO3- |
4.查阅资料:无水醋酸钠是无色无味的结晶体,在空气中可被风化,可燃.用无水醋酸钠与碱石灰加热可以制得X气体.并作相应的实验:
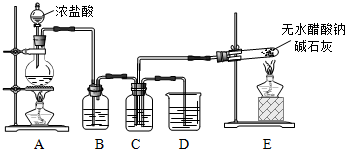
(1)装置E中反应方程式是CH3COONa+NaOH$→_{△}^{CaO}$Na2CO3+X↑,X的化学式是CH4.
(2)在C中收集气体X和Cl2为1:1体积混合,然后在光照下反应:
①B装置的作用是除去Cl2中含有的HCl;
②C装置所盛放试剂是饱和食盐水;光照后所得产物有CH3Cl、CH2Cl2、CHCl3、CCl4、HCl;
(3)设计一个实验方案,验证产物中生成了一种无机物:光照后,取C和D中液体各少许,分别加入两支试管中,再分别滴加2滴石蕊溶液,C中溶液红色更深;或用pH试纸测定C和D中溶液的pH等
(4)某学生为了测定X的组成进行实验探究,选用了下列仪器:
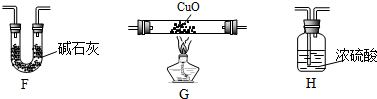
①该同学依次连接的合理顺序是E、G、H、F;
②该同学测定的相关数据是:
数据是否完全,说明原因数据是不完全,因为只能确定有机物中的碳氢元素含量,不能确定是否含有氧元素,应称取C装置实验前后的质量;
该测定含氢量是否有偏差?若有偏差,请说明原因F中吸收的是CO2,CO2质量33.6g-22.5g=11.1g,n(C)=$\frac{11.1g}{44g/mol}$=0.252mol;H中吸收的是水蒸气,H2O质量51.4g-42.4g=9.0g,n(H)=$\frac{9.0g}{18g/mol}$×2=1.0mol;
故n(C):n(H)>1:4.原因是F装置后面与空气接触,空气中的水蒸气和CO2进入了B装置,造成含碳量偏大.

(1)装置E中反应方程式是CH3COONa+NaOH$→_{△}^{CaO}$Na2CO3+X↑,X的化学式是CH4.
(2)在C中收集气体X和Cl2为1:1体积混合,然后在光照下反应:
①B装置的作用是除去Cl2中含有的HCl;
②C装置所盛放试剂是饱和食盐水;光照后所得产物有CH3Cl、CH2Cl2、CHCl3、CCl4、HCl;
(3)设计一个实验方案,验证产物中生成了一种无机物:光照后,取C和D中液体各少许,分别加入两支试管中,再分别滴加2滴石蕊溶液,C中溶液红色更深;或用pH试纸测定C和D中溶液的pH等
(4)某学生为了测定X的组成进行实验探究,选用了下列仪器:

①该同学依次连接的合理顺序是E、G、H、F;
②该同学测定的相关数据是:
| 装置 | 实验前的质量/g | 实验后的质量/g |
| F | 22.5 | 33.6 |
| H | 42.4 | 51.4 |
该测定含氢量是否有偏差?若有偏差,请说明原因F中吸收的是CO2,CO2质量33.6g-22.5g=11.1g,n(C)=$\frac{11.1g}{44g/mol}$=0.252mol;H中吸收的是水蒸气,H2O质量51.4g-42.4g=9.0g,n(H)=$\frac{9.0g}{18g/mol}$×2=1.0mol;
故n(C):n(H)>1:4.原因是F装置后面与空气接触,空气中的水蒸气和CO2进入了B装置,造成含碳量偏大.
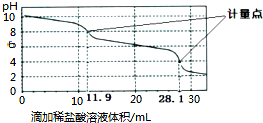
3.实验室使用pH传感器来测定Na2CO3和NaHCO3混合物中NaHCO3的含量.称取1.59g样品,溶于水配成250.00mL溶液,取出该溶液25.00mL用0.1mol•L-1盐酸进行滴定,得到如下曲线.以下说法正确的是( )
0 154814 154822 154828 154832 154838 154840 154844 154850 154852 154858 154864 154868 154870 154874 154880 154882 154888 154892 154894 154898 154900 154904 154906 154908 154909 154910 154912 154913 154914 154916 154918 154922 154924 154928 154930 154934 154940 154942 154948 154952 154954 154958 154964 154970 154972 154978 154982 154984 154990 154994 155000 155008 203614

| A. | 上一计量点前发生反应的离子方程式为HCO3-+H+═H2O+CO2↑ | |
| B. | 下一个计量点溶液中存在大量的阴离子是Cl-、HCO3- | |
| C. | 此样品n(NaHCO3)=(28.1-2×11.9)×10-3mol | |
| D. | 使用该方法测定Na2CO3和NaOH混合物中氢氧化钠含量,将会得到1个计量点 |
 某课外小组分别用如图所示装置对电解原理进行实验探究.
某课外小组分别用如图所示装置对电解原理进行实验探究.