19.关于碱金属元素的下列叙述中,错误的是( )
| A. | 碱金属元素原子最外层都只有1个电子 | |
| B. | 依Li、Na、K、Rb、Cs,单质熔沸点升高,密度增大 | |
| C. | 随核电荷数递增,氢氧化物碱性增强 | |
| D. | 随电子层数增加,原子半径增大,金属还原性和金属性增强 |
17.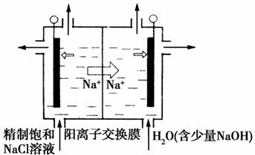 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺.
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺.
(1)①如图装置用石墨作电极,在一定条件下电解饱和食盐水制取ClO2.写出阳极产生ClO2的电极反应式:Cl--5e-+2H2O=ClO2↑+4H+.
②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解.通过阳离子交换膜的阳离子的物质的量为0.01mol.
(2)为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了Y2O3的ZrO2晶体,在高温下它能传导O2-离子.电池工作时正极反应为O2+4e-=2O2-.
(3)若以该电池为电源,用石墨做电极电解100mL含有如下离子的溶液.
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的物质的量为0.1mol.
 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺.
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺.(1)①如图装置用石墨作电极,在一定条件下电解饱和食盐水制取ClO2.写出阳极产生ClO2的电极反应式:Cl--5e-+2H2O=ClO2↑+4H+.
②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解.通过阳离子交换膜的阳离子的物质的量为0.01mol.
(2)为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了Y2O3的ZrO2晶体,在高温下它能传导O2-离子.电池工作时正极反应为O2+4e-=2O2-.
(3)若以该电池为电源,用石墨做电极电解100mL含有如下离子的溶液.
| 离子 | Cu2+ | H+ | Cl- | SO42- |
| c/mol•L-1 | 1 | 4 | 4 | 1 |
15.锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子通过,下列有关叙述正确的是( )
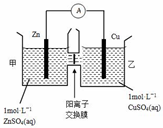

| A. | 电池工作一段时间后,乙池溶液的总质量增加 | |
| B. | 电池工作一段时间后,甲池的c(SO42-)减小 | |
| C. | 铜电极上发生氧化反应 | |
| D. | 阴阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡 |
14.把0.05molNaOH固体分别加入到100mL下列液体中,溶液的导电能力变化最小的是( )
| A. | 0.5mol/L KCl溶液 | B. | 自来水 | ||
| C. | 0.5mol/L盐酸 | D. | 0.5mol/L醋酸溶液 |
10.盐酸或硫酸和氢氧化钠溶液的中和反应没有明显的现象.某学习兴趣小组的同学为了证明氢氧化钠溶液与盐酸或硫酸发生了反应,从中和反应的热效应出发,设计了下面几种实验方案.请回答有关问题.
(1)方案一:如图1装好实验装置,图中小试管用细线吊着,细线的上端拴在细铁丝上.开始时使右端U形管两端红墨水相平.实验开始,向下插细铁丝,使小试管内盐酸和广口瓶内氢氧化钠溶液混合,此时观察到的现象是U形管内液面左边下降、右边升高,原因是盐酸和氢氧化钠发生中和反应放出热量,使瓶内气体温度升高,压强增大.

(2)方案二:该小组借助反应溶液温度的变化来判断反应的发生.如果氢氧化钠溶液与盐酸混合前后有温度的变化,则证明发生了化学反应.该小组同学将不同浓度的氢氧化钠溶液和盐酸各10mL混合,用温度计测量反应前后温度的变化,测得的部分数据如下表:
则x=7.
(3)方案三:该小组还设计了如图2示装置来证明氢氧化钠溶液确实与稀硫酸发生了反应.他们认为若洗气瓶中导管口有气泡冒出,则说明该反应放出热量,从而证明发生了反应.
①实验时,打开分液漏斗活塞,发现导管流出液体不畅,原因可能是没打开分液漏斗上部塞子
②从原理上讲,该实验设计的不合理之处为稀硫酸具有一定的体积,冒出气泡的原因可能是加入稀硫酸的体积引起的.
请你在此实验装置的基础上提出修改方案分液漏斗上口和锥形瓶之间连接一导管.
0 154777 154785 154791 154795 154801 154803 154807 154813 154815 154821 154827 154831 154833 154837 154843 154845 154851 154855 154857 154861 154863 154867 154869 154871 154872 154873 154875 154876 154877 154879 154881 154885 154887 154891 154893 154897 154903 154905 154911 154915 154917 154921 154927 154933 154935 154941 154945 154947 154953 154957 154963 154971 203614
(1)方案一:如图1装好实验装置,图中小试管用细线吊着,细线的上端拴在细铁丝上.开始时使右端U形管两端红墨水相平.实验开始,向下插细铁丝,使小试管内盐酸和广口瓶内氢氧化钠溶液混合,此时观察到的现象是U形管内液面左边下降、右边升高,原因是盐酸和氢氧化钠发生中和反应放出热量,使瓶内气体温度升高,压强增大.

(2)方案二:该小组借助反应溶液温度的变化来判断反应的发生.如果氢氧化钠溶液与盐酸混合前后有温度的变化,则证明发生了化学反应.该小组同学将不同浓度的氢氧化钠溶液和盐酸各10mL混合,用温度计测量反应前后温度的变化,测得的部分数据如下表:
| 编号 | 盐酸 | 氢氧化钠 | △t/℃ |
| 1 | 0.1mol•L-1 | 0.05mol•L-1 | 3.5 |
| 2 | 0.1mol•L-1 | 0.1mol•L-1 | x |
| 3 | 0.2mol•L-1 | 0.2mol•L-1 | 14 |
(3)方案三:该小组还设计了如图2示装置来证明氢氧化钠溶液确实与稀硫酸发生了反应.他们认为若洗气瓶中导管口有气泡冒出,则说明该反应放出热量,从而证明发生了反应.
①实验时,打开分液漏斗活塞,发现导管流出液体不畅,原因可能是没打开分液漏斗上部塞子
②从原理上讲,该实验设计的不合理之处为稀硫酸具有一定的体积,冒出气泡的原因可能是加入稀硫酸的体积引起的.
请你在此实验装置的基础上提出修改方案分液漏斗上口和锥形瓶之间连接一导管.

 氮是地球上含量丰富的元素,氮及其化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的元素,氮及其化合物在工农业生产、生活中有着重要作用. .
.
 某校开展课外研究性学习:从废旧干电池中回收碳棒、MnO2、NH4Cl、ZnCl2等物质,整个过程如下,回答有关问题:
某校开展课外研究性学习:从废旧干电池中回收碳棒、MnO2、NH4Cl、ZnCl2等物质,整个过程如下,回答有关问题: