9.短周期元素a、b、c、d的原子序数依次增大.c、a、b最外层电子数为等差数列.公差为2.a、c的价电子数之和为6.d的核外电子数等于b的核外电子数加8.下列叙述错误的是( )
| A. | a和b可形成气态化合物 | |
| B. | c的原子半径小于d的原子半径 | |
| C. | b和c形成的化合物为离子化合物 | |
| D. | a和d最高价氧化物的水化物均呈酸性 |
8.下列化学式能代表一种纯净物的是( )
| A. | C3H8 | B. | C4H10 | C. | C5H12 | D. | C2H4Br2 |
7.下列关于极性键的叙述不正确的是( )
| A. | 由不同种元素原子形成的共价键 | |
| B. | 由同种元素的两个原子形成的共价键 | |
| C. | 分子中必定含有极性键 | |
| D. | 共同电子对必然偏向吸引电子能力强的原子一方 |
6.下列各分子中所有原子都满足最外层为8电子稳定结构的是( )
| A. | BeCl2 | B. | CO2 | C. | HCl | D. | N2 |
5.使1mol某烷烃完全燃烧需要消耗氧气5mol,该烷烃的化学式是( )
| A. | C2H6 | B. | C3H8 | C. | C4H10 | D. | C5H12 |
4. A到F是原子序数依次增大的前四周期元素:
A到F是原子序数依次增大的前四周期元素:
回答下列问题:
(1)写出E、F的元素符号Mg、Cr,B、C、D元素的第一电离能由大到小的顺序为N>O>C(用元素符号表示),A元素分别与B、D元素形成的两种微粒都具有与NH3相似的结构,属于等电子体,它们的化学式依次是CH3-、H3O+.
(2)在CH3Cl、C6H6、HCHO、CH3OH、CH≡CH中,碳原子采取sp2杂化的有C6H6、HCHO;应用价层电子对互斥理论,预测COCl2的空间构型为平面三角形.
(3)F元素的原子基态价层电子排布图是 .
.
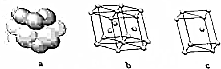
(4)E单质晶体中原子的堆积模型如图,晶胞是图中的c(填“a”、“b”或“c”);配位数是12‘若紧邻的四个E原子的中心连线构成的几何体的体积是Vcm3,E单质的密度为ρg•cm-3,则E的相对原子质量是计算式是6NA•V•ρ.
 A到F是原子序数依次增大的前四周期元素:
A到F是原子序数依次增大的前四周期元素:| A | A是原子半径最小的元素 |
| B | B基态原子的价层电子排布式为nsnnpn |
| D | D原子最外层电子数是次外层电子数的三倍 |
| E | C的三价阴离子和E的二价阳离子具有相同的电子层结构 |
| F | F元素的基态原子有六个成单电子 |
(1)写出E、F的元素符号Mg、Cr,B、C、D元素的第一电离能由大到小的顺序为N>O>C(用元素符号表示),A元素分别与B、D元素形成的两种微粒都具有与NH3相似的结构,属于等电子体,它们的化学式依次是CH3-、H3O+.
(2)在CH3Cl、C6H6、HCHO、CH3OH、CH≡CH中,碳原子采取sp2杂化的有C6H6、HCHO;应用价层电子对互斥理论,预测COCl2的空间构型为平面三角形.
(3)F元素的原子基态价层电子排布图是
 .
.(4)E单质晶体中原子的堆积模型如图,晶胞是图中的c(填“a”、“b”或“c”);配位数是12‘若紧邻的四个E原子的中心连线构成的几何体的体积是Vcm3,E单质的密度为ρg•cm-3,则E的相对原子质量是计算式是6NA•V•ρ.
3.常温下将0.1mol的Cl2通入0.5L的水中(不计溶液体积变化),制得氯水,关于这份氯水下列说法正确的是( )
0 154770 154778 154784 154788 154794 154796 154800 154806 154808 154814 154820 154824 154826 154830 154836 154838 154844 154848 154850 154854 154856 154860 154862 154864 154865 154866 154868 154869 154870 154872 154874 154878 154880 154884 154886 154890 154896 154898 154904 154908 154910 154914 154920 154926 154928 154934 154938 154940 154946 154950 154956 154964 203614
| A. | 若不考虑HClO和H20的电离,该溶液中H+的浓度为0.1mol/L | |
| B. | 若在该溶液中加入足量Na0H,则可得到0.1mol的NaClO | |
| C. | 若将此溶液在强光下光照,产生气泡,则气泡主要成分是O2 | |
| D. | 此溶液久置后,由于HClO的大量分解,会导致其pH值升高 |
 根据氧化还原反应Zn+2H+═Zn2++H2↑设计的原电池如图所示:
根据氧化还原反应Zn+2H+═Zn2++H2↑设计的原电池如图所示: