19.在0.1mol•L-1NH3•H2O溶液中存在如下电离平衡:NH3•H2O?NH4++OH-.对于该平衡,下列叙述中正确的是( )
| A. | 降低温度,溶液中c(NH4+)增大 | |
| B. | 加入水时,溶液中$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$ 增大 | |
| C. | 加入水时,溶液中c(H+)减小 | |
| D. | 加入少量NaOH固体,平衡向逆反应方向移动,溶液中c(OH-)减小 |
18.在25°C时,在水中通入氯化氢气体,当溶液的PH=3时,此时由水电离出的c(H+)是( )
| A. | 10-3mol/L | B. | 10-7 mol/L | C. | 10-11 mol/L | D. | 10-14mol/L |
17.某温度下在容积不变的密闭容器中发生如下反应:2SO2+O2?2SO3(g),若开始时只充入2molSO3(g),达到平衡时,混合气体的压强比起始时增大了20%;若开始时只充入了2mol SO2和1molO2的混合气体,达到平衡时SO2的转化率为( )
| A. | 20% | B. | 40% | C. | 60% | D. | 80% |
16.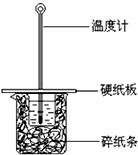 某同学按照课本实验要求,用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH 溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.下列说法,不正确的是( )
某同学按照课本实验要求,用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH 溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.下列说法,不正确的是( )
 某同学按照课本实验要求,用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH 溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.下列说法,不正确的是( )
某同学按照课本实验要求,用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH 溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.下列说法,不正确的是( )| A. | 采用0.55mol/L的NaOH溶液是保证盐酸完全被中和 | |
| B. | 图中实验装置缺少环形玻璃搅拌棒 | |
| C. | 烧杯间填满碎纸条的作用是保温隔热,防止热量损失 | |
| D. | 若烧杯上不盖硬纸板,测得的△H将偏小 |
15.在固定容积的容器中盛有1molPCl5,200℃时发生如下反应:PCl5(g)?PCl3+Cl2(g)达到平衡时,PCl5体积分数为M%.若恒温下向容器中再通入1molPCl5,再次达平衡时,PCl5所占体积分数为N%,则M和N的关系是( )
| A. | M>N | B. | M<N | C. | M=N | D. | 无法判断 |
14.常温下,1mol化学键分解成气态原子所需要的能量用E表示.结合表中信息判断下列说法不正确的是( )
| 共价键 | H-H | F-F | H-F | H-Cl | H-I |
| E(kJ•mol-1 ) | 436 | 157 | 568 | 432 | 298 |
| A. | 432 kJ•mol -1>E(H-Br)>298 kJ•mol -1 | |
| B. | 表中最稳定的共价键是H-F键 | |
| C. | H 2 (g)→2H (g)△H=+436 kJ•mol -1 | |
| D. | H 2 (g)+F 2 (g)=2HF(g)△H=-25 kJ•mol -1 |
13.下列电离方程式正确的是( )
| A. | NH3•H2O═NH4++OH- | B. | H2S?S2-+2H+ | ||
| C. | CaCO3?Ca2++CO32- | D. | CH3COONH4═CH3COO-+NH4+ |
12.在甲酸的下列性质中,可以证明它是弱电解质的是( )
| A. | 1mol/L的甲酸溶液中c(H+)约为0.01mol/L | |
| B. | 甲酸与水以任意比例互溶 | |
| C. | 10mL 1mol/L的甲酸溶液恰好与10mL 1mol/L的NaOH溶液完全反应 | |
| D. | 在相同温度下,物质的量浓度相同的甲酸导电性比硫酸弱 |
11.下列说法正确的是( )
0 154765 154773 154779 154783 154789 154791 154795 154801 154803 154809 154815 154819 154821 154825 154831 154833 154839 154843 154845 154849 154851 154855 154857 154859 154860 154861 154863 154864 154865 154867 154869 154873 154875 154879 154881 154885 154891 154893 154899 154903 154905 154909 154915 154921 154923 154929 154933 154935 154941 154945 154951 154959 203614
| A. | 吸热反应一定是非自发的化学反应,放热反应不需要加热就能发生反应 | |
| B. | 其它条件不变时,增大压强可以增大活化分子百分数,使化学反应速率加快 | |
| C. | 温度、压强一定时,熵增加的反应都能自发进行 | |
| D. | 应用盖斯定律,可计算某些难以直接测量的反应焓变 |