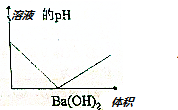
5.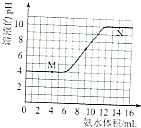 常温下,用一定浓度的氨水滴定一定体积未知浓度的土壤浸出溶液,溶液的pH变化与滴入氨水体积的关系如图所示,下列有关说法不正确的是( )
常温下,用一定浓度的氨水滴定一定体积未知浓度的土壤浸出溶液,溶液的pH变化与滴入氨水体积的关系如图所示,下列有关说法不正确的是( )
 常温下,用一定浓度的氨水滴定一定体积未知浓度的土壤浸出溶液,溶液的pH变化与滴入氨水体积的关系如图所示,下列有关说法不正确的是( )
常温下,用一定浓度的氨水滴定一定体积未知浓度的土壤浸出溶液,溶液的pH变化与滴入氨水体积的关系如图所示,下列有关说法不正确的是( )| A. | 该土壤是酸性土壤 | |
| B. | 当溶液中c(H+)=c(OH-)时,消耗氨水的体积为9mL | |
| C. | M、N点由水电离出的氢离子浓度一定相等 | |
| D. | 将20mL此氨水与10mL同浓度的盐酸混合,充分反应后存在:C(NH4+)>c(Cl-)>c(NH3•H2O)>c(OH-)>c(H+) |
4. 常温下,取浓度均为0.01mol•L-1的HA溶液和MOH溶液各20mL,分别用0.01mol•L-1NaOH溶液、0.01mol•L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )
常温下,取浓度均为0.01mol•L-1的HA溶液和MOH溶液各20mL,分别用0.01mol•L-1NaOH溶液、0.01mol•L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )
 常温下,取浓度均为0.01mol•L-1的HA溶液和MOH溶液各20mL,分别用0.01mol•L-1NaOH溶液、0.01mol•L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )
常温下,取浓度均为0.01mol•L-1的HA溶液和MOH溶液各20mL,分别用0.01mol•L-1NaOH溶液、0.01mol•L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )| A. | HA和MOH均为弱电解质 | |
| B. | 曲线a中,滴加溶液到20mL时,c(Cl-)=c(M+)=c(OH-)=c(H+) | |
| C. | 曲线b中,滴加溶液到20mL时,c(Na+)>c(A-)>c(OH-)>c(H+) | |
| D. | 曲线b中,滴加溶液到10mL时,c(A-)+c(OH-)=c(H+)+c(HA) |
2.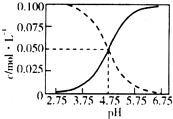 25℃时,c(CH3COOH)+c(CH3COO-)=0.1mol•L-1的醋酸、醋酸钠混合溶液中,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列叙述正确的是( )
25℃时,c(CH3COOH)+c(CH3COO-)=0.1mol•L-1的醋酸、醋酸钠混合溶液中,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列叙述正确的是( )
 25℃时,c(CH3COOH)+c(CH3COO-)=0.1mol•L-1的醋酸、醋酸钠混合溶液中,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列叙述正确的是( )
25℃时,c(CH3COOH)+c(CH3COO-)=0.1mol•L-1的醋酸、醋酸钠混合溶液中,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列叙述正确的是( )| A. | 25℃时,CH3COOH的电离常数K的值5×10-2.75 | |
| B. | 随pH增大,$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$增大 | |
| C. | pH=4的溶液中,c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) | |
| D. | pH=5的溶液中,c(H+)+c(Na+)+c(CH3COOH)-c(OH-)=0.1 mol•L-1 |
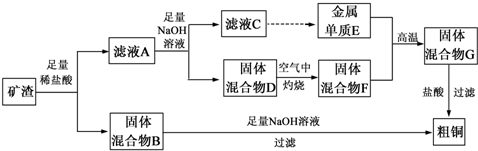
19.对下列流程有关判断正确的是( )
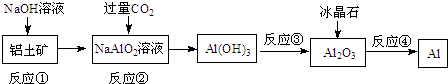

| A. | 流程中涉及的反应均为非氧化还原反应 | |
| B. | 反应②产生的阴离子主要为CO32- | |
| C. | 实验室中完成反应③应在蒸发皿中进行 | |
| D. | 反应①中发生的主要反应为:Al2O3+2OH-=2AlO2-+H2O |
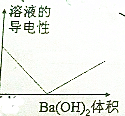
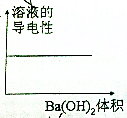
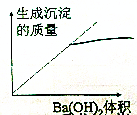
18.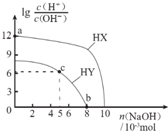 常温下,浓度均为0.1mol?L-1、体积均为100mL的两种一元酸HX、HY的溶液中,分别加入NaOH固体,lg$\frac{c({H}^{+})}{c(O{H}^{-})}$随加入NaOH的物质的量的变化如图所示.下列叙述正确的是( )
常温下,浓度均为0.1mol?L-1、体积均为100mL的两种一元酸HX、HY的溶液中,分别加入NaOH固体,lg$\frac{c({H}^{+})}{c(O{H}^{-})}$随加入NaOH的物质的量的变化如图所示.下列叙述正确的是( )
 常温下,浓度均为0.1mol?L-1、体积均为100mL的两种一元酸HX、HY的溶液中,分别加入NaOH固体,lg$\frac{c({H}^{+})}{c(O{H}^{-})}$随加入NaOH的物质的量的变化如图所示.下列叙述正确的是( )
常温下,浓度均为0.1mol?L-1、体积均为100mL的两种一元酸HX、HY的溶液中,分别加入NaOH固体,lg$\frac{c({H}^{+})}{c(O{H}^{-})}$随加入NaOH的物质的量的变化如图所示.下列叙述正确的是( )| A. | HX的酸性弱于HY | |
| B. | a点由水电离出的c(H+)=10-12 mol?L-1 | |
| C. | c点溶液中:c(Y-)>c(HY) | |
| D. | b点时酸碱恰好完全反应 |
16.氨水是实验室中的常用试剂.某课外活动小组欲通过实验测定NH3•H2O的电离常数.
【讨论】选用以下试剂和仪器:浓度大约为0.1mol/L的氨水、0.1000mol/L盐酸、甲基橙、蒸馏水、酸式滴定管、碱式滴定管、锥形瓶、胶头滴管、烧杯、pH计、铁架台
在组装仪器是发现缺少了一种仪器,缺少的仪器是滴定管夹.添加这种仪器后进行实验.
【实验过程】
【反思】:该小组在实验条件下测得氨水的电离常数K=1.60×10-5.查阅资料得知:25℃时氨水的电离常数K=1.75×10-5.检查滴定过程操作、计算均没有错误,该小组讨论后认为实验测得氨水的电离常数是准确的,但是应该补充一项实验内容,补充的实验内容是测定氨水的温度.
【拓展应用】25℃时,pH=5的氯化铵溶液中$\frac{c({H}^{+})×c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$=0.175.(写出推导过程并计算出结果)
0 154692 154700 154706 154710 154716 154718 154722 154728 154730 154736 154742 154746 154748 154752 154758 154760 154766 154770 154772 154776 154778 154782 154784 154786 154787 154788 154790 154791 154792 154794 154796 154800 154802 154806 154808 154812 154818 154820 154826 154830 154832 154836 154842 154848 154850 154856 154860 154862 154868 154872 154878 154886 203614
【讨论】选用以下试剂和仪器:浓度大约为0.1mol/L的氨水、0.1000mol/L盐酸、甲基橙、蒸馏水、酸式滴定管、碱式滴定管、锥形瓶、胶头滴管、烧杯、pH计、铁架台
在组装仪器是发现缺少了一种仪器,缺少的仪器是滴定管夹.添加这种仪器后进行实验.
【实验过程】
| 实验步骤 | 实验目的 |
| (滴定前的所有操作正确,已略去) 步骤1: ①用碱式滴定管量取20.00mL的氨水放入锥形瓶中,滴入2滴甲基橙. ②用酸式滴定管取0.1000mol/L盐酸滴定氨水. ③当锥形瓶中的溶液由黄色变成橙色时,停止滴定,纪录数据. ④重复滴定操作2~3次. | 测定氨水的准确浓度 |
| 步骤2:用pH计测定氨水的pH. | 测定氨水中c(OH-)浓度 |
| 步骤3:通过实验数据计算氨水的电离常数K | |
【拓展应用】25℃时,pH=5的氯化铵溶液中$\frac{c({H}^{+})×c(N{{H}_{4}}^{+})}{c(N{H}_{3}•{H}_{2}O)}$=0.175.(写出推导过程并计算出结果)
 实验室有化学纯的浓硫酸,其试剂瓶标签上的部分内容如图:
实验室有化学纯的浓硫酸,其试剂瓶标签上的部分内容如图: