1.SO2通入下列溶液中,溶液褪色或变浅,说明SO2具有漂白作用的组合是( )
①KMnO4(H+,aq) ②品红溶液③溴水④氯水⑤Fe3+(aq)
①KMnO4(H+,aq) ②品红溶液③溴水④氯水⑤Fe3+(aq)
| A. | ①③⑤ | B. | ①②③④ | C. | ①③④⑤ | D. | 只有② |
20.下列说法中正确的是( )
| A. | 电子云通常是用小黑点来表示电子的多少 | |
| B. | 能量高的电子在离核近的区域运动,能量低的电子在离核远的区域运动 | |
| C. | 处于最低能量的原子叫基态原子 | |
| D. | 电子仅在激发态跃迁到基态时才会产生原子光谱 |
19.NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 在标准状况下,22.4L乙醛完全燃烧后,生成CO2的分子数为2NA | |
| B. | 1L 0.1mol/L乙酸溶液中所含乙酸分子数为0.1NA | |
| C. | 常温常压下,14g乙烯、丙烯、丁烯的混合气体所含原子总数为3NA | |
| D. | 1mol甲基所含电子数为10NA |
18.下列氯元素含氧酸酸性最强的是( )
| A. | HClO | B. | HClO2 | C. | HClO3 | D. | HClO4 |
15.下列说法或表示方法中正确的是( )
| A. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 已知C(s)+$\frac{ax}{0.02}$O2(g)=CO(g)的反应热为110.5kJ/mol,说明碳的燃烧热为110.5kJ | |
| C. | 已知反应X+Y=M+N为放热反应,故不必加热就可发生 | |
| D. | 稀溶液中:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ•mol-1,若将含0.5 molH2SO4的浓溶液与含1 molNaOH的溶液混合,放出的热量大于57.3KJ |
14.下列反应无论怎样调整反应物的用量都只能生成一种物质的是( )
0 154659 154667 154673 154677 154683 154685 154689 154695 154697 154703 154709 154713 154715 154719 154725 154727 154733 154737 154739 154743 154745 154749 154751 154753 154754 154755 154757 154758 154759 154761 154763 154767 154769 154773 154775 154779 154785 154787 154793 154797 154799 154803 154809 154815 154817 154823 154827 154829 154835 154839 154845 154853 203614
| A. | 甲烷和氯气混合后光照发生反应 | B. | 乙炔和氯气的加成反应 | ||
| C. | 甲苯与等物质的量的Br2发生反应 | D. | 乙烯与水的加成反应 |



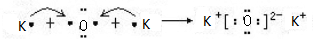

 .
.