5.将-CH3、-OH、-COOH、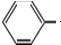 四种原子团两两结合,所得化合物水溶液呈酸性的共有( )
四种原子团两两结合,所得化合物水溶液呈酸性的共有( )
 四种原子团两两结合,所得化合物水溶液呈酸性的共有( )
四种原子团两两结合,所得化合物水溶液呈酸性的共有( )| A. | 3种 | B. | .4种 | C. | .5种 | D. | .6种 |
4. 电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用,其原理如图所示.下列说法正确的是( )
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用,其原理如图所示.下列说法正确的是( )
 电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用,其原理如图所示.下列说法正确的是( )
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用,其原理如图所示.下列说法正确的是( )| A. | 石墨电极上发生氧化反应 | |
| B. | 根据图示,物质A为CO2 | |
| C. | 甲烷燃料电池中CO32-向空气一极移动 | |
| D. | 为增强污水的导电能力,可向污水中加入适量乙醇 |
3.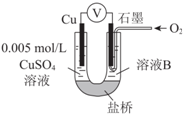 某小组同学利用原电池装置探究物质的性质.
某小组同学利用原电池装置探究物质的性质.
资料显示:原电池装置中,负极反应物的还原性越强,或正极反应物的氧化性越强,原电池的电压越大.
(1)同学们利用下表中装置进行实验并记录.
①同学们认为实验Ⅰ中铁主要发生了析氢腐蚀,其正极反应式是2H++2e-=H2↑.
②针对实验Ⅱ现象:甲同学认为不可能发生析氢腐蚀,其判断依据是在金属活动性顺序中,Cu在H后,Cu不能置换出H2;乙同学认为实验Ⅱ中应发生吸氧腐蚀,其正极的电极反应式是O2+4H++4e-=2H2O.
(2)同学们仍用上述装置并用Cu和石墨为电极继续实验,探究实验Ⅱ指针偏转原因及影响O2氧化性的因素.
①丙同学比较实验Ⅱ、Ⅲ、Ⅳ的电压表读数为:c>a>b,请解释原因是O2浓度越大,其氧化性越强,使电压值增大.
②丁同学对Ⅳ、Ⅴ进行比较,其目的是探究对O2氧化性的溶液的酸碱性影响.
③实验Ⅳ中加入Na2SO4溶液的目的是排除溶液中的Na+(或SO42-)对实验的可能干扰.
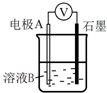
④为达到丁同学的目的,经讨论,同学们认为应改用如图装置对Ⅳ、Ⅴ重复进行实验,其设计意图是排除Cu在酸碱性不同的溶液中,其还原性不同对该实验结果的影响;重复实验时,记录电压表读数依次为c′、d′,且c′>d′,由此得出的结论是溶液酸性越强,O2的氧化性越强(介质或环境的pH影响物质的氧化性).
 某小组同学利用原电池装置探究物质的性质.
某小组同学利用原电池装置探究物质的性质.资料显示:原电池装置中,负极反应物的还原性越强,或正极反应物的氧化性越强,原电池的电压越大.
(1)同学们利用下表中装置进行实验并记录.
| 装置 | 编号 | 电极A | 溶液B | 操作及现象 |
 | Ⅰ | Fe | pH=2的 H2SO4 | 连接装置后,石墨表面产生无色气泡;电压表指针偏转 |
| Ⅱ | Cu | pH=2的H2SO4 | 连接装置后,石墨表面无明显现象;电压表指针偏转,记录读数为a |
②针对实验Ⅱ现象:甲同学认为不可能发生析氢腐蚀,其判断依据是在金属活动性顺序中,Cu在H后,Cu不能置换出H2;乙同学认为实验Ⅱ中应发生吸氧腐蚀,其正极的电极反应式是O2+4H++4e-=2H2O.
(2)同学们仍用上述装置并用Cu和石墨为电极继续实验,探究实验Ⅱ指针偏转原因及影响O2氧化性的因素.
| 编号 | 溶液B | 操作及现象 |
| Ⅲ | 经煮沸的pH=2的 H2SO4 | 溶液表面用煤油覆盖,连接装置后,电压表指针微微偏转,记录读数为b |
| Ⅳ | pH=2的H2SO4 | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为c;取出电极,向溶液中加入数滴浓Na2SO4溶液混合后,插入电极,保持O2通入,电压表读数仍为c |
| Ⅴ | pH=12的NaOH | 在石墨一侧缓慢通入O2并连接装置,电压表指针偏转,记录读数为d |
②丁同学对Ⅳ、Ⅴ进行比较,其目的是探究对O2氧化性的溶液的酸碱性影响.
③实验Ⅳ中加入Na2SO4溶液的目的是排除溶液中的Na+(或SO42-)对实验的可能干扰.
④为达到丁同学的目的,经讨论,同学们认为应改用如图装置对Ⅳ、Ⅴ重复进行实验,其设计意图是排除Cu在酸碱性不同的溶液中,其还原性不同对该实验结果的影响;重复实验时,记录电压表读数依次为c′、d′,且c′>d′,由此得出的结论是溶液酸性越强,O2的氧化性越强(介质或环境的pH影响物质的氧化性).
1.草酸钴可用于指示剂和催化剂的制备.用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)制取COC2O4•2H2O工艺流程如下:

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
(1)浸出过程中加入Na2SO3的目的是还原Fe3+、Co3+为Fe2+、Co2+.
(2)NaClO3在反应中氯元素被还原为最低价,该反应的离子方程式为ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O
(3)加Na2CO3能使浸出液中某些金属离子转化成氢氧化物沉淀.试用离子方程式和必要的文字简述其原理:加入的碳酸钠(或CO32-)与H+反应,c(H+)降低,使Fe3+和Al3+(用R3+代替)的水解平衡R3++3H2O?R(OH)3+3H+,向右移动,而产生氢氧化物沉淀
(4)滤液I“除钙、镁”是将其转化为MgF2、CaF2沉淀.已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,当加入过量NaF后,所得滤液$\frac{{c({M{g^{2+}}})}}{{c({C{a^{2+}}})}}$=0.7.
(5)萃取剂对金属离子的萃取率与pH的关系如图1所示,在滤液II中适宜萃取的pH为3.0~3.5左右.
(6)已知:NH3•H2O?NH4++OH- Kb=1.8×10-5;
H2C2O4?H++HC2O4- Ka1=5.4×10-2;HC2O4-?H+C2O42- Ka2=5.4×10-5
a.1 b.2 c.3 d.4
则该流程中所用(NH4)2C2O4溶液的pH<7(填“>”或“<”或“=”)
(7)CoC2O4•2H2O热分解质量变化过程如图2所示(其中600℃以前是隔绝空气加热,600℃以后是在空气中加热);A、B、C均为纯净物;C点所示产物的化学式是Co3O4(或CoO•Co2O3)


已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
(2)NaClO3在反应中氯元素被还原为最低价,该反应的离子方程式为ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O
(3)加Na2CO3能使浸出液中某些金属离子转化成氢氧化物沉淀.试用离子方程式和必要的文字简述其原理:加入的碳酸钠(或CO32-)与H+反应,c(H+)降低,使Fe3+和Al3+(用R3+代替)的水解平衡R3++3H2O?R(OH)3+3H+,向右移动,而产生氢氧化物沉淀
(4)滤液I“除钙、镁”是将其转化为MgF2、CaF2沉淀.已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,当加入过量NaF后,所得滤液$\frac{{c({M{g^{2+}}})}}{{c({C{a^{2+}}})}}$=0.7.
(5)萃取剂对金属离子的萃取率与pH的关系如图1所示,在滤液II中适宜萃取的pH为3.0~3.5左右.
(6)已知:NH3•H2O?NH4++OH- Kb=1.8×10-5;
H2C2O4?H++HC2O4- Ka1=5.4×10-2;HC2O4-?H+C2O42- Ka2=5.4×10-5
a.1 b.2 c.3 d.4
则该流程中所用(NH4)2C2O4溶液的pH<7(填“>”或“<”或“=”)
(7)CoC2O4•2H2O热分解质量变化过程如图2所示(其中600℃以前是隔绝空气加热,600℃以后是在空气中加热);A、B、C均为纯净物;C点所示产物的化学式是Co3O4(或CoO•Co2O3)

19.A、B、C三种元素的原子核外具有相同的电子层数,其最高价氧化物对应水化物的酸性强弱顺序是 HAO4>H2BO4>H3CO4,则下列判断中错误的是( )
| A. | 原子半径 A>B>C | B. | 气态氢化物的稳定性HA>H2B>H3C | ||
| C. | 阴离子还原性C3->B2->A- | D. | 非金属性A>B>C |
18.下列关于化学键的说法中,正确的是( )
| A. | 离子键就是阴、阳离子间的静电引力 | |
| B. | 共价化合物中只含有共价键 | |
| C. | 一个阳离子只可与一个阴离子之间存在离子键 | |
| D. | 金属元素和非金属元素化合一定形成离子键 |
17.下列物质中,既含有离子键又含有共价键的是( )
| A. | CO2 | B. | Na2O | C. | MgBr2 | D. | NH4Cl |
16.通常状况下,NC13是一种油状液体,其分子空间构型与氨分子相似,下列对NC13的有关叙述正确的是( )
0 154636 154644 154650 154654 154660 154662 154666 154672 154674 154680 154686 154690 154692 154696 154702 154704 154710 154714 154716 154720 154722 154726 154728 154730 154731 154732 154734 154735 154736 154738 154740 154744 154746 154750 154752 154756 154762 154764 154770 154774 154776 154780 154786 154792 154794 154800 154804 154806 154812 154816 154822 154830 203614
| A. | NCl3分子是非极性分子 | |
| B. | 分子中的所有原于均达到8电子稳定结构 | |
| C. | NBr3的熔点比NCl3的熔点低 | |
| D. | 分子中N-C1键键长比CCl4分子中C-C1键键长长 |
 ;
; .
.