8.在1L 1mol/L的氨水中,下列说法正确的是( )
| A. | 含1 mol NH3分子 | B. | 含NH3和NH4+之和为1mol | ||
| C. | 含NH3、NH4+、NH3•H2O之和为1 mol | D. | 含NH3•H2O 1mol |
5.设NA为阿伏加德罗常数的值.下列说正确的是( )
| A. | 室温下,1 L pH=13的NaOH溶液中,由水电离的OH-数目为0.1NA | |
| B. | 2.0gH218O与D216O的混合物中所含中子数为NA | |
| C. | 50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| D. | 常温常压下,4.4g乙醛所含σ键数目为0.7NA |
3.下表是元素周期表的一部分,针对表中的①~=10 ⑩中元素,填空回答以下问题:
(1)在这些元素中,室温下其单质为液态的元素在上表中对应的“序号”是⑩,其原子的原子结构示意图为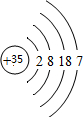 ;
;
(2)元素的最高价氧化物对应的水化物中酸性最强的是(填物质化学式,下同)HClO4,碱性最强的是KOH,
(3)②⑧⑩三种元素的氢化物中沸点最低的是(填氢化物化学式)HCl.
(4)室温下,其单质在冷浓硫酸或空气中,表面都生成致密的氧化膜,此元素在上表中对应的“序号”是⑤,其单质是能与NaOH溶液反应生成H2的“非金属”,该元素在上表中对应的“序号”是⑥,此反应的化学方程式是:Si+2NaOH+H2O=Na2SiO3+2H2↑,
(5)在②③④⑤⑦⑧元素中,原子半径最大的序号是⑧,离子半径最小的序号是⑤;
(6)⑦与⑩不在同一周期,也不在同族,但可通过一个化学反应判断出其阴离子还原性的强弱,此反应的离子方程式为:Br2+S2-═2Br-+S.
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
 ;
;(2)元素的最高价氧化物对应的水化物中酸性最强的是(填物质化学式,下同)HClO4,碱性最强的是KOH,
(3)②⑧⑩三种元素的氢化物中沸点最低的是(填氢化物化学式)HCl.
(4)室温下,其单质在冷浓硫酸或空气中,表面都生成致密的氧化膜,此元素在上表中对应的“序号”是⑤,其单质是能与NaOH溶液反应生成H2的“非金属”,该元素在上表中对应的“序号”是⑥,此反应的化学方程式是:Si+2NaOH+H2O=Na2SiO3+2H2↑,
(5)在②③④⑤⑦⑧元素中,原子半径最大的序号是⑧,离子半径最小的序号是⑤;
(6)⑦与⑩不在同一周期,也不在同族,但可通过一个化学反应判断出其阴离子还原性的强弱,此反应的离子方程式为:Br2+S2-═2Br-+S.
2.下列叙述,错误的是( )
| A. | 从上至下,卤素单质的密度依次增大,碱金属单质的密度也依次增大 | |
| B. | 从上至下,卤素单质的沸点逐渐升高,碱金属单质的熔点逐渐降低 | |
| C. | 除了I2外,其它卤素单质都能将Fe氧化到+3价 | |
| D. | F2不能从NaCl溶液中置换出Cl2 |
1.下列关于性质递变规律的叙述,不正确的是( )
| A. | 还原性Na>Mg>Al | B. | 氧化性Cl2>S>P | ||
| C. | 酸性H2SO4>H3PO4>HClO4 | D. | 稳定性HCl>H2S>PH3 |
20.常温下,将pH=5的硫酸溶液稀释500倍,c(SO42-)和c(H+)之比约为( )
| A. | 1:1 | B. | 1:2 | C. | 1:10 | D. | 10:1 |
19.在25℃时,在水中通入氯化氢气体,当溶液的pH等于3时,此时由水本身电离出的c(H+)是(mol•L-1)( )
0 154624 154632 154638 154642 154648 154650 154654 154660 154662 154668 154674 154678 154680 154684 154690 154692 154698 154702 154704 154708 154710 154714 154716 154718 154719 154720 154722 154723 154724 154726 154728 154732 154734 154738 154740 154744 154750 154752 154758 154762 154764 154768 154774 154780 154782 154788 154792 154794 154800 154804 154810 154818 203614
| A. | 10-3 | B. | 10-7 | C. | 10-11 | D. | 10-14 |
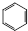 +HNO3$\stackrel{催化剂}{→}$
+HNO3$\stackrel{催化剂}{→}$ +H2O,反应类型取代反应
+H2O,反应类型取代反应 MgBr2
MgBr2