20.下列各项叙述中正确的是( )
| A. | 在同一个电子层上运动的电子,其自旋方向肯定不同 | |
| B. | 杂化轨道可用于形成σ键、π键或用于容纳未参与成键的孤电子对 | |
| C. | 物质的键能越大,该物质本身具有的能量越低 | |
| D. | 在周期表中原子的族序数等于它的最外层电子数 |
17.下列说法中正确的是( )
| A. | 物质发生化学反应都伴随着能量变化 | |
| B. | 伴有能量变化的物质变化都是化学变化 | |
| C. | 在一个确定的化学反应关系中,反应物的总能量与生产物的总能量有可能相同 | |
| D. | 如果旧化学键断裂吸收的能量大于新化学键形成释放的能量,则该反应为放热反应 |
16.下列各说法正确的是( )
| A. | 对于2SO2(g)+O2(g)?2SO3(g)△H=-QkJ/mol(Q>0),若向一密闭容器中加入1molSO2和0.5molO2充分反应后,放出的热量为0.5QkJ | |
| B. | 热化学方程式中的化学计量数表示相应物质的物质的量,不能用分数表示 | |
| C. | 需要加热才能发生的反应不一定是吸热反应 | |
| D. | 小苏打在水中的电离方程式:NaHCO3═Na++H++CO${\;}_{3}^{2-}$ |
15.根据元素周期表和元素周期律,下列推断中错误的是( )
| A. | 砹是一种有色固体,它的气态氢化物很不稳定 | |
| B. | F2与水反应比Cl2与水反应剧烈 | |
| C. | 铷的最高价氧化物的水化物一定是强碱 | |
| D. | 由Cl元素和S元素的最低化合价分别为-1和-2,推知元素的非金属性S>Cl |
14.按碳骨架分类,下列说法正确的是( )
| A. | 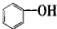 属于醇类化合物 属于醇类化合物 | B. | 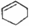 属于芳香族化合物 属于芳香族化合物 | ||
| C. | 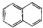 属于脂环化合物 属于脂环化合物 | D. | CH3CH(CH3)2 属于链状化合物 |
13.某溶液中Cl-、Br-、I-的物质的量之比为2:3:4.要使溶液中的Cl-、Br-、I-的物质的量之比变为4:3:2,则通入Cl2的物质的量与原溶液中I-的物质的量之比为( )
| A. | 4:1 | B. | 2:1 | C. | 1:4 | D. | 1:2 |
12.X、Y是元素周期表ⅦA族中的两种元素,X的非金属性比Y的强.则下列叙述中,正确的是( )
| A. | X原子的电子层数比Y原子的电子层数多 | |
| B. | X的单质一定能将Y从NaY的水溶液中置换出来 | |
| C. | X的单质比Y的单质更容易与氢气反应 | |
| D. | X的氢化物水溶液的酸性一定比Y的氢化物水溶液的酸性强 |
11.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
0 154560 154568 154574 154578 154584 154586 154590 154596 154598 154604 154610 154614 154616 154620 154626 154628 154634 154638 154640 154644 154646 154650 154652 154654 154655 154656 154658 154659 154660 154662 154664 154668 154670 154674 154676 154680 154686 154688 154694 154698 154700 154704 154710 154716 154718 154724 154728 154730 154736 154740 154746 154754 203614
| A. | 1 mol O2与Na完全反应,转移电子数一定为4NA | |
| B. | 22.4 L NH3中含有共价键的数目为3NA | |
| C. | 142 g Na2SO4和Na2HPO4混合物中含有的阴、阳离子总数是3NA | |
| D. | 标准状况下,11.2 L SO3所含的分子数目为0.5NA |