3.已知X、Y、Z、W、R是原子序数依次增大的五种短周期主族元素,其中Y、R原子最外层电子数相等;X元素最低负价绝对值与W元素最高正价相等;工业上常用电解熔融氧化物的方法冶炼W单质;Z、W、R的最高价氧化物对应的水化物两两反应均生成盐和水.下列说法正确的是( )
| A. | 原子半径由大到小的顺序:Z、W、Y | |
| B. | 简单气态氢化物的稳定性由强到弱的顺序:X、Y、R | |
| C. | W的最高价氧化物对应的水化物碱性比Z的强 | |
| D. | R的最高价氧化物对应的水化物化学式一定是HRO4 |
2.常温下,反应2H2S(g)+SO2(g)═3S(s)+2H2O(l)能自发进行.下列说法正确的是( )
| A. | 该反应为吸热反应 | |
| B. | 该反应中,SO2为还原剂 | |
| C. | 1 mol H2S中含有的共价键的数目为3 mol | |
| D. | 常温下,H2S的还原性强于S的还原性 |
1.下列说法正确的是( )
| A. | 分子式为C3H6的有机物只有两种同分异构体 | |
| B. | 标准状况下,22.4 L CCl4的质量为154 g | |
| C. | 选用适当的催化剂,既可以改变化学反应速率,也可以改变反应物的平衡转化率 | |
| D. | 2 g H2(g)在O2(g)中完全燃烧生成H2O(l)放出热量为285.8 kJ,则该反应的热化学方程式可表示为:2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ•mol-1 |
20.下列有关化学用语的表示正确的是( )
| A. | 质量数为37的氯原子:${\;}_{37}^{17}$Cl | B. | Al3+的结构示意图: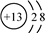 | ||
| C. | NaClO的电子式: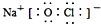 | D. | 硝基苯的结构简式: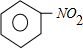 |
19.美好的生活离不开化学,我们应感恩化学,掌握必要的化学知识.下列说法错误的是( )
| A. | 合理使用化肥可以提高农作物的产量 | |
| B. | 二氧化氯、臭氧均可用作自来水消毒剂 | |
| C. | 氢氧化铝和碳酸钠均可用于治疗胃酸过多 | |
| D. | 化妆品中的甘油可起到保湿滋润皮肤的作用 |
17. 已知T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如表.
已知T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如表.
(1)TY2是一种常用的溶剂,是非极性分子(填“极性分子”或“非极性分子”),分子中存在2个σ键.W的最简单氢化物容易液化,理由是氟化氢分子之间存在着氢键.
(2)在25℃、101kPa下,已知13.5g的X固体单质在O2中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为4Al(s)+3 O2(g)=2Al2O3(s)△H=-3352kJ/mol.
(3)基态Y原子中,电子占据的最高能层符号为M;该能层具有的原子轨道数为9、电子数为6.Y、氧、W元素的电负性由大到小的顺序为F>O>S(用元素符号作答).
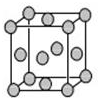
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00g•cm-3,则晶胞边长为$\root{3}{4.72×1{0}^{-23}}$(用含立方根的式子表示);
ZYO4常作电镀液,其中YO42-的空间构型是正四面体,其中Y原子的杂化轨道类型是sp3.Z的单质与人体分泌物中的盐酸以及空气反应可生成超氧酸:
Z+HCl+O2=ZCl+HO2,HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性.下列说法或表示正确的是AD
A.O2是氧化剂B.HO2是氧化产物
C.HO2在碱中能稳定存在D.1mol Z参加反应有1mol 电子发生转移.
 已知T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如表.
已知T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如表.| 元素 | 相关信息 |
| T | T元素可形成自然界硬度最大的单质 |
| W | W与T同周期,核外有一个未成对电子 |
| X | X原子的第一电离能至第四电离能分别是:I1=578kJ•mol-1,I2=1817kJ•mol-1, I3=2745kJ•mol-1,I4=11575kJ•mol-1 |
| Y | 常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质 |
| Z | Z的一种同位素的质量数为63,中子数为34 |
(2)在25℃、101kPa下,已知13.5g的X固体单质在O2中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为4Al(s)+3 O2(g)=2Al2O3(s)△H=-3352kJ/mol.
(3)基态Y原子中,电子占据的最高能层符号为M;该能层具有的原子轨道数为9、电子数为6.Y、氧、W元素的电负性由大到小的顺序为F>O>S(用元素符号作答).
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00g•cm-3,则晶胞边长为$\root{3}{4.72×1{0}^{-23}}$(用含立方根的式子表示);
ZYO4常作电镀液,其中YO42-的空间构型是正四面体,其中Y原子的杂化轨道类型是sp3.Z的单质与人体分泌物中的盐酸以及空气反应可生成超氧酸:
Z+HCl+O2=ZCl+HO2,HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性.下列说法或表示正确的是AD
A.O2是氧化剂B.HO2是氧化产物
C.HO2在碱中能稳定存在D.1mol Z参加反应有1mol 电子发生转移.
15.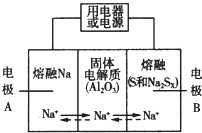 钠硫电池以熔融金属Na、熔融S和多硫化钠(Na2SX)分别作为两个电极的反应物,多孔固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:
钠硫电池以熔融金属Na、熔融S和多硫化钠(Na2SX)分别作为两个电极的反应物,多孔固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:
Na2SX$?_{放电}^{充电}$2Na+xS ( 3<x<5 )
(1)根据如表数据,判断该电池工作的适宜温度应为C(选填字母序号).
A.100℃以下
B.100℃~300℃
C.300℃~350℃
D.350℃~2050℃
(2)关于钠硫电池,下列说法正确的是AD(选填字母序号).
A.放电时,电极A为负极
B.放电时,Na+的移动方向为从B到A
C.充电时,电极A应连接电源的正极
D.充电时电极B的电极反应式为SX2--2e-=xS
(3)25℃时,若用钠硫电池作为电源电解500mL 0.2mol•L-1NaCl溶液,当溶液的pH变为l3时,电路中通过的电子的物质的量为0.05mol,两极的反应物的质量差为2.3g(假设电解前两极的反应物的质量相等).
 钠硫电池以熔融金属Na、熔融S和多硫化钠(Na2SX)分别作为两个电极的反应物,多孔固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:
钠硫电池以熔融金属Na、熔融S和多硫化钠(Na2SX)分别作为两个电极的反应物,多孔固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如图所示:Na2SX$?_{放电}^{充电}$2Na+xS ( 3<x<5 )
| 物质 | Na | S | Al2O3 |
| 熔点/℃ | 97.8 | 115 | 2050 |
| 沸点/℃ | 892 | 444.6 | 2980 |
A.100℃以下
B.100℃~300℃
C.300℃~350℃
D.350℃~2050℃
(2)关于钠硫电池,下列说法正确的是AD(选填字母序号).
A.放电时,电极A为负极
B.放电时,Na+的移动方向为从B到A
C.充电时,电极A应连接电源的正极
D.充电时电极B的电极反应式为SX2--2e-=xS
(3)25℃时,若用钠硫电池作为电源电解500mL 0.2mol•L-1NaCl溶液,当溶液的pH变为l3时,电路中通过的电子的物质的量为0.05mol,两极的反应物的质量差为2.3g(假设电解前两极的反应物的质量相等).
14.下列是从海藻灰和智利硝石矿层中提取碘的主要反应:
①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2
②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2
下列说法正确的是( )
0 154527 154535 154541 154545 154551 154553 154557 154563 154565 154571 154577 154581 154583 154587 154593 154595 154601 154605 154607 154611 154613 154617 154619 154621 154622 154623 154625 154626 154627 154629 154631 154635 154637 154641 154643 154647 154653 154655 154661 154665 154667 154671 154677 154683 154685 154691 154695 154697 154703 154707 154713 154721 203614
①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2
②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2
下列说法正确的是( )
| A. | 氧化性:MnO2>SO42->IO3->I2 | |
| B. | I2在反应①中是还原产物,在反应②中是氧化产物 | |
| C. | 反应①②中生成等量的I2时转移电子数之比为1:5 | |
| D. | NaHSO3溶液呈酸性,NaHSO3溶液中c(HSO3-)>c(H2SO3)>c(SO32-) |
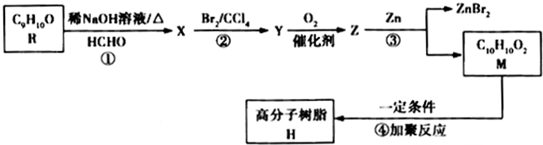
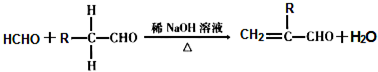
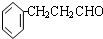 .
. .
. .
. .
. .
.