12.已知下列热化学方程式:
Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-24.8kJ•mol-1
3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H=-47.2kJ•mol-1
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.5kJ•mol-1
则14gCO气体与足量FeO充分反应得到Fe单质和CO2气体时的反应热为( )
Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-24.8kJ•mol-1
3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H=-47.2kJ•mol-1
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.5kJ•mol-1
则14gCO气体与足量FeO充分反应得到Fe单质和CO2气体时的反应热为( )
| A. | -109kJ•mol-1 | B. | -218kJ•mol-1 | C. | +109kJ•mol-1 | D. | +218kJ•mol-1 |
11.下列有机化学方程式书写正确的是( )
| A. | CH4+Cl2 $\stackrel{光照}{→}$CH2Cl2+H2 | |
| B. | 2CH3CH2OH+O2 $→_{△}^{催化剂}$2CH3CHO+H2O | |
| C. | CH3CH2OH+CH3COOH $\stackrel{浓硫酸}{→}$CH3COOCH2CH3 | |
| D. | H2C═CH2+Br2→CH3CHBr2 |
10.下列说法不正确的是( )
| A. | CH3CH2CH3与CH4互为同系物 | |
| B. | 乙醇和乙酸都能与金属钠反应 | |
| C. | 正丁烷(CH3CH2CH2CH3)与异丁烷(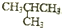 )互为同分异构体 )互为同分异构体 | |
| D. | 甲烷与苯在空气中燃烧的现象相同 |
9.毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备
BaCl2•2H2O的流程如下:

(1)写出“浸取”环节发生的主要反应的离子方程式:BaCO3+2H+═Ba2++CO2↑+H2O实验室用37%的盐酸配置15%的盐酸,除量筒外还需使用下列仪器中的ad.
a.烧杯 b.容量瓶 c.滴定管 d.玻璃棒
(2)下图是一些难溶氢氧化物在不同pH下的沉淀一溶解图

①滤渣I中含Fe(OH)3(填化学式).再加入NaOH调节pH=12.5可除去Mg2+、Ca2+(填离子
符号).
②加入H2C204应避免过量的原因是H2C2O4过量会导致生成BaC2O4沉淀,产品产量减少.
(3)25℃,H2C204和HF两种酸的电离平衡常数如下:
①HC2O4-的电离平衡常数表达式Ka2=$\frac{c({H}^{+})c({C}_{2}{{O}_{4}}^{2-})}{c(H{C}_{2}{{O}_{4}}^{2-})}$.
②H2C2O4溶液和NaF溶液反应的离子方程式为H2C2O4+F-═HF+HC2O4-.
BaCl2•2H2O的流程如下:

(1)写出“浸取”环节发生的主要反应的离子方程式:BaCO3+2H+═Ba2++CO2↑+H2O实验室用37%的盐酸配置15%的盐酸,除量筒外还需使用下列仪器中的ad.
a.烧杯 b.容量瓶 c.滴定管 d.玻璃棒
(2)下图是一些难溶氢氧化物在不同pH下的沉淀一溶解图

①滤渣I中含Fe(OH)3(填化学式).再加入NaOH调节pH=12.5可除去Mg2+、Ca2+(填离子
符号).
②加入H2C204应避免过量的原因是H2C2O4过量会导致生成BaC2O4沉淀,产品产量减少.
(3)25℃,H2C204和HF两种酸的电离平衡常数如下:
| H2C204 | Ka1=5.36×10-2 | Ka2=5.35×10-5 |
| HF | Ka=6.32×10-4 | |
②H2C2O4溶液和NaF溶液反应的离子方程式为H2C2O4+F-═HF+HC2O4-.
7.在标准状况下,将0.672L CO2通入含1.6g NaOH的溶液中,反应后得到Na2CO3和NaHCO3的混合物2.74g,则混合物中Na2CO3和NaHCO3的物质的量之比为( )
| A. | 2:3 | B. | 1:2 | C. | 3:1 | D. | 1:3 |
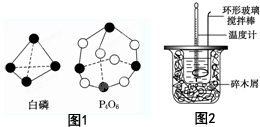
6. Na2CO3和NaHCO3与盐酸反应热效应的测定.按如图所示连接好装置,为探究NaHCO3、Na2CO3和盐酸反应过程中的热效应,进行实验并测得如下数据:
Na2CO3和NaHCO3与盐酸反应热效应的测定.按如图所示连接好装置,为探究NaHCO3、Na2CO3和盐酸反应过程中的热效应,进行实验并测得如下数据:
由上述数据所得出的以下结论中,正确的是( )
A.NaHCO3(s)的溶解是放热过程
B.Na2CO3(s)的溶解是吸热过程
C.Na2CO3(s)与盐酸的反应是放热反应
D.仅根据实验③就可以确定HCO3-(aq)+H+(aq)═CO2(g)+H2O(l)△H>0.
 Na2CO3和NaHCO3与盐酸反应热效应的测定.按如图所示连接好装置,为探究NaHCO3、Na2CO3和盐酸反应过程中的热效应,进行实验并测得如下数据:
Na2CO3和NaHCO3与盐酸反应热效应的测定.按如图所示连接好装置,为探究NaHCO3、Na2CO3和盐酸反应过程中的热效应,进行实验并测得如下数据:| 序号 | 48mL试剂 | 固体 | 混合前温度/℃ | 混合后温度/℃ |
| ① | 水 | 2 g NaHCO3 | 20.0 | 18.6 |
| ② | 水 | 2 g Na2CO3 | 20.0 | 21.6 |
| ③ | 盐酸(0.1mol•L-1) | 2 g NaHCO3 | 20.0 | 17.2 |
| ④ | 盐酸(0.1mol•L-1) | 2 g Na2CO3 | 20.0 | 22.6 |
A.NaHCO3(s)的溶解是放热过程
B.Na2CO3(s)的溶解是吸热过程
C.Na2CO3(s)与盐酸的反应是放热反应
D.仅根据实验③就可以确定HCO3-(aq)+H+(aq)═CO2(g)+H2O(l)△H>0.
5.分类是化学学习中经常用到的方法,下列对一些物质或化学反应的分类以及依据正确的是(双选)( )
0 154432 154440 154446 154450 154456 154458 154462 154468 154470 154476 154482 154486 154488 154492 154498 154500 154506 154510 154512 154516 154518 154522 154524 154526 154527 154528 154530 154531 154532 154534 154536 154540 154542 154546 154548 154552 154558 154560 154566 154570 154572 154576 154582 154588 154590 154596 154600 154602 154608 154612 154618 154626 203614
| A. | H2SO4是酸,因为H2SO4中含有氢元素 | |
| B. | 豆浆是胶体,因为豆浆中的分散质粒子直径在1~100 nm之间 | |
| C. | Na在Cl2中燃烧属于氧化还原反应,因为反应中有电子得失 | |
| D. | Na和H2O的反应不是离子反应,因为反应中没有离子参加 |
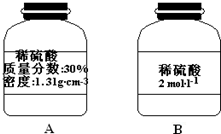
 (1)已知:2SO2(g)+O2═2SO3(g)△H=-196.6kJ•mol-1,2NO(g)+O2═2NO2(g)△H=-113.0kJ•mol-1.则反应NO2(g)+SO2(g)═SO3(g)+NO(g) 的△H=-41.8kJ/mol.
(1)已知:2SO2(g)+O2═2SO3(g)△H=-196.6kJ•mol-1,2NO(g)+O2═2NO2(g)△H=-113.0kJ•mol-1.则反应NO2(g)+SO2(g)═SO3(g)+NO(g) 的△H=-41.8kJ/mol.