1.已知 X、Y、U、V、W、Z是六种常见元素,其中X、Y、U、V、W五种短周期元素在周期表中的位置如图所示:
U的最简单气态氢化物能使湿润的红色石蕊试纸变蓝.Z是人体血红蛋白中存在的金属元素.请填写下列空白:
(1)Z元素在周期表中的位置第四周期第Ⅷ族,W的原子结构示意图
(2)X、U、V、W形成的简单离子半径由大到小的顺序为S2->Cl->N3->Al3+(用离子符号表示)
(3)用电子式表示Y的最高价氧化物的形成过程
(4)X、W两元素的最高价氧化物对应水化物能相互反应,该反应的离子方程式为Al(OH)3+3H+=Al3++3H2O
(5)Na2V的水溶液呈碱性,用离子方程式解释其原因S2-+H2O?HS-+OH-,其水溶液中离子浓度由大到小的顺序为c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+).
| Y | U | |||
| X | V | W |
(1)Z元素在周期表中的位置第四周期第Ⅷ族,W的原子结构示意图

(2)X、U、V、W形成的简单离子半径由大到小的顺序为S2->Cl->N3->Al3+(用离子符号表示)
(3)用电子式表示Y的最高价氧化物的形成过程

(4)X、W两元素的最高价氧化物对应水化物能相互反应,该反应的离子方程式为Al(OH)3+3H+=Al3++3H2O
(5)Na2V的水溶液呈碱性,用离子方程式解释其原因S2-+H2O?HS-+OH-,其水溶液中离子浓度由大到小的顺序为c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+).
20.下列说法正确的是( )
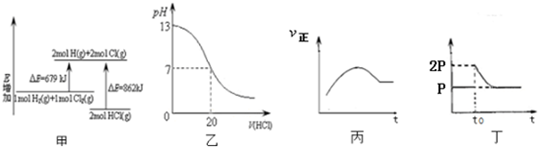

| A. | 图甲表示H2(g)+Cl2(g)=2HCl(g)的能量变化,则该反应的反应热△H=+183 kJ/mol | |
| B. | 图乙表示室温时用0.1 mol/L盐酸滴定20 mL 0.1 mol/LNaOH溶液,溶液pH变化 | |
| C. | 图丙表示向恒容绝热的密闭容器中通入A和B,发生2A (g)+B (g)?2C(g)反应,其正反应速率随时间变化的示意图,则该反应为吸热反应 | |
| D. | 图丁表示在恒温密闭容器中,2BaO2(s)?2BaO(s)+O2(g)达到平衡,t0时刻将容器体积缩小为原来的1/2,体系重新达到平衡过程体系压强的变化 |
19.下列装置所示的实验能达到目的是( )
| A. |  检验装置气密性 | B. | 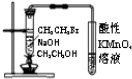 验证溴乙烷发生消去反应生成乙烯 | ||
| C. |  测定中和热 | D. | 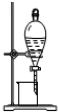 从碘的CCl4溶液中分离出碘 |
18.根据如图回答,下列说法不正确的是( )
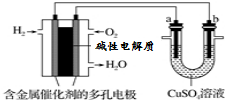

| A. | 此装置用于电镀铜时,电解一段时间,硫酸铜溶液的浓度不变 | |
| B. | 若a为纯铜,b为粗铜,该装置可用于粗铜的电解精炼 | |
| C. | 燃料电池中正极反应为O2+4e-+2H2O=4OH- | |
| D. | 电子经导线流入b电极 |
17.下列说法中正确的是( )
| A. | 能使石蕊溶液呈红色的溶液:Fe2+、Na+、Ba2+、Cr2O72-可以大量共存 | |
| B. | 氢氧化钡溶液与等物质的量的稀硫酸混合,离子方程式为:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| C. | 50℃,pH=1的硫酸溶液中:c(H+)=0.1mol/L | |
| D. | 25℃,pH相同的NaOH、CH3COONa、Na2CO3、NaHCO3溶液的浓度c (NaOH)<c (CH3COONa)<c (NaHCO3)<c (Na2CO3) |
16.下列描述正确的是( )
| A. | 16O→18O的转化属于化学变化 | |
| B. | 冰醋酸、消石灰、明矾、生石灰分别属于酸、碱、盐、氧化物 | |
| C. | SiO2既能与氢氟酸反应,也能与氢氧化钠溶液反应,属于两性氧化物 | |
| D. | 少量Cu将足量浓、稀硝酸分别还原为NO2和NO,其转移电子数之比为1:3 |
15.化学与生活密切相关,下列说法正确的是( )
0 154427 154435 154441 154445 154451 154453 154457 154463 154465 154471 154477 154481 154483 154487 154493 154495 154501 154505 154507 154511 154513 154517 154519 154521 154522 154523 154525 154526 154527 154529 154531 154535 154537 154541 154543 154547 154553 154555 154561 154565 154567 154571 154577 154583 154585 154591 154595 154597 154603 154607 154613 154621 203614
| A. | 绿色化学的核心就是治理工业生产对环境产生的污染 | |
| B. | 铁、钙、碘都是人体必不可少的微量元素 | |
| C. | 食盐可作调味剂,但不可作食品防腐剂 | |
| D. | “地沟油”经过加工处理后,可以用来制肥皂和生物柴油 |

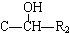 (R代表烃基或氢原子,下同.)
(R代表烃基或氢原子,下同.)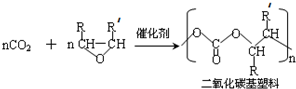
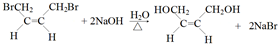 ,反应④的化学反应方程式
,反应④的化学反应方程式 ,反应⑤的化学反应方程式
,反应⑤的化学反应方程式
 和高分子化合物PCL的合成路线如下:
和高分子化合物PCL的合成路线如下:
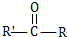 $\stackrel{过氧化物}{→}$
$\stackrel{过氧化物}{→}$ (R、R′代表烃基)
(R、R′代表烃基)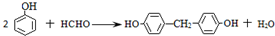 .
. .
.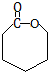 .高分子化合物PCL的结构简式是
.高分子化合物PCL的结构简式是 .
. 、
、 .
.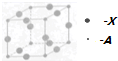 A、B、C、D、X五种元素的原子序数依次递增,A、B的常见单质是构成空气的主要成分;C 的基态原子核外电子占有7个轨道,但只有1个未成对电子;D的基态原子的M能层中只有1对成对电子和2个未成对电子;X元素处于第四周期ⅠB族.
A、B、C、D、X五种元素的原子序数依次递增,A、B的常见单质是构成空气的主要成分;C 的基态原子核外电子占有7个轨道,但只有1个未成对电子;D的基态原子的M能层中只有1对成对电子和2个未成对电子;X元素处于第四周期ⅠB族.