2.镍镉(Ni-Cd)可充电电池在现代生活中有广泛的应用.已知镍镉电池的电解质溶液是KOH溶液,放电时的电池反应是:Cd+2NiO(OH)+2H2O=Cd(OH)2+2Ni(OH)2,下列说法正确的是( )
| A. | 放电时电解质溶液的密度减小 | B. | 放电时K+向Cd极区移动 | ||
| C. | 充电时阳极Cd元素被氧化 | D. | 充电时阴极附近的pH增大 |
1.设NA为阿伏加德罗常数值,下列说法中正确的是( )
| A. | 氧化还原反应中,若消耗7.1g Cl2,必转移0.2NA个电子 | |
| B. | 将1.0molFeCl3全部制成胶体,其中氢氧化铁胶粒为NA个 | |
| C. | 12g NaHSO4在熔融时离子总数为0.3NA | |
| D. | 标准状况下,11.2L氦气所含的原子数为0.5NA |
20.关于aL bmol/L的浓硫酸的说法正确的是( )
| A. | 与足量Cu共热,转移的电子为ab mol | |
| B. | 常温时加入Al,不会发生化学反应 | |
| C. | 若加入mg Zn片,Zn片完全溶解,可收集到的标准状况下气体体积为22.4m/65 L | |
| D. | 蔗糖与浓硫酸混合,只体现浓硫酸的脱水性 |
19.下列说法正确的是( )
| A. | 可用丁达尔现象区分溶液与胶体 | |
| B. | 化学变化能够实现一种原子变为另一种原子 | |
| C. | O3是由3个氧原子构成的化合物 | |
| D. | CuSO4•5H2O是一种混合物 |
18.下列有关硫酸和硝酸的说法中正确的是( )
| A. | 将过量的Zn投入一定量的浓H2SO4中,最终生成的气体只有SO2 | |
| B. | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 | |
| C. | 向50mL12mol•L-1的浓硝酸中加入足量铜片其充分反应,生成0.3molNO2 | |
| D. | 运输保存浓硫酸的槽罐车一旦泄露后应立即用大量水冲洗 |
16.一定温度下,有两个体积均为2L的恒容密闭容器Ⅰ和Ⅱ,向Ⅰ中加入1molCO和2molH2,向Ⅱ中加入2molCO和4molH2,均发生下列反应,并建立平衡:CO(g)+2H2(g)?CH3OH(g).测得不同温度下CO平衡转化率如图所示.下列说法正确的是( )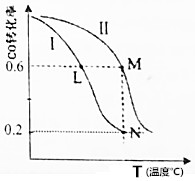

| A. | 该反应的△H>0 | |
| B. | M点化学平衡常数K=0.59 | |
| C. | L、M两点容器内压强:P(M)>2P(L) | |
| D. | 向N点平衡体系中再加入1molCH3OH,建立新平衡时被分解的CH3OH物质的量小于0.4mol |
15.下列各组中的两种物质在溶液中的反应,可用同一离子方程式表示的是( )
| A. | Ba(OH)2和 盐酸; Ba(OH)2 和 H2SO4 | |
| B. | BaCl2 和 Na2SO4; Ba(OH)2 和 (NH4)2SO4 | |
| C. | NaHCO3和 H2SO4; Ca(HCO3)2 和 HNO3 | |
| D. | Ba(OH)2 和 HNO3; Cu(OH)2 和 H2SO4 |
14.已知aAn+,bB(n+1)+,cCn-,dD(n+1)-是具有相同的电子层结构的短周期元素形成的简单离子,下列叙述正确的是( )
| A. | 原子半径:C>D>A>B | B. | 原子序数:b>a>c>d | ||
| C. | 离子半径:Cn+>D(n+)->An+>B(n+)+ | D. | 单质还原性:A>B>C>D |
13.下列分子中的所有原子满足最外层8个电子结构结构的是( )
0 154391 154399 154405 154409 154415 154417 154421 154427 154429 154435 154441 154445 154447 154451 154457 154459 154465 154469 154471 154475 154477 154481 154483 154485 154486 154487 154489 154490 154491 154493 154495 154499 154501 154505 154507 154511 154517 154519 154525 154529 154531 154535 154541 154547 154549 154555 154559 154561 154567 154571 154577 154585 203614
| A. | HCl | B. | BF3 | C. | NCl3 | D. | PCl5 |