6.1.52g铜镁合金完全溶解于足量的浓硝酸中,得到NO2气体1344mL (标准状况),向反应后的溶液中加入1.0mol/L NaOH溶液,发现金属离子全部沉淀,下列说法不正确的是( )
| A. | 该合金中铜与镁的物质的量之比是2:1 | |
| B. | 可得到2.54 g沉淀 | |
| C. | 如果是铜铝合金,则产生的NO2 的体积不会是1344mL | |
| D. | 恰好全部沉淀时,加入NaOH溶液的体积是600 mL |
18.常温下,在10mL 0.1mol•L-1 Na2CO3溶液中逐滴加入0.1mol•L-1 HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法不正确的是( )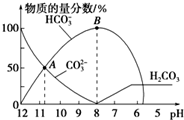

| A. | 在A点所示的溶液中:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-) | |
| B. | 在B点所示的溶液中,浓度最大的离子是Na+ | |
| C. | 当溶液的pH为7时,溶液的总体积大于20mL | |
| D. | 25℃时,CO32-水解常数Kh=2×10-4mol•L-1,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH=10 |
17. 已知:H2SO3?HSO${\;}_{3}^{-}$+H+ Ka1、HSO${\;}_{3}^{-}$?SO${\;}_{3}^{2-}$+H+ Ka2
已知:H2SO3?HSO${\;}_{3}^{-}$+H+ Ka1、HSO${\;}_{3}^{-}$?SO${\;}_{3}^{2-}$+H+ Ka2
常温下,向某浓度的H2SO3溶液中逐滴加入一定量浓度的NaOH溶液,所得溶液中H2SO3、HSO3-和SO32-三种微粒的物质的量分数与溶液的关系如图所示,则下列说法中不正确的是( )
0 154367 154375 154381 154385 154391 154393 154397 154403 154405 154411 154417 154421 154423 154427 154433 154435 154441 154445 154447 154451 154453 154457 154459 154461 154462 154463 154465 154466 154467 154469 154471 154475 154477 154481 154483 154487 154493 154495 154501 154505 154507 154511 154517 154523 154525 154531 154535 154537 154543 154547 154553 154561 203614
 已知:H2SO3?HSO${\;}_{3}^{-}$+H+ Ka1、HSO${\;}_{3}^{-}$?SO${\;}_{3}^{2-}$+H+ Ka2
已知:H2SO3?HSO${\;}_{3}^{-}$+H+ Ka1、HSO${\;}_{3}^{-}$?SO${\;}_{3}^{2-}$+H+ Ka2常温下,向某浓度的H2SO3溶液中逐滴加入一定量浓度的NaOH溶液,所得溶液中H2SO3、HSO3-和SO32-三种微粒的物质的量分数与溶液的关系如图所示,则下列说法中不正确的是( )
| A. | 曲线3表示的微粒是SO32- | |
| B. | 溶液pH=4.2时,c(Na+)+c(H+)=c(OH-)+2c(SO32-) | |
| C. | 常温下,$\frac{{K}_{a1}}{{K}_{a2}}$=1000 | |
| D. | 溶液pH=1.2时:c(Na+)+c(H+)=c(OH-)+c(HSO3) |
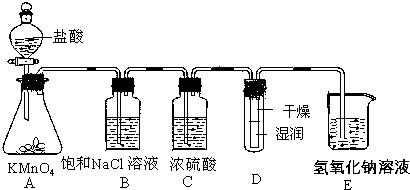

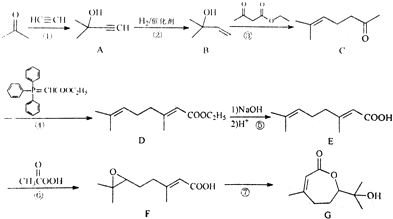
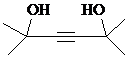 .
.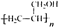 ,写出合成流程图(无机试剂任用).合成流程图示例如下:
,写出合成流程图(无机试剂任用).合成流程图示例如下: