14.下列说法正确的是( )
| A. | 通常状况下,1 g氢气燃烧生成液态水时放出142.9 kJ热量,则表示氢气燃烧热的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=-142.9 kJ•mol-1 | |
| B. | 已知:H2(g)+F2(g)═2HF(g)△H=-270 kJ•mol-1,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ | |
| C. | 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ•mol-1 | |
| D. | 已知:①C(s,石墨)+O2(g)═CO2(g)△H=-393.5 kJ•mol-1,②C(s,金刚石)+O2(g)═CO2(g)△H=-395.0 kJ•mol-1,则C(s,金刚石)═C(s,石墨)△H=-1.5 kJ•mol-1 |
13.下列事实一定能证明HNO2是弱电解质的是( )
①常温下NaNO2溶液的pH大于7
②用HNO2溶液做导电实验,灯泡很暗
③HNO2和NaCl不能发生反应
④常温下0.1mol•L-1 HNO2溶液的pH=2.1
⑤常温下pH=3的 HNO2溶液和pH=11的NaOH溶液等体积混合,pH小于7
⑥常温下pH=2的 HNO2溶液稀释至100倍,pH约为3.1.
①常温下NaNO2溶液的pH大于7
②用HNO2溶液做导电实验,灯泡很暗
③HNO2和NaCl不能发生反应
④常温下0.1mol•L-1 HNO2溶液的pH=2.1
⑤常温下pH=3的 HNO2溶液和pH=11的NaOH溶液等体积混合,pH小于7
⑥常温下pH=2的 HNO2溶液稀释至100倍,pH约为3.1.
| A. | ①④⑥ | B. | ①②③④ | C. | ①④⑤⑥ | D. | 全部 |
11.下列说法中,不正确的是( )
| A. | 由于蒸发溶剂而析出晶体后的溶液仍为饱和溶液 | |
| B. | 在饱和溶液中,溶质的溶解速率等于结晶速率 | |
| C. | 任何物质的饱和溶液升高温度时,都变成不饱和溶液 | |
| D. | 溶质刚开始溶解时的溶液为不饱和溶液 |
10.下列物质中,含有Cl-的是( )
①盐酸
②氯化钠溶液
③氯化钠固体
④次氯酸
⑤氯化氢气体.
①盐酸
②氯化钠溶液
③氯化钠固体
④次氯酸
⑤氯化氢气体.
| A. | ①②⑤ | B. | ①②③ | C. | ③④⑤ | D. | ②④⑤ |
9.具有下列电子数的微粒,能确定它的质子数的是( )
| A. | 2 | B. | 8 | C. | 10 | D. | 18 |
8.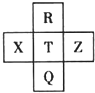 元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
 元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )| A. | 非金属性:Z<T<X | |
| B. | X最高价氧化物的水化物的表达式为H2XO4 | |
| C. | 气态氢化物稳定性:R<T<Q | |
| D. | R与Q的电子数相差26 |
7.用48g乙醇(其中的氧用18O标记)在浓硫酸存在条件下与足量的乙酸充分反应.下列有关叙述中不正确的是( )
| A. | 生成的水分子中含有18O | B. | 生成的乙酸乙酯中含有18O | ||
| C. | 可能生成88g乙酸乙酯 | D. | 不可能生成90g乙酸乙酯 |
6.下列有机化合物的分类不正确的是( )
| A. |  不饱和烃 | B. |  芳香族化合物 | C. | 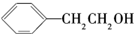 醇 醇 | D. |  苯的同系物 |
5.将盛有NH4HCO3的试管加热,使放出的气体依次通过盛有足量Na2O2的干燥管,足量浓H2SO4的洗气瓶,最后得到的气体( )
0 154322 154330 154336 154340 154346 154348 154352 154358 154360 154366 154372 154376 154378 154382 154388 154390 154396 154400 154402 154406 154408 154412 154414 154416 154417 154418 154420 154421 154422 154424 154426 154430 154432 154436 154438 154442 154448 154450 154456 154460 154462 154466 154472 154478 154480 154486 154490 154492 154498 154502 154508 154516 203614
| A. | NH3 | B. | O2 | C. | H2O | D. | CO2 |