4.如图是一种微生物燃料电池的原理示意图.下列有关该微生物燃料电池的说法正确的是( ) 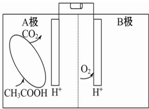

| A. | A极为正极,B极为负极 | |
| B. | 电池内电解质溶液中所含的H+由B极移向A极 | |
| C. | A极的电极反应为:CH3COOH-8e-+2H2O═2CO2↑+8H+ | |
| D. | 电池工作过程中,电解质溶液的pH会明显下降 |
2.下列各物质中,一定是同系物的是( )
| A. | C3H6和2-甲基1-丁烯 | |
| B. | 3,3-二甲基-1-丁炔和3-甲基1-戊炔 | |
| C. |  和 和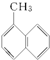 | |
| D. | C4H10和C9H20 |
1.下列有关说法正确的是( )
| A. | 常温下pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度前者比后者大 | |
| B. | 反应Hg(1)+H2SO4(aq)=HgSO4(aq)+H2(g)在常温下不能自发进行,则△H>0 | |
| C. | 将纯水加热至较高温度,K变大、pH变小、呈酸性 | |
| D. | N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时增大氮气的浓度,正逆反应速率均增大,平衡正向移动,氢气的转化率提高 |
19.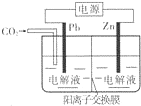 采用电化学法还原CO2是一种使CO2资源化的方法,下图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )
采用电化学法还原CO2是一种使CO2资源化的方法,下图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )
 采用电化学法还原CO2是一种使CO2资源化的方法,下图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )
采用电化学法还原CO2是一种使CO2资源化的方法,下图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )| A. | Zn与电源的负极相连 | |
| B. | ZnC2O4在交换膜右侧生成 | |
| C. | 电解的总反应为:2C02+Zn$\frac{\underline{\;电解\;}}{\;}$ZnC2O4 | |
| D. | 通入11.2 L CO2时,转移0.5 mol电子 |
18.短周期的四种非金属元素m、n、p、q原子序数依次增大,n与q为同主族元素,m和p原子最外层电子数之和等于n和q原子最外层电子数之和,p的单质在常温下能与水剧烈反应.下列说法一定正确的是( )
| A. | 原子半径:m>n | B. | 氢化物的稳定性:n>p | ||
| C. | q的最高价氧化物的水化物为强酸 | D. | n在自然界中能以游离态存在 |
17.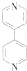 金属有机骨架材料(MOFs)为继碳纳米管后的又一种新型多孔材料.如图所示有机物可用于合成该材料,下列有关该有机物的说法不正确的是( )
金属有机骨架材料(MOFs)为继碳纳米管后的又一种新型多孔材料.如图所示有机物可用于合成该材料,下列有关该有机物的说法不正确的是( )
 金属有机骨架材料(MOFs)为继碳纳米管后的又一种新型多孔材料.如图所示有机物可用于合成该材料,下列有关该有机物的说法不正确的是( )
金属有机骨架材料(MOFs)为继碳纳米管后的又一种新型多孔材料.如图所示有机物可用于合成该材料,下列有关该有机物的说法不正确的是( )| A. | 6.8g该有机物含0.2 molN | |
| B. | 该有机物能发生加成反应 | |
| C. | 该有机物的一氯代物只有2种 | |
| D. | 分子中的所有原子可能处于同一平面 |
16.下列离子方程式或电离方程式正确的是( )
| A. | NaHSO3溶液呈酸性:NaHSO3═Na++H++S032- | |
| B. | 向Na2SiO3溶液中通人少量CO2:SiO32-+CO2+H2O═H2SiO3↓+CO32- | |
| C. | 将一小块钠投入稀醋酸中:2Na+2H+═2Na++H2 | |
| D. | 在Na2S203溶液中滴加稀硝酸:2H++S2O32-═S+SO2+H2O |
15.下列叙述正确的是( )
0 154245 154253 154259 154263 154269 154271 154275 154281 154283 154289 154295 154299 154301 154305 154311 154313 154319 154323 154325 154329 154331 154335 154337 154339 154340 154341 154343 154344 154345 154347 154349 154353 154355 154359 154361 154365 154371 154373 154379 154383 154385 154389 154395 154401 154403 154409 154413 154415 154421 154425 154431 154439 203614
| A. | 工业上利用电解法冶炼铝和铁 | |
| B. | 生产和生活中常用可溶性铝盐和铜盐净水 | |
| C. | 工业合成氨的反应属于能自发进行的反应,故能迅速发生 | |
| D. | 热的纯碱溶液清洗带油污的餐具与盐类和酯类的水解均有关 |
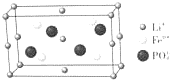 锂的某些化合物是性能优异的材料.请回答:
锂的某些化合物是性能优异的材料.请回答: