16.有一真空密闭容器中,盛有amolPCl5,加热到200℃时,发生如下反应PCl5(g)?PCl3(g)+Cl2(g),反应达平衡时,PCl5所占体积分数为M%,若在同一温度下,同一容器中,最初投入2amolPCl5反应达平衡时,PCl5所占体积分数为N%,则M与N的关系正确的是( )
| A. | M<N | B. | 2M=N | C. | N<M | D. | M=N |
12.下表列出了①~⑨九种元素在周期表中的位置:
请按要求回答下列问题.
(1)化学性质最不活泼的元素的原子结构示意图为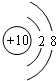
(2)⑥④⑦的氢化物的稳定性最强的是:H2O(写氢化物的化学式);
(3)元素③④⑤形成的离子半径由大到小的顺序是N3->O2->Na+(用离子符号表示)
(4)用电子式表示元素⑤与⑦的化合物的形成过程: .
.
| ⅠA | Ⅷ | ||||||
| ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| ② | ③ | ④ | ⑧ | ||||
| ⑤ | ⑥ | ⑦ | ⑨ | ||||
(1)化学性质最不活泼的元素的原子结构示意图为
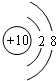
(2)⑥④⑦的氢化物的稳定性最强的是:H2O(写氢化物的化学式);
(3)元素③④⑤形成的离子半径由大到小的顺序是N3->O2->Na+(用离子符号表示)
(4)用电子式表示元素⑤与⑦的化合物的形成过程:
 .
.
11.氢化钠(NaH)是一种白色的离子化合物,其中钠元素是+1价;氢化钠与水反应生成H2和NaOH.下列叙述中,不正确的是( )
| A. | NaH的电子式为Na+[:H]- | |
| B. | NaH中氢元素的离子的电子层排布与氦原子的电子层排布相同 | |
| C. | 微粒半径H-<Li+ | |
| D. | NaH与H2O反应时,水作氧化剂 |
10.短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,已知Y、W的原子序数之和是Z的3倍,下列说法正确的是( )
| Y | Z | ||
| X | W |
| A. | 原子半径:X<Y<Z | |
| B. | 最高价氧化物的水化物的酸性:Y<W | |
| C. | 原子序数:X>W>Z>Y | |
| D. | Z、Y的单质均可与H2反应,且反应的剧烈程度:Y>Z |
9.(1)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式:H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ•mol-1.已知18g液态水转化成水蒸气需吸热44kJ,则反应2H2(g)+O2(g)═2H2O(l)的△H=-571.6kJ•mol-1,氢气的标准燃烧热△H=-285.8kJ•mol-1.
(2)已知H2(g)+Cl2(g)═2HCl(g)△H=-184.6kJ•mol-1.其它相关数据如下表:
则表中a为431.8.
(3)已知:2SO2(g)+O2(g)═2SO3(g)△H=-196.6kJ•mol-1
2NO(g)+O2(g)═2NO2(g)△H=-113.0kJ•mol-1
则反应NO2(g)+SO2(g)═SO3(g)+NO(g)的△H=-41.8kJ•mol-1.
0 154205 154213 154219 154223 154229 154231 154235 154241 154243 154249 154255 154259 154261 154265 154271 154273 154279 154283 154285 154289 154291 154295 154297 154299 154300 154301 154303 154304 154305 154307 154309 154313 154315 154319 154321 154325 154331 154333 154339 154343 154345 154349 154355 154361 154363 154369 154373 154375 154381 154385 154391 154399 203614
(2)已知H2(g)+Cl2(g)═2HCl(g)△H=-184.6kJ•mol-1.其它相关数据如下表:
| H2(g) | Cl2 (g) | HCl (g) | |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | 243 | a |
(3)已知:2SO2(g)+O2(g)═2SO3(g)△H=-196.6kJ•mol-1
2NO(g)+O2(g)═2NO2(g)△H=-113.0kJ•mol-1
则反应NO2(g)+SO2(g)═SO3(g)+NO(g)的△H=-41.8kJ•mol-1.
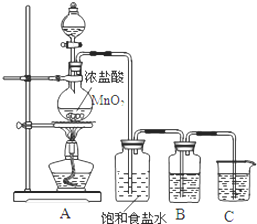 为验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
为验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题: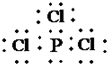 .
.
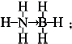 ;与氨硼烷互为等电子体的有机小分子是CH3CH3(写结构简式).
;与氨硼烷互为等电子体的有机小分子是CH3CH3(写结构简式).