7. 如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )
如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )
 如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )
如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.下列说法不正确的是( )| A. | 电子由O2所在的铂电极流出 | |
| B. | 该电池的负极反应式为:CH3CH2OH+H2O-4e-═CH3COOH+4H+ | |
| C. | O2所在的铂电极处发生还原反应 | |
| D. | 微处理器通过检测电流大小计算出被测气体中酒精的含量 |
6.下列说法或表示方法正确的是( )
| A. | 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 | |
| B. | 在稀溶液中,H+(aq)+OH-(aq)═H2O(l);△H=-57.3 kJ/mol,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量等于57.3 kJ | |
| C. | 由C(石墨)=C(金刚石)△H=+1.90 kJ/mol可知石墨比金刚石稳定 | |
| D. | 在101 kPa时,2 g H2 完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(g)△H=-571.6kJ/mol |
5.用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 1 mol N2所含有的原子数为NA | |
| B. | 标准状况下,22.4 L水中含有的水分子数为NA | |
| C. | 24 g O2分子和24 g O3分子所含的氧原子数目相等 | |
| D. | 1mol•L-1的盐酸中氯离子为NA |
2.根据下列反应判断有关物质还原性由强到弱的顺序是( )
H2SO3+I2+H2O═2HI+H2SO4;2FeCl3+2HI═2FeCl2+2HCl+I2.
H2SO3+I2+H2O═2HI+H2SO4;2FeCl3+2HI═2FeCl2+2HCl+I2.
| A. | FeCl2>HI>H2SO3 | B. | HI>FeCl2>H2SO3 | C. | H2SO3>HI>FeCl2 | D. | FeCl2>H2SO3>HI |
17.原子序数依次增大的X、Y、Z、W四中短周期元素,X、W原子的最外层电子数与其电子层数相等,X、Z的最外层电子数之和与Y、W的最外层电子数之和相等.气体甲由X、Y两种元素组成,其在标准状况下的密度为0.76g•L-1,下列说法正确的是( )
| A. | 非金属性:X<W<Y<Z | |
| B. | X的简单阴离子和Z、W的简单离子均能促进水的电离 | |
| C. | 原子半径:Z<Y<W,而简单离子半径:W<Y<Z | |
| D. | Y的最高价氧化物对应的水化物与W的单质反应可制备X的单质 |
16.下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
0 154136 154144 154150 154154 154160 154162 154166 154172 154174 154180 154186 154190 154192 154196 154202 154204 154210 154214 154216 154220 154222 154226 154228 154230 154231 154232 154234 154235 154236 154238 154240 154244 154246 154250 154252 154256 154262 154264 154270 154274 154276 154280 154286 154292 154294 154300 154304 154306 154312 154316 154322 154330 203614
| A. | 0.1mol•L-1的某二元弱碱的酸式盐NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A) | |
| B. | 25℃时,pH=12的氨水和pH=12的盐酸等体积混合:c(Cl-)>c(NH${\;}_{4}^{+}$)>c(H+)>c(OH-) | |
| C. | 等体积、等物质的量浓度的醋酸和氢氧化钠溶液混合:c(OH-)=c(H+)+c(CH3COOH) | |
| D. | 向NH4HSO4溶液中加入等物质的量的NaOH形成的溶液中:c(Na+)=c(SO${\;}_{4}^{2-}$)+c(NH${\;}_{4}^{+}$)+c(H+)+c(OH-) |
 运用碳及其化合物的性质,完成下列小题:
运用碳及其化合物的性质,完成下列小题: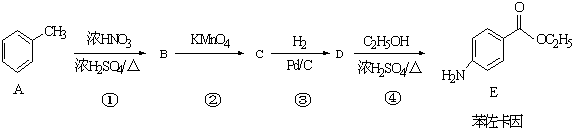
 .
.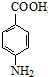 +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$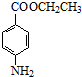 +H2O
+H2O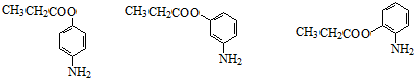 (其中一种)(任写一种)
(其中一种)(任写一种) )的合成路线图(其他原料任选).
)的合成路线图(其他原料任选).