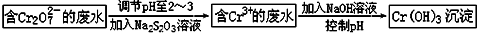2.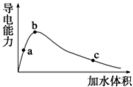 25℃时,将一定量的冰醋酸(即无水乙酸)加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )
25℃时,将一定量的冰醋酸(即无水乙酸)加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )
 25℃时,将一定量的冰醋酸(即无水乙酸)加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )
25℃时,将一定量的冰醋酸(即无水乙酸)加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )| A. | 醋酸的电离度:a<b<c | |
| B. | 溶液中c(H+):b>a>c | |
| C. | a、b、c三点的溶液都有c(H+)=c(CH3COO-)+c(OH-) | |
| D. | 从b点到c点,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$的比值减小 |
20. 以下元素均为短周期元素:
以下元素均为短周期元素:
(1)B在周期表中的位置第二周期第 VIA族,C离子的结构示意图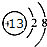 .
.
(2)D的最低价含氧酸的电子式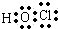 .
.
(3)M的简单气态氢化物与B的单质形成燃料电池(KOH为电解液),写出其负极反应方程式2NH3-6e-+6OH-═N2+6H2O.
(4)A在真空高压下能与由D、E组成的分子呈正四面体结构的化合物Y反应生成2种固体物质,其中一种是自然界中硬度最大的物质.该反应的化学方程式:4Na+CCl4$\frac{\underline{\;真空高压\;}}{\;}$4NaCl+C;
(5)仅由A、B、E组成的一种生活中的常用盐,其中A的质量分数为43%,其水溶液与D单质物质的量比为1:1反应的离子方程式为CO32-+Cl2+H2O=ClO-+Cl-+HCO-3.
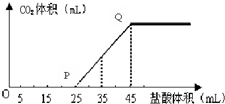
(6)A的最高价氧化物的水化物的溶液中通入一定量CO2得溶液X,X中逐滴加入1mol•L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:
①X溶液中溶质的化学式NaOH和Na2CO3.
②当加入35mL盐酸时,产生CO2的体积为224mL(标准状况).
 以下元素均为短周期元素:
以下元素均为短周期元素:| 元素代号 | 相关信息 |
| M | 非金属元素,其气态氢化物的水溶液呈碱性 |
| A | A的单质与冷水剧烈反应,得到强碱性溶液 |
| B | B的原子最外层电子数是 内层电子数的三倍 |
| C | 在第三周期中,C的简单离子半径最小 |
| D | A、B、D组成的36电子的化合物X是家用消毒剂的主要成分 |
| E | 所有有机物中都含有E元素 |
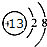 .
.(2)D的最低价含氧酸的电子式
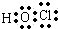 .
.(3)M的简单气态氢化物与B的单质形成燃料电池(KOH为电解液),写出其负极反应方程式2NH3-6e-+6OH-═N2+6H2O.
(4)A在真空高压下能与由D、E组成的分子呈正四面体结构的化合物Y反应生成2种固体物质,其中一种是自然界中硬度最大的物质.该反应的化学方程式:4Na+CCl4$\frac{\underline{\;真空高压\;}}{\;}$4NaCl+C;
(5)仅由A、B、E组成的一种生活中的常用盐,其中A的质量分数为43%,其水溶液与D单质物质的量比为1:1反应的离子方程式为CO32-+Cl2+H2O=ClO-+Cl-+HCO-3.
(6)A的最高价氧化物的水化物的溶液中通入一定量CO2得溶液X,X中逐滴加入1mol•L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:
①X溶液中溶质的化学式NaOH和Na2CO3.
②当加入35mL盐酸时,产生CO2的体积为224mL(标准状况).
19.镁及其化合物用途非常广泛,目前世界上60%的镁是从海水中提取.从海水中先将海水淡化获得淡水和浓海水,浓海水的主要成分如下:
再利用浓海水提镁的一段工艺流程如下图:
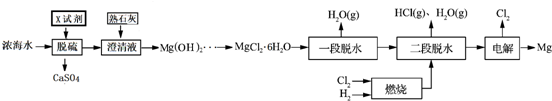
请回答下列问题
(1)浓海水主要含有的四种离子中质量浓度最小的是Mg2+.在上述流程中,可以循环使用的物质是Cl2、HCl.
(2)在该工艺过程中,X试剂的化学式为CaCl2.
(3)“一段脱水”目的是制备MgCl2•2H2O;“二段脱水”的目的是制备电解原料.若将MgCl2•6H2O直接加热脱水,则会生成Mg(OH)Cl.若电解原料中含有Mg(OH)Cl,电解时Mg(OH)Cl与阴极产生的Mg反应,使阴极表面产生MgO钝化膜,降低电解效率.生成MgO的化学方程式为2Mg(OH)Cl+Mg=MgCl2+2MgO+H2↑.
(4)若制得Mg(OH)2的过程中浓海水的利用率为80%,由Mg(OH)2至“二段脱水”制得电解原料的过程中镁元素的利用率为90%,则1m3浓海水可得“二段脱水”后的电解原料质量为84672g.
(5)以LiCl-KCl共熔盐为电解质的Mg-V2O5电池是战术导弹的常用电源,该电池的总反应为:Mg+V2O5+2LiCl═MgCl2+V2O4•Li2O 该电池的正极反应式为V2O5+2Li++2e-=V2O4•Li2O.
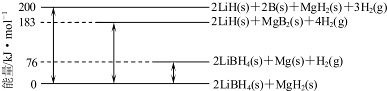
(6)Mg合金是重要的储氢材料.2LiBH4/MgH2体系放氢焓变示意图如下,则:
Mg(s)+2B(s)═MgB2(s)△H=-93 kJ•mol-1.
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g•L-1) | 63.7 | 28.8 | 144.6 | 46.4 |

请回答下列问题
(1)浓海水主要含有的四种离子中质量浓度最小的是Mg2+.在上述流程中,可以循环使用的物质是Cl2、HCl.
(2)在该工艺过程中,X试剂的化学式为CaCl2.
(3)“一段脱水”目的是制备MgCl2•2H2O;“二段脱水”的目的是制备电解原料.若将MgCl2•6H2O直接加热脱水,则会生成Mg(OH)Cl.若电解原料中含有Mg(OH)Cl,电解时Mg(OH)Cl与阴极产生的Mg反应,使阴极表面产生MgO钝化膜,降低电解效率.生成MgO的化学方程式为2Mg(OH)Cl+Mg=MgCl2+2MgO+H2↑.
(4)若制得Mg(OH)2的过程中浓海水的利用率为80%,由Mg(OH)2至“二段脱水”制得电解原料的过程中镁元素的利用率为90%,则1m3浓海水可得“二段脱水”后的电解原料质量为84672g.
(5)以LiCl-KCl共熔盐为电解质的Mg-V2O5电池是战术导弹的常用电源,该电池的总反应为:Mg+V2O5+2LiCl═MgCl2+V2O4•Li2O 该电池的正极反应式为V2O5+2Li++2e-=V2O4•Li2O.
(6)Mg合金是重要的储氢材料.2LiBH4/MgH2体系放氢焓变示意图如下,则:
Mg(s)+2B(s)═MgB2(s)△H=-93 kJ•mol-1.

18.NaCl在生产中有重要作用.
(1)某小组用NaCl进行以下实验:
①Ⅰ中白色沉淀的化学式是AgCl.
②Ⅱ中能说明沉淀变黑的离子方程式是2AgCl(s)+S2-(aq)=Ag2S(s)+2Cl-,沉淀能发生转化的主要原因是Ag2S比AgCl溶解度更小.
③经检测步骤Ⅲ中乳白色沉淀是AgCl和S的混合物.请写出黑色沉淀变为乳白色的化学方程式2Ag2S+O2+4NaCl+2H2O=4AgCl+2S+4NaOH,从化学平衡移动的角度解释在沉淀变色过程中NaCl的作用Ag2S被O2氧化生成S时释放出Ag+,NaCl中的Cl-与Ag+结合成AgCl沉淀,c(Ag+)减小,③中平衡向正反应方向移动,最终出现乳白色沉淀.
(2)电解法是治理铵盐为主要水体污染物的一种方法,原理是:在污水中加入一定量NaCl进行电解,产生的Cl2与水反应生成HClO,HClO 将NH4+氧化为N2,使水体脱氮.请写出酸性条件下HClO 与NH4+反应的离子方程式3HClO+2NH4+=N2↑+3Cl-+5H++3H2O.研究发现:污水呈弱酸性比强酸性更有利于使NH4+氧化为N2而脱氮,原因是酸性较强时,Cl2+H2O?H++Cl-+HClO 的化学平衡向逆反应方向移动,生成的HClO减少,不利脱氮.
(1)某小组用NaCl进行以下实验:
| 步 骤 | 现 象 |
| Ⅰ.将NaCl溶液与AgNO3溶液混合 | 产生白色沉淀 |
| Ⅱ.向所得固液混合物中加Na2S溶液 | 沉淀变为黑色 |
| Ⅲ.将Ⅱ中经过滤洗得到的黑色沉淀分成两份,在一份沉淀中加蒸馏水,另一份沉淀中加入NaCl溶液,同时浸泡较长时间. | 加蒸馏水的沉淀仍为黑色,加入NaCl溶液的沉淀变为乳白色 |
②Ⅱ中能说明沉淀变黑的离子方程式是2AgCl(s)+S2-(aq)=Ag2S(s)+2Cl-,沉淀能发生转化的主要原因是Ag2S比AgCl溶解度更小.
③经检测步骤Ⅲ中乳白色沉淀是AgCl和S的混合物.请写出黑色沉淀变为乳白色的化学方程式2Ag2S+O2+4NaCl+2H2O=4AgCl+2S+4NaOH,从化学平衡移动的角度解释在沉淀变色过程中NaCl的作用Ag2S被O2氧化生成S时释放出Ag+,NaCl中的Cl-与Ag+结合成AgCl沉淀,c(Ag+)减小,③中平衡向正反应方向移动,最终出现乳白色沉淀.
(2)电解法是治理铵盐为主要水体污染物的一种方法,原理是:在污水中加入一定量NaCl进行电解,产生的Cl2与水反应生成HClO,HClO 将NH4+氧化为N2,使水体脱氮.请写出酸性条件下HClO 与NH4+反应的离子方程式3HClO+2NH4+=N2↑+3Cl-+5H++3H2O.研究发现:污水呈弱酸性比强酸性更有利于使NH4+氧化为N2而脱氮,原因是酸性较强时,Cl2+H2O?H++Cl-+HClO 的化学平衡向逆反应方向移动,生成的HClO减少,不利脱氮.
17.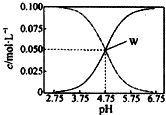 25℃时,有均满足c(CH3COO- )+c(CH3COOH)=0.10mol/L的醋酸与醋酸钠的混合溶液系列,在溶液中c(CH3COOH)、c(CH3COO- )与pH的关系如图所示.下列有关溶液中离子浓度关系的叙述中,不正确的是( )
25℃时,有均满足c(CH3COO- )+c(CH3COOH)=0.10mol/L的醋酸与醋酸钠的混合溶液系列,在溶液中c(CH3COOH)、c(CH3COO- )与pH的关系如图所示.下列有关溶液中离子浓度关系的叙述中,不正确的是( )
 25℃时,有均满足c(CH3COO- )+c(CH3COOH)=0.10mol/L的醋酸与醋酸钠的混合溶液系列,在溶液中c(CH3COOH)、c(CH3COO- )与pH的关系如图所示.下列有关溶液中离子浓度关系的叙述中,不正确的是( )
25℃时,有均满足c(CH3COO- )+c(CH3COOH)=0.10mol/L的醋酸与醋酸钠的混合溶液系列,在溶液中c(CH3COOH)、c(CH3COO- )与pH的关系如图所示.下列有关溶液中离子浓度关系的叙述中,不正确的是( )| A. | 25℃时,醋酸的电离常数K=1.0×10-4.75 | |
| B. | W点表示的溶液中:c(CH3COO-)=c(CH3COOH)>c( Na+) | |
| C. | pH=5.5的溶液中:c(CH3COOH)>c(CH3COO- )>c(H+)>c(OH- ) | |
| D. | pH=4.0的溶液中:c( Na+)+c(H+)+c(CH3COOH)-c(OH- )=0.10mol/L |
14.现拟分离乙酸乙酯、乙酸、乙醇的混合物,如图是分离操作步骤流程图.下列有关说法错误的是( )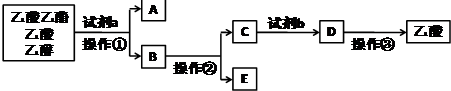
0 154090 154098 154104 154108 154114 154116 154120 154126 154128 154134 154140 154144 154146 154150 154156 154158 154164 154168 154170 154174 154176 154180 154182 154184 154185 154186 154188 154189 154190 154192 154194 154198 154200 154204 154206 154210 154216 154218 154224 154228 154230 154234 154240 154246 154248 154254 154258 154260 154266 154270 154276 154284 203614

| A. | 操作①用到的玻璃仪器主要有分液漏斗、烧杯 | |
| B. | 工业制备无水E物质的方法是在E中加生石灰后进行操作② | |
| C. | 试剂b可用硫酸 | |
| D. | 操作③用到的仪器和用品主要有漏斗、烧杯、玻璃棒、滤纸 |
 硝基还原为氨基:
硝基还原为氨基: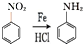
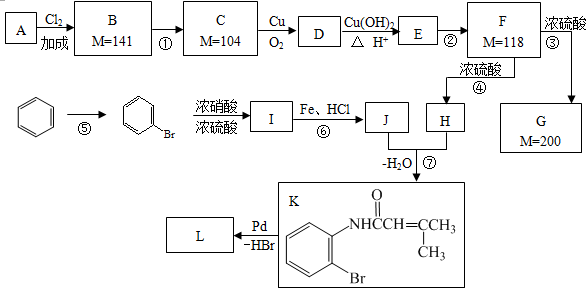
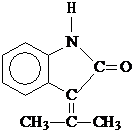 .
.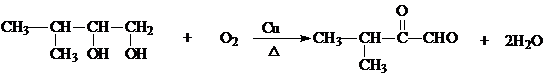 .
. .
.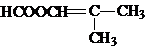 .
.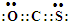 .
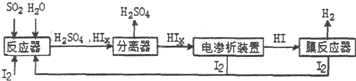
.
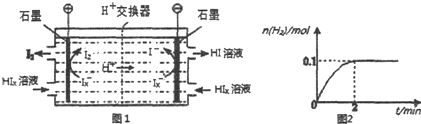
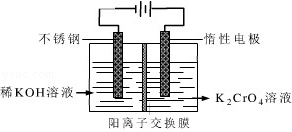 铬是人体必需的微量元素,它与脂类代谢有密切联系,但铬过量会引起污染,危害人类健康.
铬是人体必需的微量元素,它与脂类代谢有密切联系,但铬过量会引起污染,危害人类健康.