1.下列溶液中,Cl-的物质的量浓度最大的是( )
| A. | 15 mL 1 mol/L 的FeCl3溶液 | |
| B. | 9.5 g MgCl2溶于水配成100 mL 溶液 | |
| C. | 143.5 g AgCl加入到100 mL 水中 | |
| D. | 在含有1.505×1021个Al3+的50 mL的AlCl3溶液 |
20.n g CO2中有m个O原子,则阿伏加德罗常数NA的数值可表示为( )
| A. | 22m/n mol-1 | B. | m/22n mol-1 | C. | n/32m mol-1 | D. | n/32mmol-1 |
19.X元素的阳离子和Y元素的阴离子具有与氩原子相同的电子层结构,下列叙述正确的是( )
| A. | 原子序数X>Y | B. | 最外层电子数X>Y | C. | 原子半径X<Y | D. | 最高正价X>Y |
18.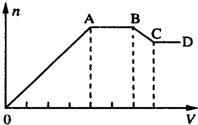 某溶液中,可能含有下表所列离子中的某几种:
某溶液中,可能含有下表所列离子中的某几种:
取少量该溶液,向其中加入某试剂X,产生沉淀的物质的量(n)与加入试剂X的体积(V)关系如图所示:
(1)若X是NaOH溶液,原溶液中一定含有的阴离子有Cl-;BC段反应的离子方程式为Al(OH)3+OH-=[Al(OH)4]-或Al(OH)3+OH-=AlO2?+H2O.
(2)若X是盐酸,则原溶液中一定含有的金属阳离子是Na+;AB段发生反应的总离子方程式为CO32-+2H+=H2O+CO2↑;OA段生成沉淀的物质的量之比为11:2.
 某溶液中,可能含有下表所列离子中的某几种:
某溶液中,可能含有下表所列离子中的某几种:| 阳离子 | Al3+、Mg2+、NH4+、Na+ |
| 阴离子 | CO32-、SiO32-、[Al(OH)4]-、Cl- |
(1)若X是NaOH溶液,原溶液中一定含有的阴离子有Cl-;BC段反应的离子方程式为Al(OH)3+OH-=[Al(OH)4]-或Al(OH)3+OH-=AlO2?+H2O.
(2)若X是盐酸,则原溶液中一定含有的金属阳离子是Na+;AB段发生反应的总离子方程式为CO32-+2H+=H2O+CO2↑;OA段生成沉淀的物质的量之比为11:2.
16.常温下,下列各组离子在制定溶液中一定能大量共存的是( )
| A. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1×1014的溶液:Ca2+、Na+、ClO-、NO3- | |
| B. | 1.0mol•L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| C. | 含有0.1mo•L-1的Ca2+溶液:Na+、K+、CO32-、Cl- | |
| D. | 澄清透明的溶液中:Na+、K+、MnO4-、AlO2- |
15.原子序数依次增大的五种短周期元素 X、Y、Z、R、T,有关信息如下表.下列说法正确的是( )
| 元素 | X | Y | Z | R | T |
| 原子半径/nm | 0.037 | 0.077 | 0.074 | 0.186 | 0.102 |
| 主要化合价 | +1 | +4、-4 | -2 | +1 | +6、-2 |
| A. | X、Y、Z 位于同一周期 | |
| B. | R 与 Z 所形成的化合物均只含离子键 | |
| C. | 氢化物的沸点:Y<Z<T | |
| D. | 第一电离能:Y<Z |
14.pH等于11的NaOH溶液和NaCN溶液中,水的电离程度大小的比较正确的是( )
| A. | 相等 | B. | 前者比后者大11倍 | ||
| C. | 后者是前者的1011倍 | D. | 后者是前者的108倍 |
13.下列有关表述正确的是( )
0 154047 154055 154061 154065 154071 154073 154077 154083 154085 154091 154097 154101 154103 154107 154113 154115 154121 154125 154127 154131 154133 154137 154139 154141 154142 154143 154145 154146 154147 154149 154151 154155 154157 154161 154163 154167 154173 154175 154181 154185 154187 154191 154197 154203 154205 154211 154215 154217 154223 154227 154233 154241 203614
| A. | 次氯酸的电子式: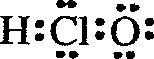 | B. | 硫原子的价电子排布式:3s23p4 | ||
| C. | 氮化硅的分子式:Si4N3 | D. | N原子的电子排布图为: |
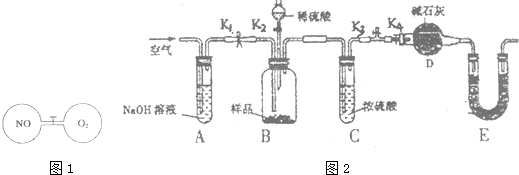
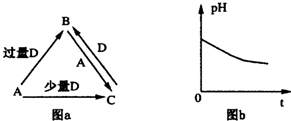
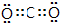 .
.