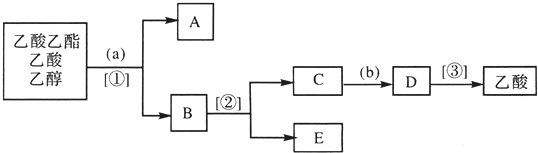
6.发生在美国的墨西哥湾原油泄漏事件极大地破坏了生态环境,该事件警示人类应合理的开发和利用能源.随着经济的飞速发展,机动车越来越多,对石油产品的需求激增,为了环保和降低成本,很多国家转型研究电动车.LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车.电池的正极材料是LiFePO4,负极材料是石墨,含U导电固体为电解质,电池反应为:FePO4+Li$?_{充电}^{放点}$LiFePO4.下列有关LiFePO4电池说法正确的是( )
| A. | 可加入烧碱溶液以提高电池的性能,碱性电池的能量和可储存时间均较高 | |
| B. | 放电时电池内部Li+向负极移动 | |
| C. | 充电过程中,电池正极材料的质量减少 | |
| D. | 放电时电池正极反应为:FePO4+Li+-e-═LiFePO4 |
5.含有2~5个碳原子的直链烷烃沸点和燃烧热的数据见下表:( )
*燃烧热:1mol物质完全燃烧,生成二氧化碳、液态水时所放出的热量.根据表中数据,下列判断错误的是( )
| 烷烃名称 | 乙烷 | 丙烷 | 丁烷 | 戊烷 |
| 沸点(℃) | -88.6 | -42.1 | -0.5 | 36.1 |
| *燃烧热(kJ•mol-1) | 1560.7 | 2219.2 | 2877.6 | 3535.6 |
| A. | 正庚烷在常温常压下肯定不是气体 | |
| B. | 直链烷烃燃烧热和其所含碳原子数呈线性关系 | |
| C. | 随碳原子数增加,直链烷烃沸点逐渐升高 | |
| D. | 随碳原子数增加,直链烷烃沸点和燃烧热都成比例增加 |
4.下列图象表达正确的是( )
| A. | 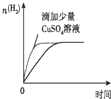 等质量锌粉与足量盐酸反应 | |
| B. | 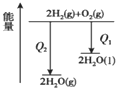 氢气与氧气反应中的能量变化 | |
| C. | 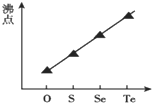 气态氢化物沸点 | |
| D. | 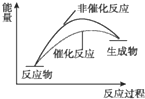 催化反应与非催化反应过程中的能量关系 |
1.下列离子方程式正确的是( )
| A. | 向AlCl3溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 将Al投入到烧碱溶液中:2Al+2OH-═AlO2-+2H2O | |
| C. | 将Al(OH)3投入到烧碱溶液中:Al(OH)3+OH-═AlO2-+2H2O | |
| D. | 向NaHCO3溶液中加入适量KOH溶液:HCO3-+OH-═CO2↑+H2O |
20.德国卡尔•肖莱马是有机化学的奠基人和杰出的有机化学理论家.他的主要贡献是对脂肪烃的系统研究并解决了烷烃的异构理论.根据下表中烃的分子式排列规律,判断空格中烃的同分异构体数目是( )
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| CH4 | C2H4 | C3H8 | C4H8 | C6H12 | C7H16 | C8H16 |
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
19.用质量均为100g的Cu作电极,电解AgNO3溶液.稍电解一段时间后,两电极的质量相差14g,此时两电极的质量分别为( )
| A. | 阳极100g,阴极128g | B. | 阳极96.8g,阴极110.8g | ||
| C. | 阳极94.8g,阴极108.8g | D. | 阳极95.9g,阴极114.0g |
18.用Cl2生产某些含氯有机物时会产生副产物HCl,利用反应4HCl+O2$?_{400℃}^{CuO/CuCl_{2}}$2Cl2+2H2O可实现氯的循环利用.已知:
Ⅰ.反应中,4 mol HCl被氧化放出115.6 kJ 的热量;
Ⅱ.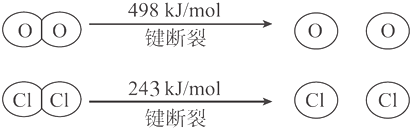
则断开1molH-O键与断开1molH-Cl键所需能量相差约为( )
0 154025 154033 154039 154043 154049 154051 154055 154061 154063 154069 154075 154079 154081 154085 154091 154093 154099 154103 154105 154109 154111 154115 154117 154119 154120 154121 154123 154124 154125 154127 154129 154133 154135 154139 154141 154145 154151 154153 154159 154163 154165 154169 154175 154181 154183 154189 154193 154195 154201 154205 154211 154219 203614
Ⅰ.反应中,4 mol HCl被氧化放出115.6 kJ 的热量;
Ⅱ.

则断开1molH-O键与断开1molH-Cl键所需能量相差约为( )
| A. | 12kJ | B. | 32kJ | C. | 115.6kJ | D. | 127.6kJ |