16.已知(CH3)2C=CH2,可表示为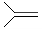 ,脱落酸(如图)可用作植物生长抑制剂,下
,脱落酸(如图)可用作植物生长抑制剂,下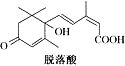 列对该物质的叙述正确的是( )
列对该物质的叙述正确的是( )
 ,脱落酸(如图)可用作植物生长抑制剂,下
,脱落酸(如图)可用作植物生长抑制剂,下 列对该物质的叙述正确的是( )
列对该物质的叙述正确的是( )| A. | 其分子式为C15H22O4 | |
| B. | 其属于芳香族化合物 | |
| C. | 能与氢氧化钠溶液反应,但不能与碳酸氢钠溶液反应 | |
| D. | 该物质在一定条件下可发生自身取代反应生成含七元环的物质. |
15.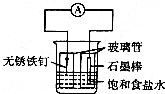 如图为铁的吸氧腐蚀实验装置,下列说法中错误的是( )
如图为铁的吸氧腐蚀实验装置,下列说法中错误的是( )
 如图为铁的吸氧腐蚀实验装置,下列说法中错误的是( )
如图为铁的吸氧腐蚀实验装置,下列说法中错误的是( )| A. | 右玻璃管内液面高于左玻璃管内液面 | |
| B. | 溶液中的Cl-向铁钉方向移动 | |
| C. | 石墨棒做正极,电极反应式为O2+2H2O+4e-═4OH- | |
| D. | 向插人铁钉的玻璃管内滴人Na0H溶液,可观察到铁钉附近的溶液中有沉淀生成 |
14.ABn型分子中,若A原子的最外层未达到稳定结构,则该分子被称为缺电子分子.下列分子属于缺电子分子的是( )
| A. | CO2 | B. | BeCl2 | C. | BF3 | D. | XeF2 |
13.在标准状况下,用干燥烧瓶收集一瓶氯化氢气体倒置于盛水的水槽时,水充满烧瓶(假设烧瓶里溶液不扩散出水槽),烧瓶里盐酸的密度为ρ g•cm-1.该盐酸物质的量浓度、溶质的质量分数分别为( )
| A. | e=$\frac{1}{11.2}$mol•L-1、ω=$\frac{36.5}{224ρ}$% | B. | e=$\frac{1}{22.4}$mol•L-1、ω=$\frac{36.5}{224ρ}$% | ||
| C. | e=$\frac{1}{22.4}$mol•L-1、ω=$\frac{36.5}{112ρ}$% | D. | e=$\frac{1}{11.2}$mol•L-1、ω=$\frac{23}{224}$% |
10.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 22.4L氯气和氢气的混合气体含有2NA个原子 | |
| B. | 0.1mol/L的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA | |
| C. | 标准状况下,22.4L乙烯和丙烯的混合气体中含有的碳原子数目为2.5NA | |
| D. | 1molFeI2与1molCl2反应转移的电子数为2NA |
9.NA为阿伏伽德罗常数的值.下列说法正确的是( )
0 153957 153965 153971 153975 153981 153983 153987 153993 153995 154001 154007 154011 154013 154017 154023 154025 154031 154035 154037 154041 154043 154047 154049 154051 154052 154053 154055 154056 154057 154059 154061 154065 154067 154071 154073 154077 154083 154085 154091 154095 154097 154101 154107 154113 154115 154121 154125 154127 154133 154137 154143 154151 203614
| A. | 2.0gH2O与D2O的混合物中所含中子数为NA | |
| B. | 标准状况下1.4 g乙烯所含共用电子对数为0.25NA | |
| C. | 3 mol单质Fe完全转变为Fe3O4,失去8 NA个电子 | |
| D. | 50ml 12 mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA |

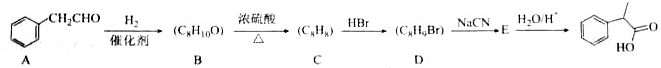
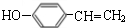 .
.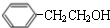 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$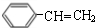 +H2O;C→D的反应类型为加成反应
+H2O;C→D的反应类型为加成反应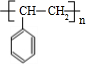 .
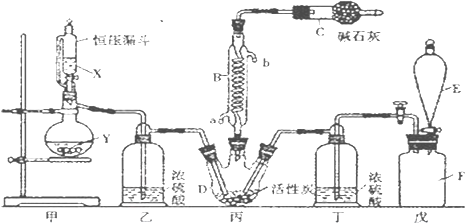
.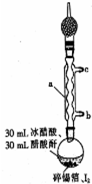 四碘化锡是一种橙红色结晶,熔点为144.5℃,沸点为364℃,不溶于冷水,溶于醇、苯、氯仿等,遇水易水解,常用作分析试剂和有机合成试剂.实验室制备四碘化锡的主要步骤如下:
四碘化锡是一种橙红色结晶,熔点为144.5℃,沸点为364℃,不溶于冷水,溶于醇、苯、氯仿等,遇水易水解,常用作分析试剂和有机合成试剂.实验室制备四碘化锡的主要步骤如下: