7.下列变化不可能通过一步反应直接完成的是( )
| A. | Al2O3→Al(OH)3 | B. | Na→Na2O2 | C. | Fe(OH)2→Fe(OH)3 | D. | Al(OH)3→AlO2- |
6.下列物质属于非电解质一组的是( )
| A. | CO2、NH3、CH4 | B. | H2SO4、HNO3、BaCl2 | ||
| C. | CO2、NH3、Cu | D. | KNO3、NaOH、HCl |
5.下列物质暴露在空气中,不容易变质的是( )
| A. | Na | B. | FeSO4 | C. | SiO2 | D. | Na2O2 |
4.FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断正确的是( )
| A. | 加入KSCN溶液不一定变红色 | B. | 溶液中一定含Fe2+ | ||
| C. | 溶液中一定含Cu2+ | D. | 剩余固体中一定含Cu和Fe |
3.下列化学方程式中能用H++OH-═H2O表示的是( )
| A. | NH3•H2O+HCl═NH4Cl+H2O | B. | Ba(OH)2+H2SO4═BaSO4↓+2H2O | ||
| C. | Al(OH)3+3HCl═AlCl3+3H2O | D. | KOH+HNO3═KNO3+H2O |
2.下列叙述不正确的是( )
| A. | NH3易液化,液氨常用作制冷剂 | |
| B. | 与金属反应时,稀HNO3可能被还原为更低价态,则稀HNO3氧化性强于浓HNO3 | |
| C. | 二氧化硅是生产光导纤维的重要原料 | |
| D. | 稀HNO3和活泼金属反应时不能得到氢气 |
1.将足量的两份铝,分别加入到等物质的量的盐酸和氢氧化钠溶液中,放出气体的物质的量之比为( )
| A. | 3:2 | B. | 2:3 | C. | 1:1 | D. | 1:3 |
18.X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
(1)Y的轨道表示式为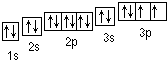 ;
;
(2)X、Y、Z三种元素的原子半径从大到小的顺序是S>Cl>C(用元素符号表示);
(3)XY2的分子中存在2个σ键,分子的空间构形为直线形,在H-Y、H-Z两种共价键中,键长较长的是H-S;
(4)W3+的核外电子排布式是1s22s22p63s23p63d5;
(5)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y.此反应的化学方程式是2CO+SO2=S+2CO2;
(6)请设计一个实验方案,比较Y、Z单质氧化性的强弱在Na2S溶液中滴加Cl2水,若溶液出现浑浊,说明Cl2的氧化性比S强.
0 153956 153964 153970 153974 153980 153982 153986 153992 153994 154000 154006 154010 154012 154016 154022 154024 154030 154034 154036 154040 154042 154046 154048 154050 154051 154052 154054 154055 154056 154058 154060 154064 154066 154070 154072 154076 154082 154084 154090 154094 154096 154100 154106 154112 154114 154120 154124 154126 154132 154136 154142 154150 203614
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为56,中子数为30 |
 ;
;(2)X、Y、Z三种元素的原子半径从大到小的顺序是S>Cl>C(用元素符号表示);
(3)XY2的分子中存在2个σ键,分子的空间构形为直线形,在H-Y、H-Z两种共价键中,键长较长的是H-S;
(4)W3+的核外电子排布式是1s22s22p63s23p63d5;
(5)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y.此反应的化学方程式是2CO+SO2=S+2CO2;
(6)请设计一个实验方案,比较Y、Z单质氧化性的强弱在Na2S溶液中滴加Cl2水,若溶液出现浑浊,说明Cl2的氧化性比S强.