16.下列离子方程式正确的是( )
| A. | 硫酸镁溶液加氨水:Mg2++2NH3•H2O═Mg(OH)2↓+2NH4+ | |
| B. | 碳酸氢铵溶液加足量氢氧化钠并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$H2O+NH3↑ | |
| C. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| D. | 氧化亚铁溶于稀硝酸:FeO+2H+═Fe2++H2O |
15.实验室为了使用方便,通常将氯气溶解于水中形成氯水或将其降温加压形成液氯来使用.下列有关这两种液体的实验描述都正确的是( )
| A. | 两种液体都可以使干燥的布条褪色 | |
| B. | 两种液体都可以使干燥的蓝色石蕊试纸变红 | |
| C. | 用这两种液体都可给自来水消毒 | |
| D. | 分别向这两种液体中投人几颗金属锌粒均有气泡产生 |
14.下列实验操作不正确的是( )
| A. | 过滤时如果发现滤液是浑浊的,则滤液还要进行过滤 | |
| B. | 在进行蒸馏时,要加少量碎瓷片,防止液体暴沸 | |
| C. | 在进行分液操作时,分液漏斗内外气体相通,眼睛要注视烧杯中的溶液 | |
| D. | 在进行蒸馏时,温度计不要插入溶液中 |
13.在密闭容器中下列可逆反应达到平衡,增大压强和升高温度都能使平衡向正反应方向移动的是( )
| A. | N2(气体)+O2(气体)?2NO(气体) 正反应吸热 | |
| B. | NH4HCO3(固体)?NH3(气体)+H2O(气体)+CO2(气体) 正反应吸热 | |
| C. | 3O2(气体)?2O3(气体) 正反应吸热 | |
| D. | 2NO2(气体)?N2O4(气体) 正反应放热 |
9.电石制取乙炔产生大量废渣:电石渣(主要成分为Ca(OH)2,另外还含有Fe和Al化学物及SO2等杂质),可用下面工艺实现电石渣吸收氯碱工业废气中的氯气,综合治理废渣和废气,回答下列问题:
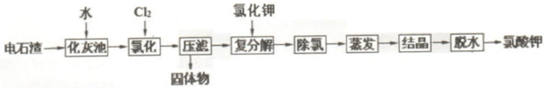
已知:①几种物质溶解度与温度的关系
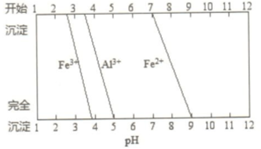
②几种离子开始和完全沉淀与pH的关系图
(1)某导电塑料是以乙炔为单体加聚合成,其化学为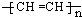 .
.
(2)化灰池中为加快水浸的速度,常采取的措施搅拌、加热.
(3)为除去Fe/Al 等杂质,氯化过程中需要控制溶液 pH为6-7.
(4)氯化过程的温度控制在 75~80℃,该过程主要反应的离子方程式为6Cl2+6Ca(OH)2=6Ca2++10Cl-+2ClO3-. 温度过低会发生副反应,产生的副产物为Ca(ClO)2(写化学式).
(5)复分解反应中,常控制温度为 20℃,加入KCl 发生的反应的方程式Ca(ClO3)2+2KCl=CaCl2+2KClO3+6H2O.
(6)通常用石墨电极电解 KClO 溶液制备 KClO3,则阳极的电极反应方程式为ClO--4e-+2H2O=ClO3-+4H+.
脱水过程实现固液分离,工业常用的设备是C
A.蒸馏塔 B.反应釜 C.离心机 D.交换器
(7)现代工艺氯化时通入O2做氧化剂提高效率,其氯化的化学方程式为2Ca(OH)2+2Cl2+5O2=2Ca(ClO3)2+2H2O.

已知:①几种物质溶解度与温度的关系
| 温度/ | 0 | 10 | 20 | 30 | 40 |
| S(CaCl2)/g | 59.5 | 64.7 | 74.5 | 100 | 128 |
| S[Ca(ClO3)2]/g | 209 | ||||
| S(KClO3)/g | 3.3 | 5.2 | 7.3 | 10.2 | 13.9 |

(1)某导电塑料是以乙炔为单体加聚合成,其化学为
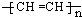 .
.(2)化灰池中为加快水浸的速度,常采取的措施搅拌、加热.
(3)为除去Fe/Al 等杂质,氯化过程中需要控制溶液 pH为6-7.
(4)氯化过程的温度控制在 75~80℃,该过程主要反应的离子方程式为6Cl2+6Ca(OH)2=6Ca2++10Cl-+2ClO3-. 温度过低会发生副反应,产生的副产物为Ca(ClO)2(写化学式).
(5)复分解反应中,常控制温度为 20℃,加入KCl 发生的反应的方程式Ca(ClO3)2+2KCl=CaCl2+2KClO3+6H2O.
(6)通常用石墨电极电解 KClO 溶液制备 KClO3,则阳极的电极反应方程式为ClO--4e-+2H2O=ClO3-+4H+.
脱水过程实现固液分离,工业常用的设备是C
A.蒸馏塔 B.反应釜 C.离心机 D.交换器
(7)现代工艺氯化时通入O2做氧化剂提高效率,其氯化的化学方程式为2Ca(OH)2+2Cl2+5O2=2Ca(ClO3)2+2H2O.
8. Cu2O为暗红色固体,有毒,它是一种用途广泛的材料. Y已知:①Cu2O溶于硫酸,立即发生反应:Cu2O+2H+=Cu2++Cu+H2O ②部分难溶物的颜色和常温下的Ksp如下表所示:
Cu2O为暗红色固体,有毒,它是一种用途广泛的材料. Y已知:①Cu2O溶于硫酸,立即发生反应:Cu2O+2H+=Cu2++Cu+H2O ②部分难溶物的颜色和常温下的Ksp如下表所示:
(Ⅰ) 某同学利用乙醛与新制氢氧化铜加热制的砖红色沉淀.
①乙醛与新制氢氧化铜反应生成砖红色沉淀的化学方程式为2Cu(OH)2+NaOH+CH3CHO$\frac{\underline{\;\;△\;\;}}{\;}$Cu2O↓+CH3COONa+3H2O.
②砖红色沉淀加入稀硫酸,现象为溶液由无色变为蓝色,有红色不溶物.
③砖红色沉淀加入浓盐酸,完全溶解得到无色溶液;若改加稀盐酸,则得到白色沉淀,其离子方程式为Cu2O+2H++2Clˉ=2CuCl↓+H2O.
(Ⅱ) Cu2O常用电解法制备,流程如下:
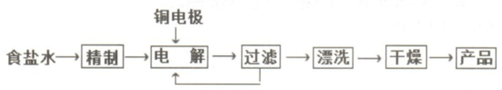
(1)精制食盐水需要除去其中的钙镁离子,依次加入的试剂为NaOH、Na2CO3、HCl.
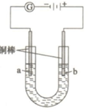
(2)实验室模拟电解装置如图,观察的现象如下所示:
①开始无明显现象,随后液面以下的铜棒表面逐渐变暗;
②5min后,b极附近开始出现白色沉淀,并逐渐增多,且向a极扩散;
③10min后,最靠近a极的白色沉淀开始变成红色;
④12min后,b极附近的白色沉淀开始变成黄色,然后逐渐变成橙黄色;
⑤a极一直有大量气泡产生;
⑥停止电解,将U形管中悬浊液静置一段时间后,上层溶液呈无色,没有出现蓝色,下层沉淀全部显砖红色.
则:ⅰ)电解池的阳极反应式为Cu+Cl--e-=CuCl↓.ⅱ)b极附近的白色沉淀开始变成黄色,颜色变化的离子方程式为CuCl+OH-=CuOH+Cl-.
此时溶液中c(OH-)/c(Cl-)=8.3×10-9.
(3)Cu2O在潮湿空气中容易被氧气氧化为CuO而变质,请设计实验方案检验其是否变质:加入足量浓盐酸,溶液变为绿色,则含有CuO.
 Cu2O为暗红色固体,有毒,它是一种用途广泛的材料. Y已知:①Cu2O溶于硫酸,立即发生反应:Cu2O+2H+=Cu2++Cu+H2O ②部分难溶物的颜色和常温下的Ksp如下表所示:
Cu2O为暗红色固体,有毒,它是一种用途广泛的材料. Y已知:①Cu2O溶于硫酸,立即发生反应:Cu2O+2H+=Cu2++Cu+H2O ②部分难溶物的颜色和常温下的Ksp如下表所示:| Cu(OH)2 | CuOH | CuCl | Cu2O | |
| 颜色 | 蓝色 | 黄色 | 白色 | 砖红色 |
| Ksp(25) | 1.6×10-19 | 1.0×10-14 | 1.2×10-6 |
①乙醛与新制氢氧化铜反应生成砖红色沉淀的化学方程式为2Cu(OH)2+NaOH+CH3CHO$\frac{\underline{\;\;△\;\;}}{\;}$Cu2O↓+CH3COONa+3H2O.
②砖红色沉淀加入稀硫酸,现象为溶液由无色变为蓝色,有红色不溶物.
③砖红色沉淀加入浓盐酸,完全溶解得到无色溶液;若改加稀盐酸,则得到白色沉淀,其离子方程式为Cu2O+2H++2Clˉ=2CuCl↓+H2O.
(Ⅱ) Cu2O常用电解法制备,流程如下:

(1)精制食盐水需要除去其中的钙镁离子,依次加入的试剂为NaOH、Na2CO3、HCl.
(2)实验室模拟电解装置如图,观察的现象如下所示:
①开始无明显现象,随后液面以下的铜棒表面逐渐变暗;
②5min后,b极附近开始出现白色沉淀,并逐渐增多,且向a极扩散;
③10min后,最靠近a极的白色沉淀开始变成红色;
④12min后,b极附近的白色沉淀开始变成黄色,然后逐渐变成橙黄色;
⑤a极一直有大量气泡产生;
⑥停止电解,将U形管中悬浊液静置一段时间后,上层溶液呈无色,没有出现蓝色,下层沉淀全部显砖红色.
则:ⅰ)电解池的阳极反应式为Cu+Cl--e-=CuCl↓.ⅱ)b极附近的白色沉淀开始变成黄色,颜色变化的离子方程式为CuCl+OH-=CuOH+Cl-.
此时溶液中c(OH-)/c(Cl-)=8.3×10-9.
(3)Cu2O在潮湿空气中容易被氧气氧化为CuO而变质,请设计实验方案检验其是否变质:加入足量浓盐酸,溶液变为绿色,则含有CuO.
7.X、Y、Z为短周期主族元素,X的最外层电子数为内层电子数的2倍,Y的最高化合价与最低化合价的代数和为4,Z与Y同周期,Z的原子半径小于Y.下列叙述不正确的是( )
0 153932 153940 153946 153950 153956 153958 153962 153968 153970 153976 153982 153986 153988 153992 153998 154000 154006 154010 154012 154016 154018 154022 154024 154026 154027 154028 154030 154031 154032 154034 154036 154040 154042 154046 154048 154052 154058 154060 154066 154070 154072 154076 154082 154088 154090 154096 154100 154102 154108 154112 154118 154126 203614
| A. | Z的氢化物是同主族简单氢化物中沸点最低的一种 | |
| B. | 非金属性:Z>Y>X | |
| C. | XY2中各原子最外层均满足8电子结构 | |
| D. | X、Y、Z的氢化物中化学键均为极性共价键 |
 胆矾晶体(CuSO4•5H2O)中4个水分子与铜离子形成配位键,另一个水分子只以氢键与相邻微粒结合.某兴趣小组称取2.500g胆矾晶体,逐渐升温使其失水,并准确测定不同温度下剩余固体的质量,得到如右图所示的实验结果示意图.以下说法正确的是CD(填标号).
胆矾晶体(CuSO4•5H2O)中4个水分子与铜离子形成配位键,另一个水分子只以氢键与相邻微粒结合.某兴趣小组称取2.500g胆矾晶体,逐渐升温使其失水,并准确测定不同温度下剩余固体的质量,得到如右图所示的实验结果示意图.以下说法正确的是CD(填标号).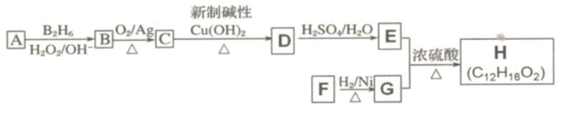
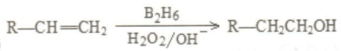
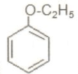 是同分异构体
是同分异构体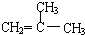 .
.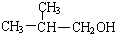 +O2$→_{△}^{Ag}$2
+O2$→_{△}^{Ag}$2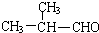 +2H2O.
+2H2O.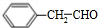 ;F分子中最多有15个原子共面.
;F分子中最多有15个原子共面.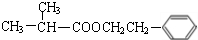 +NaOH$\stackrel{△}{→}$
+NaOH$\stackrel{△}{→}$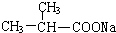 +
+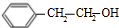 .
.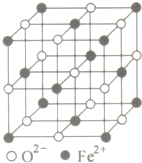 有些食物中铁元素含量非常丰富,其中非血红素铁是其存在的形式之一,主要是三价铁与蛋白质和羧酸结合成络合物.
有些食物中铁元素含量非常丰富,其中非血红素铁是其存在的形式之一,主要是三价铁与蛋白质和羧酸结合成络合物.