2.现有20gD2O和36gH2O,下列说法不正确的是( )
| A. | 它们的分子数之比为1:2 | |
| B. | 它们的中子数之比为5:8 | |
| C. | 它们的电子数之比为1:2 | |
| D. | 分别与1mol钠反应,生成气体的质量比为1:1 |
1.可以用AG来表示溶液的酸度.AG与pH的关系如图:则下列说法正确的是( )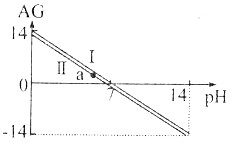

| A. | AG与pH的关系一定是AG=14-2pH | |
| B. | 直线Ⅰ和Ⅱ是因溶液的温度不同引起的,且T(Ⅰ)>T(Ⅱ) | |
| C. | AG=0时,溶液一定呈中性 | |
| D. | a点的溶液中可以有大量Na+、Cl-、Fe3+存在 |
19.下列叙述正确的是( )
| A. | 0.5mol•L-1CuCl2溶液含有3.01×1023个Cu2+ | |
| B. | 28g聚乙烯分子含有的碳原子数为 NA | |
| C. | 0.2mol PCl5分子中,键数目为NA | |
| D. | 标准状况下,3.36L H2O含有9.03×1023个H2O分子 |
17.25℃,两种酸的电离平衡常数如下表.
实验室常用饱和NaHCO3溶液除去CO2中少量的SO2,请写出SO2和NaHCO3溶液反应的主要离子方程式SO2+HCO3-=HSO3-+CO2.
0 153888 153896 153902 153906 153912 153914 153918 153924 153926 153932 153938 153942 153944 153948 153954 153956 153962 153966 153968 153972 153974 153978 153980 153982 153983 153984 153986 153987 153988 153990 153992 153996 153998 154002 154004 154008 154014 154016 154022 154026 154028 154032 154038 154044 154046 154052 154056 154058 154064 154068 154074 154082 203614
| Ka1 | Ka2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
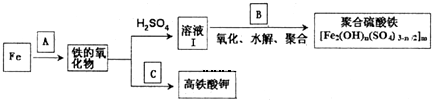
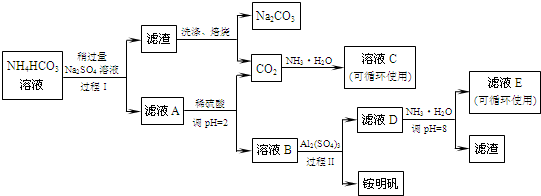
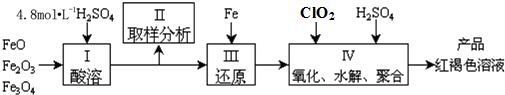
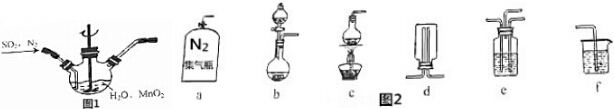
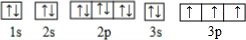 .
.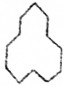 名称是环十二烷;1mol该烃完全燃烧需消耗的氧气18mol.
名称是环十二烷;1mol该烃完全燃烧需消耗的氧气18mol.