16.下列性质中,不能说明乙酸是弱电解质的是( )
①醋酸钠溶液的pH 大于7
②常温时,0.1mol/L乙酸溶液的pH约为3
③乙酸能和碳酸钙反应放出CO2
④10mL 1mol/L乙酸溶液与10mL 1mol/L的NaOH溶液恰好完全反应
⑤同pH的盐酸和乙酸分别与足量铁片反应,乙酸产生H2多
⑥pH=1的醋酸溶液用水稀释1000倍后,pH<4.
①醋酸钠溶液的pH 大于7
②常温时,0.1mol/L乙酸溶液的pH约为3
③乙酸能和碳酸钙反应放出CO2
④10mL 1mol/L乙酸溶液与10mL 1mol/L的NaOH溶液恰好完全反应
⑤同pH的盐酸和乙酸分别与足量铁片反应,乙酸产生H2多
⑥pH=1的醋酸溶液用水稀释1000倍后,pH<4.
| A. | ①②③ | B. | ④⑤⑥ | C. | ②③④ | D. | ③④⑤ |
15.下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A. | 0.1 mol/L NH4Cl溶液:c(NH4+ )=c(Cl-) | |
| B. | 0.1 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) | |
| C. | 向醋酸钠溶液中加入等量醋酸,得到的酸性混合溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 等物质的量浓度的①NH4Cl溶液 ②(NH4)2SO4溶液 ③NH4HSO4溶液④(NH4)2 CO3 溶液中NH4+浓度的大小关系是②>④>①>③ |
14.下列有关实验说法正确的是( )
| A. | AlCl3溶液和Al2(SO4)3溶液分别加热蒸发,所得固体的成分相同 | |
| B. | 配制FeCl3溶液时,将FeCl3固体溶解在盐酸中,然后再用水稀释到所需的浓度 | |
| C. | 中和热测定时,用铜制搅拌器代替玻璃环形搅拌器,测定的实验结果不变 | |
| D. | 室温时将Na2CO3溶液加水稀释后,再恢复至室温,pH和KW均减小 |
13.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | 使pH试纸显深红色的溶液:NH4+、Mg2+、Cl-、NO3- | |
| B. | 由水电离的c(H+)=1×10-14 mol•L-1的溶液中:Ca2+、K+、HCO3-、SO42- | |
| C. | c(Fe3+)=0.1 mol•L-1的溶液中:K+、ClO-、SO42-、SCN- | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:NH4+、Fe2+、NO3-、AlO2- |
12.化学工业在经济发展中的作用举足轻重,下列有关工业生产的叙述中,正确的是( )
| A. | 硫酸生产中常采用高压条件提高SO2的转化率 | |
| B. | 合成氨中采用及时分离氨气提高反应速率 | |
| C. | 电解精炼铜时,溶液中c(Cu2+)会略有减小 | |
| D. | 氯碱工业电解饱和食盐水时,阳极得到氢氧化钠和氢气 |
11.下列关于电解质溶液的叙述正确的是( )
| A. | 60℃时,NaCl溶液的pH<7,则溶液呈酸性 | |
| B. | pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 | |
| D. | 相同温度下,1 mol•L-1氨水与0.5 mol•L-1氨水中c(OH-)之比是2:1 |
10.下列与化学反应能量变化相关的叙述正确的是( )
| A. | 放热反应在任何条件都能自发进行 | |
| B. | 化学反应的热效应数值与参加反应的物质多少有关 | |
| C. | 任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同 | |
| D. | 焓变是指1 mol物质参加反应时的能量变化 |
9.亚硫酸钠是食品加工中广泛使用的漂白剂、防腐剂和抗氧化剂,其在食品中的残留量通常以二氧化硫含量计算.
(1)亚硫酸盐具有一定的毒性,长期摄入过量的亚硫酸盐,红细胞和血红蛋白会减少,钙的吸收也会减少,原因是SO32-与Fe2+、Ca2+结合,形成沉淀.
检验某黑木耳中是否含有亚硫酸盐的简单方法是:将黑木耳样品剪成碎末放入烧杯,加入20mL水和10mL盐酸,加热一会儿,滴入试剂A,观察现象既可.
(2)加热的作用是加快亚硫酸钠的溶解,加热时间不能太长的原因是防止亚硫酸受热分解成二氧化硫逸出.
(3)试剂A是品红溶液.
在足量的亚硫酸钠溶液中加入1~2滴液溴,振荡后溶液变为无色.
(4)写出以上反应的离子方程式3SO32-+Br2+H2O=2HSO3-+SO42-+2Br-.
(5)以上反应后的溶液中含有SO32-、HSO3-、SO42-、Br-、OH-等阴离子.设计实验检验SO42-和Br-,写出实验方法.试剂不限.
(1)亚硫酸盐具有一定的毒性,长期摄入过量的亚硫酸盐,红细胞和血红蛋白会减少,钙的吸收也会减少,原因是SO32-与Fe2+、Ca2+结合,形成沉淀.
检验某黑木耳中是否含有亚硫酸盐的简单方法是:将黑木耳样品剪成碎末放入烧杯,加入20mL水和10mL盐酸,加热一会儿,滴入试剂A,观察现象既可.
(2)加热的作用是加快亚硫酸钠的溶解,加热时间不能太长的原因是防止亚硫酸受热分解成二氧化硫逸出.
(3)试剂A是品红溶液.
在足量的亚硫酸钠溶液中加入1~2滴液溴,振荡后溶液变为无色.
(4)写出以上反应的离子方程式3SO32-+Br2+H2O=2HSO3-+SO42-+2Br-.
(5)以上反应后的溶液中含有SO32-、HSO3-、SO42-、Br-、OH-等阴离子.设计实验检验SO42-和Br-,写出实验方法.试剂不限.
| 实验操作 | 预期现象与结论 |
| 步骤1: | 有白色沉淀生成,证明待测液中含SO42- |
| 步骤2: | 溶液呈橙黄色,证明待测液中含Br- |
7.下列叙述正确的是( )
0 153877 153885 153891 153895 153901 153903 153907 153913 153915 153921 153927 153931 153933 153937 153943 153945 153951 153955 153957 153961 153963 153967 153969 153971 153972 153973 153975 153976 153977 153979 153981 153985 153987 153991 153993 153997 154003 154005 154011 154015 154017 154021 154027 154033 154035 154041 154045 154047 154053 154057 154063 154071 203614
| A. | 0.1mol/L醋酸溶液中:c(H+)=c(CH3COO- )+c(OH- ) | |
| B. | 中和pH与体积都相同的硫酸和醋酸,消耗NaOH的量后者大于前者 | |
| C. | 由水电离的H+浓度为1.0×10-4mol/L的溶液,pH一定等于4 | |
| D. | NaHCO3溶液中:c(Na+)>c(HCO3-)>c(H2CO3)>c(OH-)>c(H+) |
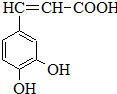 咖啡酸(如图),存在于许多中药中,如野胡萝卜、光叶水苏、荞麦、木半夏等.咖啡酸有止血作用,特别对内脏的止血效果较好.
咖啡酸(如图),存在于许多中药中,如野胡萝卜、光叶水苏、荞麦、木半夏等.咖啡酸有止血作用,特别对内脏的止血效果较好.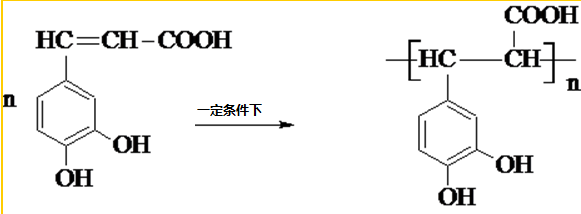 .
.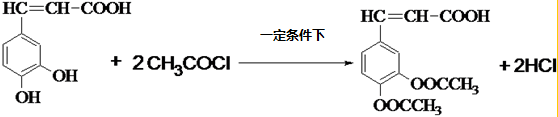 .
.