5.在相同温度时,100mL 0.01mol•L-1的醋酸溶液与10mL 0.1mol•L-1的醋酸溶液相比较,下列数据中,前者大于后者的是( )
①H+的物质的量 ②电离程度 ③中和时所需氢氧化钠溶液的量 ④醋酸的物质的量.
①H+的物质的量 ②电离程度 ③中和时所需氢氧化钠溶液的量 ④醋酸的物质的量.
| A. | ①② | B. | ②③ | C. | ①④ | D. | ②④ |
4.向含2mol NaOH、1mol Ba(OH)2、2mol NaAlO2的混合溶液中慢慢通入CO2,则通入CO2的量和生成沉淀的量的关系正确的是( )
| 选项 | A | B | C | D |
| n(CO2)(mol) | 2 | 3 | 4 | 6 |
| n(沉淀)(mol) | 2 | 2 | 3 | 3 |
| A. | A | B. | B | C. | C | D. | D |
3.下列物质中属于弱电解质的是( )
| A. | 氨水 | B. | 盐酸 | C. | 碳酸氢钠 | D. | 冰醋酸 |
2.已知0.1mo1•L-1的醋酸溶液中存在电离平衡:CH3COOH?CH3COO-+H+要使溶液中c(H+)/c(CH3COOH)比值增大,可以采取的措施是
①加少量CH3COONH4固体②加少量H2SO4③加少量冰醋酸④加少量NaOH固体⑤升高温度⑥降低温度( )
①加少量CH3COONH4固体②加少量H2SO4③加少量冰醋酸④加少量NaOH固体⑤升高温度⑥降低温度( )
| A. | ②⑤ | B. | ①③⑥ | C. | ②③⑤ | D. | ①③ |
20.化合物HIn在水溶液中因存在以下电离平衡,故可用作酸碱指示剂: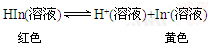
浓度为0.02mol/L的下列各溶液:①盐酸②石灰水③NaCl溶液④氨水⑤NaHCO3溶液⑥NaHSO4溶液 其中能使指示剂显红色的是( )
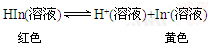
浓度为0.02mol/L的下列各溶液:①盐酸②石灰水③NaCl溶液④氨水⑤NaHCO3溶液⑥NaHSO4溶液 其中能使指示剂显红色的是( )
| A. | ①④⑤ | B. | ②⑤⑥ | C. | ③④ | D. | ①⑥ |
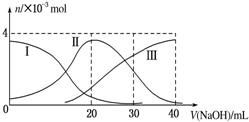
17.如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根据图示判断,下列说法正确的是( )
0 153864 153872 153878 153882 153888 153890 153894 153900 153902 153908 153914 153918 153920 153924 153930 153932 153938 153942 153944 153948 153950 153954 153956 153958 153959 153960 153962 153963 153964 153966 153968 153972 153974 153978 153980 153984 153990 153992 153998 154002 154004 154008 154014 154020 154022 154028 154032 154034 154040 154044 154050 154058 203614

| A. | H2A在水中的电离方程式是:H2A═H++HA-;HA-?H++A2- | |
| B. | 当V(NaOH)=20mL时,溶液中各离子浓度的大小顺序为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| C. | 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大 | |
| D. | 当V(NaOH)=30mL时,溶液中存在以下关系:2c(H+)+c(HA-)+2c(H2A)=c(A2-)+2c(OH-) |