12.在一定温度下,Na2CO3溶液中存在水解平衡:CO32-+H2O?HCO3-+OH-.下列说法中,正确的是( )
| A. | n(Na+)+n(H+)=n(HCO3-)+n(CO32-)+n(OH-) | |
| B. | 通入CO2,平衡向正反应方向移动 | |
| C. | 加入少量的NaOH固体,平衡向逆反应方向移动,溶液pH减小 | |
| D. | 稀释溶液,Na2CO3水解程度增大,水解平衡常数增大 |
11.常温下,关于0.1mol/L的Na2S溶液,下列叙述正确的是( )
| A. | 加入少量的NaOH固体,Na2S溶液中的c(Na+)、c(S2-)均增大 | |
| B. | Na2S溶液中存在着:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| C. | Na2S溶液中离子浓度关系为:c(Na+)>c(OH-)>c(S2-)>c(H+) | |
| D. | Na2S溶液中存在着:2c(Na+)=c(S2-)+c(HS-)+c(H2S) |
10.常温下,向20.00mL 0.100 0mol•L-1 的CH3COONa溶液中逐滴加入0.100 0mol•L-1盐酸,溶液的pH与所加盐酸体积的关系如图所示(不考虑挥发),下列说法正确的是( )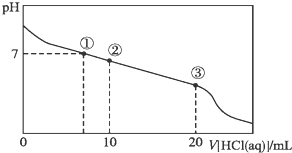

| A. | 点①所示溶液中,溶质为未反应完的CH3COONa、生成的CH3COOH和NaCl,微粒之间的关系为:c(CH3COOH)>c(Cl-)>c(OH-)=c(H+) | |
| B. | 点②所示溶液中,醋酸钠有一半与盐酸反应,微粒之间的关系为:c(Na+)>c(Cl-)>c(CH3COO-)>c(CH3COOH) | |
| C. | 点③所示溶液中,醋酸钠与盐酸恰好完全反应,微粒之间的关系为:c(Na+)>c(CH3COOH)>c(H+)>c(CH3COO-) | |
| D. | 整个过程中有可能出现:c(H+)+c(Na+)=c(CH3COOH)+c(CH3COO-) |
9.下列水解离子方程式表达正确的是( )
| A. | NaClO溶液:ClO-+H2O═HClO+OH- | B. | FeCl3溶液:Fe3++3H2O?Fe(OH)3↓+3H+ | ||
| C. | Na2S溶液:S2-+H2O?H2S+2OH- | D. | NH4Cl溶液:NH4++H2O?NH3•H2O+H+ |
8.某二元酸(H2A)在水中的电离方程式为H2A═H++HA-,HA-?H++A2-(Ka2=1.0×10-2),下列说法错误的是( )
| A. | 将同浓度的NaHA和Na2A溶液等体积混合,所得溶液的pH一定小于7 | |
| B. | 0.1 mol•L-1的NaHA溶液中离子浓度为:c(Na+))>c(HA-)>c(H+>c(A2-)>c(OH-) | |
| C. | 在0.1 mol•L-1的H2A溶液中,c(H+)>0.12 mol•L-1 | |
| D. | 在0.1 mol•L-1的Na2A溶液中,c(A2-)+c(HA-)+c(Na+)=0.3mol•L-1 |
7.T℃时,体积相等的甲、乙、丙、丁4个密闭容器中,发生反应:CO2(g)+H2(g)?CO(g)+H2O(g),起始时充入各物质的物质的量如下表所示:
则达到平衡时,CO的物质的量由大到小的顺序是( )
| CO2(g) | H2(g) | CO(g) | H2O(g) | |
| 甲 | a mol | a mol | 0 | 0 |
| 乙 | a mol | 2a mol | 0 | 0 |
| 丙 | a mol | a mol | 0 | a mol |
| 丁 | amol | amol | amol | amol |
| A. | n(丁)>n(甲)>n(乙)>n(丙) | B. | n(丁)>n(甲)>n(丙)>n(乙) | C. | n(丁)>n(乙)>n(丙)>n(甲) | D. | n(丁)>n(乙)>n(甲)>n(丙) |
6. 氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.
氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.
(1)COCl2 的空间构型为平面三角形;溴的基态原子价电子排布式为4s24p5.
(2)已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列A式发生(填字母代号,下同).
A.CsICl2═CsCl+ICl B.CsICl2═CsI+Cl2?
(3)根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是碘(或I).
(4)下列分子既不存在“s-p”σ 键,也不存在“p-p”π 键的是D.
A.HCl B.HF C.SO2 D.SCl2
(5)已知ClO2-为三角形,中心氯原子周围有四对价层电子.ClO3- 中心氯原子的杂化轨道类型为sp3杂化,写出一个与CN-互为等电子体的物质的分子式N2或CO.
(6)钙在氧气中燃烧时得到一种钙的氧化物晶体,其结构如图所示,由此可判断钙的氧化物的化学式为CaO2.已知该氧化物的密度是ρ g/cm3,则晶胞内离得最近的两个钙离子的间距为$\frac{\sqrt{2}}{2}×\root{3}{\frac{72×4}{ρ{N}_{A}}}$cm(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA).
 氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.
氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.(1)COCl2 的空间构型为平面三角形;溴的基态原子价电子排布式为4s24p5.
(2)已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列A式发生(填字母代号,下同).
A.CsICl2═CsCl+ICl B.CsICl2═CsI+Cl2?
(3)根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是碘(或I).
| 氟 | 氯 | 溴 | 碘 | |
(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
A.HCl B.HF C.SO2 D.SCl2
(5)已知ClO2-为三角形,中心氯原子周围有四对价层电子.ClO3- 中心氯原子的杂化轨道类型为sp3杂化,写出一个与CN-互为等电子体的物质的分子式N2或CO.
(6)钙在氧气中燃烧时得到一种钙的氧化物晶体,其结构如图所示,由此可判断钙的氧化物的化学式为CaO2.已知该氧化物的密度是ρ g/cm3,则晶胞内离得最近的两个钙离子的间距为$\frac{\sqrt{2}}{2}×\root{3}{\frac{72×4}{ρ{N}_{A}}}$cm(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA).
4.[实验化学]乙酰苯胺为无色晶体,有“退热冰”之称.其制备原理为:
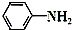 +CH3COOH$\stackrel{△}{→}$
+CH3COOH$\stackrel{△}{→}$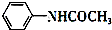 +H2O
+H2O
已知:①苯胺易被氧化; ②苯胺、醋酸和乙酰苯胺的部分物理性质如表:
制备乙酰苯胺的实验步骤如下:
步骤1:在下图1装置的圆底烧瓶中,加入6.0mL苯胺、9.0mL冰醋酸及0.2g锌粉.
步骤2:控制温度计示数约105℃,小火加热回流1h.
步骤3:趁热将反应混合物倒入盛有100mL冷水的烧杯中,抽滤,洗涤,得到粗产品.
步骤4:通过重结晶提纯粗产品后,获得无色片状晶体,干燥后得目标产品.
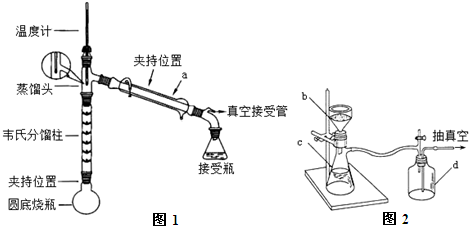
(1)仪器a的名称为冷凝管.
(2)步骤1中加入锌粉的作用是防止苯胺被氧化,同时起着沸石的作用.
(3)步骤2中控制温度计示数约105℃的原因是乙酸有挥发性,温度过高,乙酸蒸出,降低了反应物的利用率,而温度过低,不能除去反应生成水.
(4)步骤3中,抽滤装置如图2所示,仪器c的名称是吸滤瓶,当过滤的溶液具有强酸性、强碱性或强氧化性时要用玻璃纤维代替滤纸或用玻璃砂漏斗代替布氏漏斗,停止抽滤时的操作为先旋开安全瓶d上的旋塞恢复常压然后关闭抽气泵.
0 153843 153851 153857 153861 153867 153869 153873 153879 153881 153887 153893 153897 153899 153903 153909 153911 153917 153921 153923 153927 153929 153933 153935 153937 153938 153939 153941 153942 153943 153945 153947 153951 153953 153957 153959 153963 153969 153971 153977 153981 153983 153987 153993 153999 154001 154007 154011 154013 154019 154023 154029 154037 203614
 +CH3COOH$\stackrel{△}{→}$
+CH3COOH$\stackrel{△}{→}$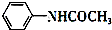 +H2O
+H2O已知:①苯胺易被氧化; ②苯胺、醋酸和乙酰苯胺的部分物理性质如表:
| 试剂名称 | 熔点℃ | 沸点℃ | 溶解度(20℃) |
| 苯胺 | -6.2 | 184.4 | 稍溶于水(3.4g),与乙醇、乙醚、苯混溶 |
| 乙酸 | 16.7 | 118 | 易溶于水、乙醇、乙醚等 |
| 乙酰苯胺 | 114~116 | 280~290 | 0.46g |
步骤1:在下图1装置的圆底烧瓶中,加入6.0mL苯胺、9.0mL冰醋酸及0.2g锌粉.
步骤2:控制温度计示数约105℃,小火加热回流1h.
步骤3:趁热将反应混合物倒入盛有100mL冷水的烧杯中,抽滤,洗涤,得到粗产品.
步骤4:通过重结晶提纯粗产品后,获得无色片状晶体,干燥后得目标产品.

(1)仪器a的名称为冷凝管.
(2)步骤1中加入锌粉的作用是防止苯胺被氧化,同时起着沸石的作用.
(3)步骤2中控制温度计示数约105℃的原因是乙酸有挥发性,温度过高,乙酸蒸出,降低了反应物的利用率,而温度过低,不能除去反应生成水.
(4)步骤3中,抽滤装置如图2所示,仪器c的名称是吸滤瓶,当过滤的溶液具有强酸性、强碱性或强氧化性时要用玻璃纤维代替滤纸或用玻璃砂漏斗代替布氏漏斗,停止抽滤时的操作为先旋开安全瓶d上的旋塞恢复常压然后关闭抽气泵.
 硫酸厂用煅烧黄铁矿(FeS2)来制取硫酸,实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制备绿矾.
硫酸厂用煅烧黄铁矿(FeS2)来制取硫酸,实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制备绿矾.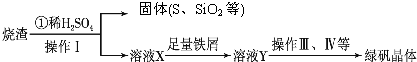
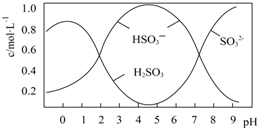 葡萄酒常用Na2S2O5做抗氧化剂.
葡萄酒常用Na2S2O5做抗氧化剂.