3.下列各组物质在溶液中不发生化学反应而能共存的是( )
| A. | Na2SO4 KNO3 Na2CO3 NH4Cl | B. | H2SO4 BaCl2 Na2SO4 NaOH | ||
| C. | MgCl2 AgNO3 KNO3 HCl | D. | NH4HCO3 NaOH NaCl HCl |
1.下列离子方程式书写不正确的是( )
| A. | Fe与HCl反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | Cu与AgNO3反应:2Ag++Cu═Cu2++2Ag | |
| C. | 醋酸与NaOH反应:CH3COOH+OH-═CH3COO-+H2O | |
| D. | CuSO4与Ba(OH)2反应:Cu2++2OH-+SO42-+Ba2+═BaSO4↓+Cu(OH)2↓ |
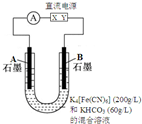
20.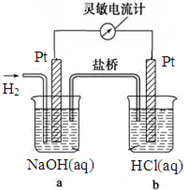 如图向a中通入H2,发现灵敏电流计指针发生偏转,持续通入H2可观察到b中铂电极表面有少量气泡产生,负极反应式为H2-2e-+2OH-=2H2O,电池的总反应为HCl+NaOH=H2O+NaCl.
如图向a中通入H2,发现灵敏电流计指针发生偏转,持续通入H2可观察到b中铂电极表面有少量气泡产生,负极反应式为H2-2e-+2OH-=2H2O,电池的总反应为HCl+NaOH=H2O+NaCl.
 如图向a中通入H2,发现灵敏电流计指针发生偏转,持续通入H2可观察到b中铂电极表面有少量气泡产生,负极反应式为H2-2e-+2OH-=2H2O,电池的总反应为HCl+NaOH=H2O+NaCl.
如图向a中通入H2,发现灵敏电流计指针发生偏转,持续通入H2可观察到b中铂电极表面有少量气泡产生,负极反应式为H2-2e-+2OH-=2H2O,电池的总反应为HCl+NaOH=H2O+NaCl.
18.以天然气替代石油生产液体燃料和基础化学品是当前化学研究和发展的重点.
(1)我国科学家包信和院士领衔的团队,创造性地构建了硅化物晶格限域的单中心铁催化剂,成功实现了甲烷一步高效生产链烃X、芳烃Y和Z等重要化工原料,反应过程本身实现了CO2的零排放,碳原子利用效率达到100%.若X、Y、Z的相对分子质量分别为28、78、128,且X、Y的核磁共振氢谱只有一个峰,Z的核磁共振氢谱有二个峰.
①有关化学键键能数据如下:
写出甲烷一步生成X的热化学方程式2CH4(g)$\stackrel{催化剂}{→}$C2H4(g)+2H2(g)△H=+166.6kJ/mol,
硅化物晶格限域的单中心铁催化剂的作用是降低反应的活化能,加快反应的速率.
②甲烷生成芳烃Y的原子利用率为81.25%.
③Z的结构简式为(CH3)3CCH2C(CH3)3,其二氯取代物有6种.
(2)碳酸乙二醇酯在锂电池中有重要用途.已知:

①请以CO2、X、空气为原料,利用绿色化学原则制备碳酸乙二醇酯,写出有关反应的化学方程式 、
、 .
.
②生产1t碳酸乙二醇酯在理论上可以吸收0.5t CO2.
(1)我国科学家包信和院士领衔的团队,创造性地构建了硅化物晶格限域的单中心铁催化剂,成功实现了甲烷一步高效生产链烃X、芳烃Y和Z等重要化工原料,反应过程本身实现了CO2的零排放,碳原子利用效率达到100%.若X、Y、Z的相对分子质量分别为28、78、128,且X、Y的核磁共振氢谱只有一个峰,Z的核磁共振氢谱有二个峰.
①有关化学键键能数据如下:
| 化学键 | H-H | C═C | C-C | C≡C | C-H |
| E/(kJ•mol-1) | 436.0 | 615 | 347.7 | 812 | 413.4 |
硅化物晶格限域的单中心铁催化剂的作用是降低反应的活化能,加快反应的速率.
②甲烷生成芳烃Y的原子利用率为81.25%.
③Z的结构简式为(CH3)3CCH2C(CH3)3,其二氯取代物有6种.
(2)碳酸乙二醇酯在锂电池中有重要用途.已知:

①请以CO2、X、空气为原料,利用绿色化学原则制备碳酸乙二醇酯,写出有关反应的化学方程式
 、
、 .
.②生产1t碳酸乙二醇酯在理论上可以吸收0.5t CO2.
17.下列有关绿色化学的叙述中,不正确的是( )
| A. | 绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染 | |
| B. | 最理想的“原子经济”就是反应物的原子全部转化为期望的最终产物 | |
| C. | 绿色化学反应选择的原料、催化剂、溶剂都应该是无毒无害的 | |
| D. | 乙烯分别与溴水和溴的四氯化碳溶液反应制备1,2-二溴乙烷的原子利用率均为100% |
16.某学生欲通过实验验证Fe2+的性质.
(1)该同学在实验前,依据Fe的还原性,填写了下表.
依照表中操作,该同学进行实验,观察到液面上方气体逐渐变为红棕色,但试管中溶液颜色却变为深棕色.为探究溶液变为深棕色的原因,该同学进行了如下实验.
(2)向原新制FeSO4溶液和反应后溶液中均加入KSCN溶液,前者不变红色,后者变红.该现象的结论是Fe2+被硝酸氧化为Fe3+.
(3)查阅资料,发现溶液的深棕色可能是NO2或NO与溶液中Fe3+或Fe2+发生反应而得到的.为此他利用如图装置(气密性已检验,尾气处理装置略)进行探究.
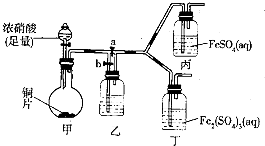
Ⅰ、打开活塞a,关闭b,并使甲装置中反应开始后,观察到丙中溶液逐渐变为深棕色,而丁中溶液并无明显变化.
Ⅱ、打开活塞b、关闭a,一段时间后再停止甲中反应.
Ⅲ、为与I中实验对照,更换丙、丁后,使甲中反应继续,观察到的现象与步骤I中相同.
①铜与足量浓硝酸反应的化学方程式是Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;
②装置乙的作用是使NO2转化为NO;
③步骤II的目的是排出乙右侧装置中残留的NO2;
④该实验可得出的结论是溶液的深棕色是由NO或NO2与Fe2+作用得到(或不是由NO或NO2与Fe3+作用得到).
(4)该同学重新进行(1)中实验,观察到了预期现象,他的实验操作是向盛有浓硝酸的试管中滴入数滴新制FeSO4溶液,振荡.
(1)该同学在实验前,依据Fe的还原性,填写了下表.
| 实验操作 | 预期现象 | 离子方程式 |
| 向盛有新制FeSO4溶液的试管中滴入数滴浓硝酸,振荡 | 试管中产生红棕色气体,溶液颜色逐渐变黄 | Fe2++NO3-+2H+=Fe3++NO2↑+H2O |
(2)向原新制FeSO4溶液和反应后溶液中均加入KSCN溶液,前者不变红色,后者变红.该现象的结论是Fe2+被硝酸氧化为Fe3+.
(3)查阅资料,发现溶液的深棕色可能是NO2或NO与溶液中Fe3+或Fe2+发生反应而得到的.为此他利用如图装置(气密性已检验,尾气处理装置略)进行探究.

Ⅰ、打开活塞a,关闭b,并使甲装置中反应开始后,观察到丙中溶液逐渐变为深棕色,而丁中溶液并无明显变化.
Ⅱ、打开活塞b、关闭a,一段时间后再停止甲中反应.
Ⅲ、为与I中实验对照,更换丙、丁后,使甲中反应继续,观察到的现象与步骤I中相同.
①铜与足量浓硝酸反应的化学方程式是Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;
②装置乙的作用是使NO2转化为NO;
③步骤II的目的是排出乙右侧装置中残留的NO2;
④该实验可得出的结论是溶液的深棕色是由NO或NO2与Fe2+作用得到(或不是由NO或NO2与Fe3+作用得到).
(4)该同学重新进行(1)中实验,观察到了预期现象,他的实验操作是向盛有浓硝酸的试管中滴入数滴新制FeSO4溶液,振荡.
15.肉桂醛常用于牙膏、口香糖、口气清新剂等口腔护理品,其结构简式如图所示.工业上电解肉桂醇制备肉桂醛,下列说法不正确的是( )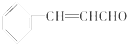
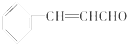
| A. | 煮沸肉桂醛与新制Cu(OH)2的混合物有砖红色沉淀生成 | |
| B. | 电解肉桂醇制得的肉桂醛在电解池的阳极生成 | |
| C. | 仅用新制银氨溶液和溴水不能鉴别肉桂醛中的碳碳双键 | |
| D. | 13.2g肉桂醛分子中含有碳碳双键数目为0.4NA |
14.有些古文或谚语包含了丰富的化学知识,从化学角度解释下列古文或谚语,其中不正确的是( )
0 153792 153800 153806 153810 153816 153818 153822 153828 153830 153836 153842 153846 153848 153852 153858 153860 153866 153870 153872 153876 153878 153882 153884 153886 153887 153888 153890 153891 153892 153894 153896 153900 153902 153906 153908 153912 153918 153920 153926 153930 153932 153936 153942 153948 153950 153956 153960 153962 153968 153972 153978 153986 203614
| 选项 | 古文或谚语 | 化学解释 |
| A | 日照香炉生紫烟 | 碘的升华 |
| B | 以曾青涂铁,铁赤色如铜 | 置换反应 |
| C | 煮豆燃豆箕,豆在斧中泣 | 化学能转化为热能 |
| D | 雷雨肥庄稼 | 自然界固氮作用 |
| A. | A | B. | B | C. | C | D. | D |
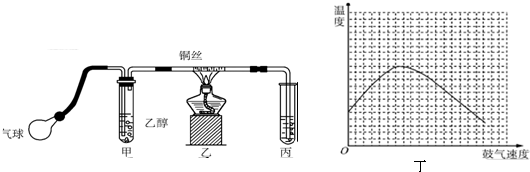
 气态废弃物中的硫化氢可用下法转化为可利用的硫.
气态废弃物中的硫化氢可用下法转化为可利用的硫.