3.在碱性溶液中能大量共存且溶液为无色透明的离子组是( )
| A. | K+ MnO4- Na+ Cl- | B. | K+ Na+ NO3- CO32- | ||
| C. | Na+ H+ NO3- SO42- | D. | Fe3+ Na+ Cl- SO42- |
2.下列说法正确的是(NA表示阿伏加德罗常数)( )
| A. | 在常温常压下,11.2 升氯气含有的分子数为0.5NA | |
| B. | 1 molFe与足量的Cl2反应转移的电子数为2NA | |
| C. | 常温常压下,32 g O2和O3的混合气体所含原子数为2NA | |
| D. | 标准状况下,22.4 LSO3含有的原子数为4NA |
1. 汽车尾气是城市主要空气污染物,研究控制汽车尾气排放是保护环境的首要任务.
汽车尾气是城市主要空气污染物,研究控制汽车尾气排放是保护环境的首要任务.
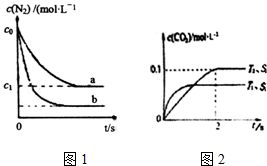
(1)汽车内燃机工作时发生反应N2(g)+O2(g)?2NO(g),是导致汽车尾气中含有NO的原因之一.T0℃时将等物质的量的N2(g)和O2(g)充入恒容密闭容器中发生反应,图1曲线a表示该反应在T0℃下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化.下列叙述正确的是ad.
a.温度T0℃下,该反应的平衡常数K=$\frac{4({c}_{0}-{c}_{1})^{2}}{{{c}_{1}}^{2}}$
b.温度T0℃下,随着反应的进行,混合气体的密度减小
c.曲线b对应的条件改变可能是充入了NO气体
d.若曲b对应的条件改变是温度,可判断△H>0
(2)汽车安装尾气催化转化器可将尾气中的主要污染物转化成无毒物质,反应为:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H.某科研小组为了探究催化剂的效果,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
①2~3s间的平均反应速率v(N2)=4.5×10-5mol•L-1•S1.
②在该温度下,反应的平衡常数K=5000.
③在使用等质量催化剂时,增大固体催化剂的表面积可提高化学反应速率.下图表示在其他条件不变时,CO2的浓度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线.由此可知该反应的△H<0(填“>”“<”),原因是温度T1到达平衡的时间短,反应速率快,故温度T2<T1,温度越高,平衡时CO2的浓度越低,说明升高温度平衡向逆反应移动,故正反应为放热反应,即△H<0.
若催化剂的表面积S1>S2,在图2中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线.
④假设在密闭容器中发生上述反应,达到平衡时能提高NO转化率的措施是降低反应体系的温度或缩小容器的体积.
(3)用NH3还原NOx生成N2和H2O也可以减少污染.现有NO、NO2的混合气3L,可用同温同压下3.5L的NH3恰好使其完全转化为N2,则原混合气体中NO和NO2的物质的量之比为1:3.
 汽车尾气是城市主要空气污染物,研究控制汽车尾气排放是保护环境的首要任务.
汽车尾气是城市主要空气污染物,研究控制汽车尾气排放是保护环境的首要任务.(1)汽车内燃机工作时发生反应N2(g)+O2(g)?2NO(g),是导致汽车尾气中含有NO的原因之一.T0℃时将等物质的量的N2(g)和O2(g)充入恒容密闭容器中发生反应,图1曲线a表示该反应在T0℃下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化.下列叙述正确的是ad.
a.温度T0℃下,该反应的平衡常数K=$\frac{4({c}_{0}-{c}_{1})^{2}}{{{c}_{1}}^{2}}$
b.温度T0℃下,随着反应的进行,混合气体的密度减小
c.曲线b对应的条件改变可能是充入了NO气体
d.若曲b对应的条件改变是温度,可判断△H>0
(2)汽车安装尾气催化转化器可将尾气中的主要污染物转化成无毒物质,反应为:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H.某科研小组为了探究催化剂的效果,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/(×10-4mol•L-1) | 10.0 | 4.50 | 2.50 | 1.60 | 1.00 | 1.00 |
| c(CO)/(×10-3mol•L-1) | 3.60 | 3.05 | 2.85 | 2.76 | 2.70 | 2.70 |
②在该温度下,反应的平衡常数K=5000.
③在使用等质量催化剂时,增大固体催化剂的表面积可提高化学反应速率.下图表示在其他条件不变时,CO2的浓度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线.由此可知该反应的△H<0(填“>”“<”),原因是温度T1到达平衡的时间短,反应速率快,故温度T2<T1,温度越高,平衡时CO2的浓度越低,说明升高温度平衡向逆反应移动,故正反应为放热反应,即△H<0.
若催化剂的表面积S1>S2,在图2中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线.
④假设在密闭容器中发生上述反应,达到平衡时能提高NO转化率的措施是降低反应体系的温度或缩小容器的体积.
(3)用NH3还原NOx生成N2和H2O也可以减少污染.现有NO、NO2的混合气3L,可用同温同压下3.5L的NH3恰好使其完全转化为N2,则原混合气体中NO和NO2的物质的量之比为1:3.
20.向CuSO4溶液中逐滴加入KI溶液至过量,产生白色沉淀CuI,溶液变为棕色.再向反应后的溶液中不断通入SO2气体,溶液逐渐变成无色.下列有关说法错误的是( )
| A. | 产生白色沉淀反应的离子方程式为:2Cu2++4I-=2CuI↓+I2 | |
| B. | 通入SO2后溶液逐渐变成无色,体现了SO2的漂白性 | |
| C. | 上述实验条件下,物质的氧化性强弱顺序为:Cu2+>I2>SO2 | |
| D. | 滴加KI溶液时,每生成1mol CuI转移1mol e- |
19.科技人员研究“变害为宝”的途径,以NO为原料通过电解制备NH4NO3.其工作原理如图所示,下列有关说法错误的是( )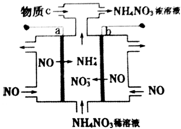

| A. | b为阳极,连接电源的正极 | |
| B. | 阴极反应式为3NO+15e-+18H+═3NH4++3H2O | |
| C. | 为使电解产物全部转化为NH4NO3,需补充的物质c为HNO3 | |
| D. | 总反应式为:8NO+7H2O$\frac{\underline{\;通电\;}}{\;}$3NH4NO3+2NHO3 |
18.下列除杂方法错误的是( )
| A. | 镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤 | |
| B. | KNO3固体中混有少量NaCl:加H2O配制热的饱和溶液,再冷却结晶、过滤 | |
| C. | 乙醇中的少量水:加入适量新制的生石灰,加热蒸馏 | |
| D. | 二氧化碳中混有少量一氧化碳:点燃除去 |
17.某实验小组分析m1g由Al、Cu、Al2O3、Fe3O4组成的混合物粉末A成分,方案如下:
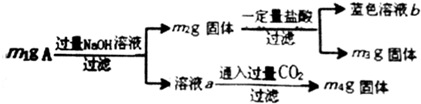
下列分析错误的是( )

下列分析错误的是( )
| A. | 由m1、m2、m4可计算出混合物中Al、Al2O3的物质的量 | |
| B. | 生成蓝色溶液的离子方程式为Cu+2Fe3+=Cu2++2Fe2+ | |
| C. | 蓝色溶液中一定有Cu2+、Fe2+、Fe3+ | |
| D. | 当m2-m3=2.96g时,Fe3O4的质量至少为2.32g |
16.已知常温下,HClO的Ka=3.0×10-8,现有3mol•L-1 NaClO消毒液,内含有一定量的NaOH,下列用来解释事实的离子方程式不合理的是( )
| A. | 该消毒液的pH约为13:ClO-+H2O?HClO+OH- | |
| B. | 该消毒液可用NaOH溶液吸收Cl2制备:Cl2+2OH-═Cl-+ClO-+H2O | |
| C. | 该消毒液与洁厕灵(主要成分为HCl)混用,产生Cl2:2H++Cl-+ClO-═Cl2↑+H2O | |
| D. | 该消毒液加白醋生成HClO,可增强漂白作用:CH3COOH+ClO-═HClO+CH3COO- |
15.下列对有关实验操作产生的影响及原因分析都正确的是( )
| 选项 | 实验目的和操作 | 影响结果 | 原因分析 |
| A | 将2g I2加入到98mLCCl4中溶解混匀后,配制质量分数为2% I2的CCl4溶液 | 偏小 | CCl4的密度大于1g•mL-1 |
| B | 用10mL的量筒测量酯化反应得到乙酸乙酯的体积,俯视液面读出数据为6.0mL | 偏小 | 平视读取应大于6.0mL |
| C | 配制2mol•L-1NaCl溶液,定容时加入的水超过了刻度线,立即用滴管吸出多余的水,再摇匀 | 无影响 | 吸出了多余的水 |
| D | 用尖嘴有气泡的碱式滴定管盛标准NaOH溶液滴定20.00mL某待测HCl溶液的浓度 | 偏大 | 流出碱液的量 变大 |
| A. | A | B. | B | C. | C | D. | D |
14.短周期元素W、X、Y、Z的原子序数依次增大,X、Y、Z的简单离子的电子层结构相同,W与Y原子的最外层电子数之和为X原子的最外层电子数的2倍,Z原子的L层电子数比其最外层电子数多5,W是植物生长不可缺少的三种营养元素之一.下列说法正确的是( )
0 153784 153792 153798 153802 153808 153810 153814 153820 153822 153828 153834 153838 153840 153844 153850 153852 153858 153862 153864 153868 153870 153874 153876 153878 153879 153880 153882 153883 153884 153886 153888 153892 153894 153898 153900 153904 153910 153912 153918 153922 153924 153928 153934 153940 153942 153948 153952 153954 153960 153964 153970 153978 203614
| A. | 单质的沸点:W>X | B. | Y的最高化合价为+7 | ||
| C. | 原子半径:r(W)<r(X)<r(Y)<r(Z) | D. | W、X、能存在于同一离子化合物中 |