3.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 含有NA个氦原子的氦气在标准状况下的体积约为22.4L | |
| B. | 常温常压下,28g N2中含有的原子数为NA | |
| C. | 标准状况下22.4L Cl2与足量的水充分反应,转移的电子数为NA | |
| D. | 标准状况下,11.2LH2O含有的分子数为0.5NA |
2.V、W、X、Y均是元素周期表中短周期元素,在周期表中的相对位置关系如表所示:
V的最简单氢化物为甲,W的最简单氢化物为乙,甲、乙混合时有白烟生成.下列说法正确的是( )
| Y | V | |||
| X | W |
| A. | 原子半径:X>W>V>Y | |
| B. | Y的最高价氧化物的电子式为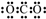 | |
| C. | X的最高价氧化物能与V、W最高价氧化物对应的水化物反应 | |
| D. | 甲、乙混合时所生成的白烟为离子化合物,只含有离子键 |
20.菜谱中记载:河虾不宜与西红柿同食.主要原因是河虾中含有五价砷,西红柿中含有比较多的维生素C,两者同食时会生成有毒的三价砷.下列说法不正确的是( )
| A. | 五价砷在维生素C作用下发生了还原反应 | |
| B. | “两者同食”发生的反应中维生素C作还原剂 | |
| C. | 河虾中含有的五价砷,没有毒性 | |
| D. | 毒药砒霜是含砷的氧化物,可以推测砒霜中所含的砷元素化合价为+5 |
19.下列实验操作中,所用仪器合理的是( )
| A. | 用25ml的碱式滴定管量取14.80mlNaOH溶液 | |
| B. | 用100ml量筒量取5.2ml的盐酸 | |
| C. | 用托盘天平称取25.20gNaCl | |
| D. | 用100ml容量瓶配制50ml1.0mol/L盐酸 |
18.只用一种试剂可区别Na2SO4、MgCl2、FeCl2、Al2(SO4)3、(NH4)2SO4五种溶液,这种试剂是( )
| A. | Ba(OH)2 | B. | H2SO4 | C. | NaOH | D. | Fe(OH)3胶体 |
17.将Mg、Cu组成的26.4g混合物投入到适量的稀硝酸中,固体完全溶解,收集到标准状况下的NO气体8.96L,向反应后的溶液中加入足量的4mol•L-1的NaOH溶液,使金属离子完全沉淀.则形成沉淀的质量是( )
| A. | 43.2 g | B. | 46.8 g | C. | 53.6 g | D. | 63.8 g |
15.在一定条件下发生下列反应,其中属于盐类水解反应的是( )
| A. | NH4++2H2O?NH3•H2O+H3O+ | B. | HCO3-+H2O?H3O++CO32- | ||
| C. | HS-+H+═H2S | D. | Cl2+H2O?H++Cl-+HClO |
14.下列电离方程式中,正确的是( )
0 153762 153770 153776 153780 153786 153788 153792 153798 153800 153806 153812 153816 153818 153822 153828 153830 153836 153840 153842 153846 153848 153852 153854 153856 153857 153858 153860 153861 153862 153864 153866 153870 153872 153876 153878 153882 153888 153890 153896 153900 153902 153906 153912 153918 153920 153926 153930 153932 153938 153942 153948 153956 203614
| A. | H2S?2H++S2- | B. | NaHCO3═Na++H++CO32- | ||
| C. | NaCl═Na++Cl- | D. | CH3COOH═CH3COO-+H+ |