14. 苯甲酸具有弱酸性,可以和乙醇发生酯化反应生成苯甲酸乙酯.苯甲酸乙脂 (密度1.05g ?cm-3)稍有水果气味,用于配制香水香精和人造精油,也大量用于食品以及用作有机合成中间体等.制备苯甲酸乙脂的过程如下:
苯甲酸具有弱酸性,可以和乙醇发生酯化反应生成苯甲酸乙酯.苯甲酸乙脂 (密度1.05g ?cm-3)稍有水果气味,用于配制香水香精和人造精油,也大量用于食品以及用作有机合成中间体等.制备苯甲酸乙脂的过程如下:
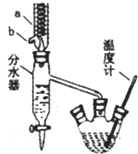
(1)制备粗产品:如图所示装置中,于50mL圆底烧瓶中加人8.0g苯甲酸(Mr=122)、20mL乙醇(Mr=46,密度0.79g?cm-3)、15mL环己烷、3mL浓硫酸,摇匀,加沸石.在分水器上加水,接通冷凝水,水浴回流约2h,反应基本完成.记录体积,继续蒸出多余环己烷和醇(从分水器中放出).
(2)粗产品纯化:加水30ml.,分批加人固体NaHCO3,分液,然后水层用20mL石油醚分两次萃取.合并有机层,用无水硫酸镁干燥.回收石油醚,加热精馏,收集210一213℃馏分.
相关数据如表:
请根据以上信息和装置图回答下述实验室制备有关问题:
(1)写出制备苯甲酸乙醋反应的化学方程式 +CH3CH2OH$?_{△}^{浓硫酸}$
+CH3CH2OH$?_{△}^{浓硫酸}$ +H2O仪器a的名称冷凝管,b口的作用为出水口,
+H2O仪器a的名称冷凝管,b口的作用为出水口,
(2)请说出在本实验中可以采取的能提高笨甲酸乙酸产率的方法加入环已烷形成水-乙醇-环已烷三元共沸物分离出反应过程中生成的水,或加过量的乙醇,或使用分液器及时分离子出生成的水等(写出任意一种即可).
(3)如何利用实验现象判断反应已基本完成加热回流至分水器中水位不再上升
(4)固体NaHCO.的作用中和硫酸和未反应的苯甲酸,加人固体NaHCO3时的实验操作所用到的主要玻璃仪器为分液漏斗.
(5)经精馏得210-213℃馏分7.0mL,则实验中苯甲酸乙脂的产率为73.7%.
 苯甲酸具有弱酸性,可以和乙醇发生酯化反应生成苯甲酸乙酯.苯甲酸乙脂 (密度1.05g ?cm-3)稍有水果气味,用于配制香水香精和人造精油,也大量用于食品以及用作有机合成中间体等.制备苯甲酸乙脂的过程如下:
苯甲酸具有弱酸性,可以和乙醇发生酯化反应生成苯甲酸乙酯.苯甲酸乙脂 (密度1.05g ?cm-3)稍有水果气味,用于配制香水香精和人造精油,也大量用于食品以及用作有机合成中间体等.制备苯甲酸乙脂的过程如下:(1)制备粗产品:如图所示装置中,于50mL圆底烧瓶中加人8.0g苯甲酸(Mr=122)、20mL乙醇(Mr=46,密度0.79g?cm-3)、15mL环己烷、3mL浓硫酸,摇匀,加沸石.在分水器上加水,接通冷凝水,水浴回流约2h,反应基本完成.记录体积,继续蒸出多余环己烷和醇(从分水器中放出).
(2)粗产品纯化:加水30ml.,分批加人固体NaHCO3,分液,然后水层用20mL石油醚分两次萃取.合并有机层,用无水硫酸镁干燥.回收石油醚,加热精馏,收集210一213℃馏分.
相关数据如表:
| 沸点(℃,1atm) | ||||||
| 苯甲酸 | 苯甲酸乙酯 | 石油醚 | 水 | 乙醇 | 环己烷 | 共沸物(环已烷-水-乙醇) |
| 249 | 212.6 | 40-80 | 100 | 78.3 | 80.75 | 62.6 |
(1)写出制备苯甲酸乙醋反应的化学方程式
 +CH3CH2OH$?_{△}^{浓硫酸}$
+CH3CH2OH$?_{△}^{浓硫酸}$ +H2O仪器a的名称冷凝管,b口的作用为出水口,
+H2O仪器a的名称冷凝管,b口的作用为出水口,(2)请说出在本实验中可以采取的能提高笨甲酸乙酸产率的方法加入环已烷形成水-乙醇-环已烷三元共沸物分离出反应过程中生成的水,或加过量的乙醇,或使用分液器及时分离子出生成的水等(写出任意一种即可).
(3)如何利用实验现象判断反应已基本完成加热回流至分水器中水位不再上升
(4)固体NaHCO.的作用中和硫酸和未反应的苯甲酸,加人固体NaHCO3时的实验操作所用到的主要玻璃仪器为分液漏斗.
(5)经精馏得210-213℃馏分7.0mL,则实验中苯甲酸乙脂的产率为73.7%.
13.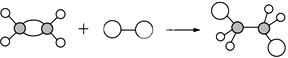 如图表示某有机反应,该反应的类型是( )
如图表示某有机反应,该反应的类型是( )
 如图表示某有机反应,该反应的类型是( )
如图表示某有机反应,该反应的类型是( )| A. | 取代反应 | B. | 加成反应 | C. | 氧化反应 | D. | 聚合反应 |
12. 如图,将新制的氯气通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色.则甲装置中所盛有的试剂不可能是( )
如图,将新制的氯气通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色.则甲装置中所盛有的试剂不可能是( )
 如图,将新制的氯气通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色.则甲装置中所盛有的试剂不可能是( )
如图,将新制的氯气通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色.则甲装置中所盛有的试剂不可能是( )| A. | 浓硫酸 | B. | NaOH溶液 | C. | Kl溶液 | D. | 饱和食盐水 |
11.根据元素周期律及物质结构的有关知识,判断以下有关排序不正确的是( )
| A. | 原子半径:Al>Mg>Na | B. | 热稳定性:HF>H2O>NH3 | ||
| C. | 酸性:HClO4>H2SO4>H2PO4 | D. | 金属性:Na>Mg>Al |
10.下列反应的离子方程式书写正确的是( )
| A. | 金属铁与过量的稀盐酸反应:2Fe+6H+→2Fe3++3H2↑ | |
| B. | 氯化亚铁溶液中通入少量氯气:Fe2++Cl2→Fe3++2Cl- | |
| C. | 氧化铝与氢氧化钠溶液反应:Al2O3+2OH-=2AlO2-+H2O | |
| D. | 氯化铝溶液中加入过量的氨水:Al3++3OH-→Al(OH)3↓ |
9.下列对有关铁和铝反应现象的描述,正确的是( )
| A. | 在氧气中点燃细铁丝产生白色的烟 | |
| B. | 铁粉和硫粉混合加热生成黑色固体 | |
| C. | 纯铝在空气中放置会长出白毛 | |
| D. | 将铝片放入CuSO4溶液反应完全后,溶液由蓝色变为红色 |
8.下列化合物中,不能由化合反应直接制得的是( )
| A. | FeCl3 | B. | FeCl2 | C. | FeS | D. | Al(OH)3 |
7.产物主要是Fe2O3的反应是( )
| A. | 铁在纯氧中燃烧 | B. | 红热的铁和水蒸气反应 | ||
| C. | Fe2(CO4)3与氨水混合 | D. | 灼烧氢氧化铁固体 |
6.目前,CO、CO2的有效开发利用成为科学家研究的重要课题.
Ⅰ.CO可用于合成甲醇
(1)已知:CO、H2、CH3OH(g)的燃烧热分别为-283kJ•mol-1、-285.8kJ•mol-1、-764.5kJ•mol-1,则CO(g)+2H2(g)?CH3OH(g)的△H=-90.1kJ•mol-1.
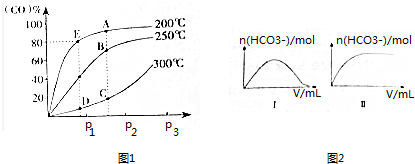
(2)将1molCO和2molH2充入密闭容器中发生上述反应.气体条件相同时,CO的平衡转化率[α(CO)]与压强(p)和温度(T)的关系如图1所示.
①A、B两点CH3OH的质量分数ω(A)>ω(B)(填“>”、“<”或“=”),理由为A点温度低于B点,该反应为放热反应,升高温度,平衡向逆反应方向移动.
②C、D两点的逆反应速率:v正(C)>v逆(D)(填“>”、“<”或“=”),理由为该反应为有气体参与的反应,C点压强大于D点,增大压强,反应速率越快.
③200℃时,测得E的容器容积为10L.该温度下,反应的平衡常数K=2500;保持温度和容积不变,再向容器中充入1molCO、1molH2和xmolCH3OH时,若使v正>v逆,则x的取值范围为0<x<58.
Ⅱ.CO2的综合利用
(3)CO2转化为甲醇有广泛应用前景.T℃时,在容积为1L的恒容密闭容器中,充入1molCO2和3molH2,发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0,其它条件不变,下列措施中能使$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大的是B(填选项字母).
A.升高温度 B.再充入1molCH3OH(g)和1molH2O(g) C.加入催化剂 D.再充入一定量CO2
(4)CO2可转化为碳酸盐,其中Na2CO3是一种用途广泛的碳酸盐.
已知:25℃时,几种酸的电离平衡常数如下表所示.
25℃时,向一定浓度的Na2CO3溶液中分别滴入等物质的量浓度的下列溶液至过量:①NaHC2O4②HNO3③HClO,溶液中的n(HCO3-)与所加入溶液体积(V)的关系如图2所示.其中,符合曲线Ⅰ的溶液为①②(填序号,下同);符合曲线Ⅱ的溶液为③.
0 153703 153711 153717 153721 153727 153729 153733 153739 153741 153747 153753 153757 153759 153763 153769 153771 153777 153781 153783 153787 153789 153793 153795 153797 153798 153799 153801 153802 153803 153805 153807 153811 153813 153817 153819 153823 153829 153831 153837 153841 153843 153847 153853 153859 153861 153867 153871 153873 153879 153883 153889 153897 203614

Ⅰ.CO可用于合成甲醇
(1)已知:CO、H2、CH3OH(g)的燃烧热分别为-283kJ•mol-1、-285.8kJ•mol-1、-764.5kJ•mol-1,则CO(g)+2H2(g)?CH3OH(g)的△H=-90.1kJ•mol-1.
(2)将1molCO和2molH2充入密闭容器中发生上述反应.气体条件相同时,CO的平衡转化率[α(CO)]与压强(p)和温度(T)的关系如图1所示.
①A、B两点CH3OH的质量分数ω(A)>ω(B)(填“>”、“<”或“=”),理由为A点温度低于B点,该反应为放热反应,升高温度,平衡向逆反应方向移动.
②C、D两点的逆反应速率:v正(C)>v逆(D)(填“>”、“<”或“=”),理由为该反应为有气体参与的反应,C点压强大于D点,增大压强,反应速率越快.
③200℃时,测得E的容器容积为10L.该温度下,反应的平衡常数K=2500;保持温度和容积不变,再向容器中充入1molCO、1molH2和xmolCH3OH时,若使v正>v逆,则x的取值范围为0<x<58.
Ⅱ.CO2的综合利用
(3)CO2转化为甲醇有广泛应用前景.T℃时,在容积为1L的恒容密闭容器中,充入1molCO2和3molH2,发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0,其它条件不变,下列措施中能使$\frac{n(C{H}_{3}OH)}{n(C{O}_{2})}$增大的是B(填选项字母).
A.升高温度 B.再充入1molCH3OH(g)和1molH2O(g) C.加入催化剂 D.再充入一定量CO2
(4)CO2可转化为碳酸盐,其中Na2CO3是一种用途广泛的碳酸盐.
已知:25℃时,几种酸的电离平衡常数如下表所示.
| H2CO3 | H2C2O4 | HNO2 | HClO |
| K1=4.4×10-7 K2=4.7×10-11 | K1=5.4×10-2 K2=5.3×10-5 | K=7.2×10-4 | K=2.9×10-8 |
