5.下列物质中,只含有离子键的是( )
| A. | NaOH | B. | NH3 | C. | CaCl2 | D. | H2S04 |
3.一定温度下,在2L的密闭容器中,冲入1molHI气体,能说明反应2HI(g)?H2(g)+I2(g)达到平衡状态的标志是( )
| A. | 单位时间内消耗1molH2,同时生成2molHI | |
| B. | 每断裂AmolH-I,同时有$\frac{A}{2}$molH-H断裂 | |
| C. | 容器中压强不再变化 | |
| D. | 容器中混合气体的密度不再变化 |
2.下列有关化学用语表达正确的是( )
| A. | 氨分子的电子式: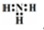 | |
| B. | 质子数为17、中子数为20的氯原子:${\;}_{17}^{20}$Cl | |
| C. | O2-的结构示意图为: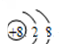 | |
| D. | ${\;}_{35}^{79}$Br的基态原子电子排布式:[Ar]4S24P5 |
1.50℃时,下列各溶液中,离子的物质的量浓度关系正确的是( )
| A. | 饱和食盐水中:c(Na+)+c(H+)=c(Cl-)+c(OH-) | |
| B. | 饱和小苏打溶液中:c(Na+)=c(HCO3-) | |
| C. | pH=4的醋酸中:c(H+)=4.0mol•L-1 | |
| D. | pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol•L-1 |
20.下列陈述正确并且有因果关系的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2有漂白性 | SO2可使溴水褪色 |
| B | SiO2有导电性 | SiO2可用于制备光导纤维 |
| C | Fe3+有强氧化性 | FeCl3溶液可用于回收废旧电路板中的铜 |
| D | 浓硫酸有强氧化性 | 浓硫酸可用于干燥H2和CO |
| A. | A | B. | B | C. | C | D. | D |
19.短周期元素X、Y、Z、W在元素周期表中的相对应位置如图所示,其中Z为地壳中含量最高的金属元素.下列说法正确的是( )
| X | ||||||
| Y | Z | W |
| A. | 工业上电解YW饱和溶液冶炼金属Y | |
| B. | Y、W的最高价氧化物的水化物均能溶解金属Z | |
| C. | 气态氢化物的稳定性:W>X | |
| D. | 简单离子半径的大小顺序:r(Y+)>r(X-) |
18.设NA表示阿伏伽德罗常数的值,下列说法正确的是(相对原子质量:H-1,N-14)( )
0 153700 153708 153714 153718 153724 153726 153730 153736 153738 153744 153750 153754 153756 153760 153766 153768 153774 153778 153780 153784 153786 153790 153792 153794 153795 153796 153798 153799 153800 153802 153804 153808 153810 153814 153816 153820 153826 153828 153834 153838 153840 153844 153850 153856 153858 153864 153868 153870 153876 153880 153886 153894 203614
| A. | 标准状况下,22.4LHCl溶于水后溶液中含有NA个HCl分子 | |
| B. | 常温常压下,33.6LCl2中含有1.5NA个Cl2分子 | |
| C. | 1.8g的NH4+离子中含有NA个电子 | |
| D. | 将0.1mol氯化铝溶于1L水中,所得溶液含有0.1NAAl3+ |
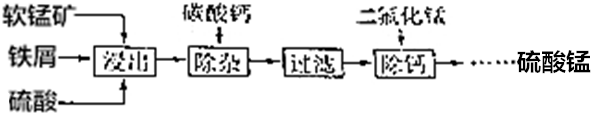
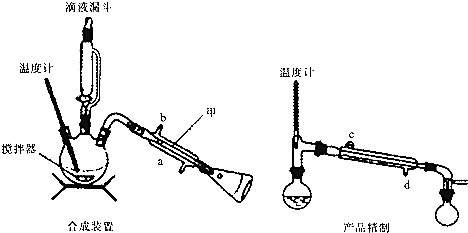
 实验室可用环己醇(沸点:160.84℃,微溶于水)制备环己酮(沸点:155.6℃,微溶于水),使用的氧化剂可以是次氯酸钠、重铬酸钾等.
实验室可用环己醇(沸点:160.84℃,微溶于水)制备环己酮(沸点:155.6℃,微溶于水),使用的氧化剂可以是次氯酸钠、重铬酸钾等.