8.某课题小组研究“铁及其化合物性质”时,向 FeSO4 溶液中滴加少量KSCN溶液,无明显现象.再滴加 H2 O2 溶液时,发现:随着H 2O 2量的增加,溶液先变红,后褪色,并有气泡产生.为弄清楚产生这种异常现象的原因,他们进行了如下探究.
[提出假设]
假设一:产生的气体可能是O 2.
假设二:产生的气体可能是N2、SO 2、CO 2 等气体.
(1 )请写出H2O 2氧化FeSO4的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
[实验设计]
为验证假设二是否成立,课题小组设计如下实验来验证气体成分.
所用试剂:H 2 O2 溶液、FeCl 2 溶液、KSCN 溶液、品红溶液、酸性高锰酸钾溶液、澄清石灰水、NaOH 溶液等.
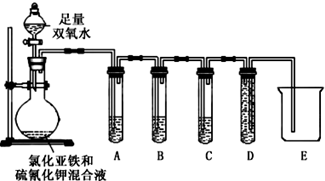
请完成下表中的内容:
[思考与交流]
(4 )根据题目中所给的信息及实验推断出物质还原性的强弱顺序:Fe2+>SCN-(填“>”或“<”),理由是向FeCl2和KSCN混合液中加入少量双氧水,溶液先变红,说明双氧水优先氧化Fe2+.
(5 )有同学认为:KSCN 被氧化的产物中可能还含有 SO 42-,请设计一个简单实验验证.
[提出假设]
假设一:产生的气体可能是O 2.
假设二:产生的气体可能是N2、SO 2、CO 2 等气体.
(1 )请写出H2O 2氧化FeSO4的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
[实验设计]
为验证假设二是否成立,课题小组设计如下实验来验证气体成分.
所用试剂:H 2 O2 溶液、FeCl 2 溶液、KSCN 溶液、品红溶液、酸性高锰酸钾溶液、澄清石灰水、NaOH 溶液等.

请完成下表中的内容:
| 实验过程和现象 | 结论 |
| (2)试管A中盛有品红溶液现象:品红溶液褪色 | 证明气体中含有SO2 |
| (3)试管B中现象紫色酸性高锰酸钾溶液颜色不变或变浅试管C中现象:澄清石灰水变浑浊 | 证明气体中含有CO2 |
(4 )根据题目中所给的信息及实验推断出物质还原性的强弱顺序:Fe2+>SCN-(填“>”或“<”),理由是向FeCl2和KSCN混合液中加入少量双氧水,溶液先变红,说明双氧水优先氧化Fe2+.
(5 )有同学认为:KSCN 被氧化的产物中可能还含有 SO 42-,请设计一个简单实验验证.
| 实验过程 | 实验现象及结论 |
6.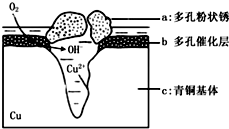 如图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图.环境中的 Cl- 扩散到孔口,并与各电极产物作用生成多孔粉状锈 Cu2 ( OH )3 Cl.下列说法正确的是( )
如图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图.环境中的 Cl- 扩散到孔口,并与各电极产物作用生成多孔粉状锈 Cu2 ( OH )3 Cl.下列说法正确的是( )
 如图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图.环境中的 Cl- 扩散到孔口,并与各电极产物作用生成多孔粉状锈 Cu2 ( OH )3 Cl.下列说法正确的是( )
如图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图.环境中的 Cl- 扩散到孔口,并与各电极产物作用生成多孔粉状锈 Cu2 ( OH )3 Cl.下列说法正确的是( )| A. | 腐蚀过程中,负极是 b 和 c | |
| B. | 生 成 Cu 2( OH )3 Cl 的 离子方程式为:2Cu2++3OH -═Cu 2( OH ) 3+ | |
| C. | 若生成 4.29gCu 2( OH )3 Cl,则理论上消耗标准状况氧气体积为0.448L | |
| D. | 正极的电极反应式为:O 2-4e-+2H+═2OH - |
5.用下列装置进行相应的实验,装置正确且能达到实验目的是( )
| A. |  用图所示装置验证 NaHCO 3 的不稳定性 | |
| B. | 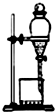 用图所示装置提取苯硝化反应后的产物 | |
| C. | 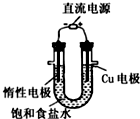 用图所示装置模拟氯碱工业生产氯气 | |
| D. | 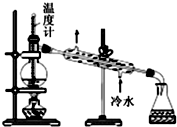 用图所示装置分馏石油 |
4.下列化学方程式与结论均正确的是( )
| 选项 | 方程式 | 结论 |
| A | 2AgI(s)+S2-(aq)?Ag2S(s)+2I-(aq) | 溶解度:Ag2S>AgI |
| B | C(s.石墨)═C(s.金刚石)△H>0 | 稳定性:金刚石>石墨 |
| C | 3Fe2++NO${\;}_{3}^{-}$+10H+═3Fe3++3H2O+NH${\;}_{4}^{+}$ | 还原性:Fe2+>NH${\;}_{4}^{+}$ |
| D | 2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3;Fe+S$\frac{\underline{\;加热\;}}{\;}$FeS | 氧化性:Cl2>S |
| A. | A | B. | B | C. | C | D. | D |
3.对二甲苯 ( PX )是生产矿泉水瓶 (聚对苯二甲酸乙二酯,简称 PET )的必要原料,生产涉及的反应之一如下:5 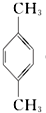 (PX)+12MnO${\;}_{4}^{-}$+36H+→5
(PX)+12MnO${\;}_{4}^{-}$+36H+→5 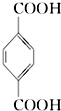 (PTA)+12Mn2++28H2O,下列有关说法错误的是( )
(PTA)+12Mn2++28H2O,下列有关说法错误的是( )
 (PX)+12MnO${\;}_{4}^{-}$+36H+→5
(PX)+12MnO${\;}_{4}^{-}$+36H+→5  (PTA)+12Mn2++28H2O,下列有关说法错误的是( )
(PTA)+12Mn2++28H2O,下列有关说法错误的是( )| A. | PTA 是该反应的氧化产物 | |
| B. | PTA 与乙二醇通过加聚反应即可生产 PET 塑料 | |
| C. | PX 分子含有苯环的同分异构体还有 3 种 | |
| D. | 该反应消耗 1molPX,共转移 12N A 个电子 ( NA 为阿伏加德罗常数) |
2.在化学学习中经常采用推理的思维方法,下列推理正确的是( )
0 153686 153694 153700 153704 153710 153712 153716 153722 153724 153730 153736 153740 153742 153746 153752 153754 153760 153764 153766 153770 153772 153776 153778 153780 153781 153782 153784 153785 153786 153788 153790 153794 153796 153800 153802 153806 153812 153814 153820 153824 153826 153830 153836 153842 153844 153850 153854 153856 153862 153866 153872 153880 203614
| A. | 加热蒸发食盐水可以得到 NaCl 晶体,加热蒸发 AlCl 3 溶液也可以得到 AlCl 3 晶体 | |
| B. | 配制浓度均为 0.1mol•L-1 的H3PO4 和 H2SO4 溶液,分别测其pH,若 H3PO 4溶液的pH大于 H2SO4 溶液的pH,可推出非金属性:S>P | |
| C. | NaHCO3 溶液中滴入酚酞显红色,NaHSO4 溶液中滴入酚酞也显红色 | |
| D. | 钠在氧气中燃烧生成过氧化钠,和钠同主族的锂在氧气中燃烧也生成过氧化锂 |
 .
. .
.
 卤族元素是典型的非金属元素,卤素单质及其化合物在生产和生活中都有重要的用途.
卤族元素是典型的非金属元素,卤素单质及其化合物在生产和生活中都有重要的用途. 、
、 、
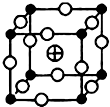
、 分别代表一种离子),晶胞边长为anm(1nm=10-9m),该晶体的化学式为KMgF3,该晶体的密度为$\frac{0.1993}{{a}^{3}}$g•cm-3.
分别代表一种离子),晶胞边长为anm(1nm=10-9m),该晶体的化学式为KMgF3,该晶体的密度为$\frac{0.1993}{{a}^{3}}$g•cm-3.
 A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中 B与C同周期,D与E、F同周期,A与D 同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍.又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体.
A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中 B与C同周期,D与E、F同周期,A与D 同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍.又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体.