15.已知某化学键的键能数据如下
则CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-184kJ•mol-1.
| 化学键 | C=O | C-O | C-H | H-H | O-H |
| 键能/kJ•mol-1 | 745 | 351 | 415 | 436 | 462 |
13. (1)已知:N2(g)+O2(g)═2NO(g)△H1=+180.5kJ/mol
(1)已知:N2(g)+O2(g)═2NO(g)△H1=+180.5kJ/mol
N2(g)+3H2(g)?2NH3(g)△H2=-92.4kJ/mol
2H2(g)+O2(g)=2H2O(g)△H3=-483.6kJ/mol
写出氨气催化氧化生成一氧化氮气体和水蒸气的热化学方程式4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=-905.0kJ/mol.
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g)?2NH3(g)反应的影响.实验结果如图所示:(图中T表示温度,n表示物质的量)
①图象中T2和T1的关系是:T2低于T1(填“高于”“低于”“等于”“无法确定”)
②比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是c(填字母).
(3)N2O5是一种新型硝化剂,其性质和制备受到人们的关注:一定温度下可发生下列反应:2N2O5(g)→4NO2(g)+O2(g)△H>0下表为反应在T1温度下的部分实验数据
①500s内NO2的平均生成速率为0.00592mol•L-1•s-1.
②该反应的化学平衡常数表达式为K=$\frac{{c}^{4}(N{O}_{2})•c({O}_{2})}{{c}^{2}({N}_{2}{O}_{5})}$.
 (1)已知:N2(g)+O2(g)═2NO(g)△H1=+180.5kJ/mol
(1)已知:N2(g)+O2(g)═2NO(g)△H1=+180.5kJ/molN2(g)+3H2(g)?2NH3(g)△H2=-92.4kJ/mol
2H2(g)+O2(g)=2H2O(g)△H3=-483.6kJ/mol
写出氨气催化氧化生成一氧化氮气体和水蒸气的热化学方程式4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=-905.0kJ/mol.
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g)?2NH3(g)反应的影响.实验结果如图所示:(图中T表示温度,n表示物质的量)
①图象中T2和T1的关系是:T2低于T1(填“高于”“低于”“等于”“无法确定”)
②比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是c(填字母).
(3)N2O5是一种新型硝化剂,其性质和制备受到人们的关注:一定温度下可发生下列反应:2N2O5(g)→4NO2(g)+O2(g)△H>0下表为反应在T1温度下的部分实验数据
| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.48 |
②该反应的化学平衡常数表达式为K=$\frac{{c}^{4}(N{O}_{2})•c({O}_{2})}{{c}^{2}({N}_{2}{O}_{5})}$.
12.下列生活或实验中电化学的应用及其相关说法正确的是( )
0 153669 153677 153683 153687 153693 153695 153699 153705 153707 153713 153719 153723 153725 153729 153735 153737 153743 153747 153749 153753 153755 153759 153761 153763 153764 153765 153767 153768 153769 153771 153773 153777 153779 153783 153785 153789 153795 153797 153803 153807 153809 153813 153819 153825 153827 153833 153837 153839 153845 153849 153855 153863 203614
| 电化学应用 | 相关解释或说法 | |
| A | 以稀H2SO4为电解质的Cu-Zn原电池 | Cu为正极,正极上发生还原反应 |
| B | 电解CuCl2溶液 | 电子经过负极→阴极$\stackrel{通过电解液}{→}$阳极→正极 |
| C | 弱酸性环境下钢铁腐蚀 | 负极产生H2,正极处吸收O2 |
| D | 将铜闸门与外加电源负极相连 | 牺牲阳极的阴极保护法,可防止钢闸门腐蚀 |
| A. | A | B. | B | C. | C | D. | D |
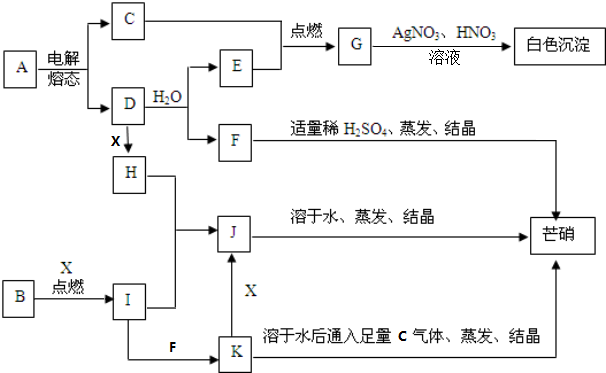
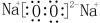 .
. .
.