18.工业制硫酸中的一步重要反应是SO2(在400-500℃下的催化氧化:2SO2+O2?2SO3,这是一个正反应放热的可逆反应,如果反应在密闭容器中进行,下述有关说法错误的是( )
| A. | 在上述条件下,SO2可能100%的转化为SO3 | |
| B. | 使用催化剂是为了加快反应速率,提高生产效率 | |
| C. | 达到平衡时,SO2与SO3的浓度保持不变 | |
| D. | 为了提高SO2的转化率,可以适当提高O2的浓度 |
17.实验室保存下列物质的方法中,不正确的是( )
| A. | 少量金属钠保存在煤油里 | |
| B. | 液溴应保存在棕色磨口玻璃塞的试剂瓶中,并加少量水进行水封 | |
| C. | 为防止氧化,FeSO4溶液存放在加有少量铜粉的试剂瓶中 | |
| D. | 硝酸应装在棕色瓶中密封避光保存 |
16.3He可以作为核聚变材料,以下关于3He的说法正确的是( )
| A. | 比4He少一个质子 | B. | 比4He多一个中子 | ||
| C. | 是4He的同素异形体 | D. | 是4He的同位素 |
13.煤化工中常需研究不同温度下的平衡常数、投料比及产率等问题,提高一氧化碳制取氢气的产率是其重要研究之一.
(1)已知:
C(石墨)+$\frac{1}{2}$O2(g)=CO(g)△H1=-111kJ/mol
H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H2=-242kJ/mol
C(石墨)+O2(g)=CO2(g)△H3=-394kJ/mol
请写出一氧化碳那与水作用转化为氢气和二氧化碳反应的热化学方程式:CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41kJ/mol;
(2)能判断该反应达到化学平衡状态的依据是( )(填序号);
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(3)已知一氧化碳与水作用转化为氢气和二氧化碳的化学平衡常数随温度的变化如下表:
在800℃时,2L的密闭容器中加入4molCO(g)和6molH2O(g),10min后达到平衡时CO2的平衡浓度为1.2mol/L,用H2浓度变化来表示的平均反应速率为0.12mol/(L•min),CO的转化率是60%;
(4)为使该反应的速率增大且平衡向正反应方向移动,可采取的措施是A.
A.增大CO浓度 B.升高温度
C.将生成物分离出去 D.使用高效催化剂.
(1)已知:
C(石墨)+$\frac{1}{2}$O2(g)=CO(g)△H1=-111kJ/mol
H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H2=-242kJ/mol
C(石墨)+O2(g)=CO2(g)△H3=-394kJ/mol
请写出一氧化碳那与水作用转化为氢气和二氧化碳反应的热化学方程式:CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41kJ/mol;
(2)能判断该反应达到化学平衡状态的依据是( )(填序号);
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(3)已知一氧化碳与水作用转化为氢气和二氧化碳的化学平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 800 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
(4)为使该反应的速率增大且平衡向正反应方向移动,可采取的措施是A.
A.增大CO浓度 B.升高温度
C.将生成物分离出去 D.使用高效催化剂.
11.下列反应中,属于加成反应的是( )
0 153663 153671 153677 153681 153687 153689 153693 153699 153701 153707 153713 153717 153719 153723 153729 153731 153737 153741 153743 153747 153749 153753 153755 153757 153758 153759 153761 153762 153763 153765 153767 153771 153773 153777 153779 153783 153789 153791 153797 153801 153803 153807 153813 153819 153821 153827 153831 153833 153839 153843 153849 153857 203614
| A. | CH3CH3+Cl2$\stackrel{光}{→}$CH3CH2Cl+HCl | |
| B. | 2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O | |
| C. | 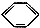 +Br2$\stackrel{Fe}{→}$ +Br2$\stackrel{Fe}{→}$ Br+HBr Br+HBr | |
| D. | CH2═CH2+Br2→CH2Br-CH2Br |

 用二氧化氯(ClO2)、铁酸钠(Na2FeO4摩尔质量为166g/mol)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术.ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+.
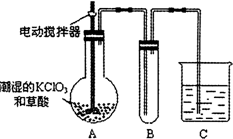
用二氧化氯(ClO2)、铁酸钠(Na2FeO4摩尔质量为166g/mol)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术.ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+. 煤的干馏是煤气化的重要方法,也是煤综合利用最“古老”的、最简单的方法.某实验小组根据教材习题设计了煤干馏实验,装置如图所示.实验时,取约2-3g的煤粒,在研体中研磨至粉末状态;用药匙将煤粉放入试管中,在具支试管中加入2mL水,按照如图所示安装好装置;点燃酒精灯,对试管预热后再集中受热,待具支试管中气泡产生的速度均匀后,在具支试管口收集气体,并用明火靠近具支试管口,可以观察到产生的气体能够燃烧.根据上述实验回答下列问题:
煤的干馏是煤气化的重要方法,也是煤综合利用最“古老”的、最简单的方法.某实验小组根据教材习题设计了煤干馏实验,装置如图所示.实验时,取约2-3g的煤粒,在研体中研磨至粉末状态;用药匙将煤粉放入试管中,在具支试管中加入2mL水,按照如图所示安装好装置;点燃酒精灯,对试管预热后再集中受热,待具支试管中气泡产生的速度均匀后,在具支试管口收集气体,并用明火靠近具支试管口,可以观察到产生的气体能够燃烧.根据上述实验回答下列问题: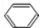 +HNO3$→_{△}^{浓硫酸}$
+HNO3$→_{△}^{浓硫酸}$ +H2O;
+H2O;
 .
.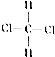 和
和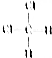 ⑧乙烷和戊烷
⑧乙烷和戊烷