10.下列有关实验操作的叙述中正确的是( )
| A. |  利用甘油密度大于乙醇且更易溶于水,进行甘油与乙醇的混合物分离 | |
| B. | 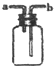 进行H2,NH3,CO2,Cl2,HCl,NO2等气体收集,也能用于NO气体收集 | |
| C. |  当X选用苯时可进行NH3和HCl的吸收,并防止倒吸 | |
| D. | 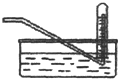 常用于实验室收集氧气、氢气等 |
7.下列对化学平衡移动的分析中,不正确的是( )
①平衡时,增加反应物物质的量,平衡一定向正反应方向移动
②已达平衡的反应2SO2(g)+O2(g)?2SO3(g),当增大O2的浓度时,O2的转化率一定升高
③反应平衡时,若减小反应器容积时,平衡一定会移动
④有气体参加的反应达平衡时,在恒容反应器中充入稀有气体,平衡一定不移动.
①平衡时,增加反应物物质的量,平衡一定向正反应方向移动
②已达平衡的反应2SO2(g)+O2(g)?2SO3(g),当增大O2的浓度时,O2的转化率一定升高
③反应平衡时,若减小反应器容积时,平衡一定会移动
④有气体参加的反应达平衡时,在恒容反应器中充入稀有气体,平衡一定不移动.
| A. | ①④ | B. | ①③ | C. | ②③④ | D. | ①②③ |
6.已知:2SO2(g)+O2(g)?2SO3(g)△H>0.该反应达到平衡后,改变下列条件有利于提高SO2转化率的是( )
| A. | 加催化剂 | B. | 降低温度 | C. | 减小压强 | D. | 加入O2 |
5.乙醛能与银氨溶液反应析出银,如果条件控制适当,析出的银会均匀分布在试管上,形成光亮的银镜,这个反应叫银镜反应.银镜的光亮程度与反应条件有关,某课外活动小组同学在课外活动中对乙醛的银镜反应进行了探究.
Ⅰ.探究银镜反应的最佳实验条件的部分实验数据如下表:
请回答下列问题:
(1)若只进行实验1和实验3,其探究目的是比较乙醛用量不同,生成银镜的时间(速度或质量均可).
(2)推理当银氨溶液的量为1mL,乙醛的量为3滴,水浴温度为40℃,反应混合液pH为11时,出现银镜的时间范围是在6.5~9min之间.
(3)进一步实验还可探索银氨溶液的用量不同或pH不同对出现银镜快慢的影响.
Ⅱ.探究对废液的回收处理:银氨溶液放久后会变成氮化银而引起爆炸,直接排放会污染环
境,且造成银资源的浪费.通过查找资料,已知从银氨溶液中提取银的一种实验流程如下:
$→_{①}^{(NH_{4})_{2}S}$$→_{②}^{过滤、洗涤}$$→_{③}^{烘干}$Ag2S$→_{④}^{铁粉还原}$银粉
(4)操作④的方法是把Ag2S和铁粉放到烧杯中加浓盐酸搅拌煮沸,使Ag2S变成银粉,反应的化学方程式为Ag2S+Fe+2HCl$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+FeCl2+H2S↑.过滤需要用到的玻璃仪器有bef(填编号).要得到纯净的Ag2S沉淀,需要洗涤沉淀,实验室过滤器中洗涤沉淀的操作是:沿着玻璃棒向过滤器注入蒸馏水浸没沉淀,水自然流下,重复2~3次.
(5)根据电化原理也可Ag2S转变为Ag,方法是:在铝质容器中加入食盐溶液,再将表面生成Ag2S的银器浸入该溶液中,一段时间后发现黑色会褪去.
①该装置中银器为正极.
②该装置总反应的化学方程式为2Al+3Ag2 S+3H2O=2Al(OH)3+6Ag+3H2S↑.
Ⅰ.探究银镜反应的最佳实验条件的部分实验数据如下表:
| 实验序号 | 银氨溶液 | 乙醛的量/滴 | 水浴温度/℃ | 反应混合液的pH | 出现银镜时间 |
| 1 | 1 | 3 | 65 | 11 | 5 |
| 2 | 1 | 3 | 45 | 11 | 6.5 |
| 3 | 1 | 5 | 65 | 11 | 4 |
| 4 | 1 | 3 | 30 | 11 | 9 |
| 5 | 1 | 3 | 50 | 11 | 6 |
| 6 | 1 | 5 | 80 | 11 | 3 |
(1)若只进行实验1和实验3,其探究目的是比较乙醛用量不同,生成银镜的时间(速度或质量均可).
(2)推理当银氨溶液的量为1mL,乙醛的量为3滴,水浴温度为40℃,反应混合液pH为11时,出现银镜的时间范围是在6.5~9min之间.
(3)进一步实验还可探索银氨溶液的用量不同或pH不同对出现银镜快慢的影响.
Ⅱ.探究对废液的回收处理:银氨溶液放久后会变成氮化银而引起爆炸,直接排放会污染环
境,且造成银资源的浪费.通过查找资料,已知从银氨溶液中提取银的一种实验流程如下:
$→_{①}^{(NH_{4})_{2}S}$$→_{②}^{过滤、洗涤}$$→_{③}^{烘干}$Ag2S$→_{④}^{铁粉还原}$银粉
(4)操作④的方法是把Ag2S和铁粉放到烧杯中加浓盐酸搅拌煮沸,使Ag2S变成银粉,反应的化学方程式为Ag2S+Fe+2HCl$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+FeCl2+H2S↑.过滤需要用到的玻璃仪器有bef(填编号).要得到纯净的Ag2S沉淀,需要洗涤沉淀,实验室过滤器中洗涤沉淀的操作是:沿着玻璃棒向过滤器注入蒸馏水浸没沉淀,水自然流下,重复2~3次.

(5)根据电化原理也可Ag2S转变为Ag,方法是:在铝质容器中加入食盐溶液,再将表面生成Ag2S的银器浸入该溶液中,一段时间后发现黑色会褪去.
①该装置中银器为正极.
②该装置总反应的化学方程式为2Al+3Ag2 S+3H2O=2Al(OH)3+6Ag+3H2S↑.
3.体积相同的甲、乙两个容器中,分别都充有等物质的量的SO3,在相同温度下发生反应:2SO3(g)?2SO2(g)+O2(g),并达到平衡.在这个过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO3的转化率为p%,则乙容器中SO3的转化率( )
| A. | 等于p% | B. | 大于p% | C. | 小于p | D. | 无法判断 |
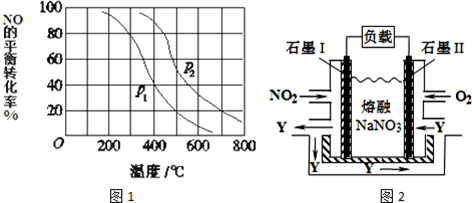
2.如图1表示mA(g)+nB(g)?pC(g)+qD(g),在不同温度下经过一定时间混合体系中C的质量分数与温度T的关系;如图2表示在一定条件下达到平衡(v正=v逆)后t时刻改变影响平衡的一个条件重新建立新平衡的反应过程,判断该反应是( )


| A. | m+n<p+q△H>0 | B. | m+n>p+q△H>0 | C. | m+n<p+q△H<0 | D. | m+n>p+q△H<0 |
1.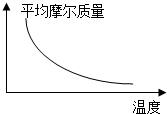 可逆反应2A+B?2C(g)(正反应放热),随温度变化气体平均摩尔质量如图所示,则下列叙述正确的是( )
可逆反应2A+B?2C(g)(正反应放热),随温度变化气体平均摩尔质量如图所示,则下列叙述正确的是( )
0 153644 153652 153658 153662 153668 153670 153674 153680 153682 153688 153694 153698 153700 153704 153710 153712 153718 153722 153724 153728 153730 153734 153736 153738 153739 153740 153742 153743 153744 153746 153748 153752 153754 153758 153760 153764 153770 153772 153778 153782 153784 153788 153794 153800 153802 153808 153812 153814 153820 153824 153830 153838 203614
 可逆反应2A+B?2C(g)(正反应放热),随温度变化气体平均摩尔质量如图所示,则下列叙述正确的是( )
可逆反应2A+B?2C(g)(正反应放热),随温度变化气体平均摩尔质量如图所示,则下列叙述正确的是( )| A. | A和B可能都是固体 | B. | A和B一定都是气体 | ||
| C. | 若B为固体,则A一定是气体 | D. | A和B不可能都是气体 |
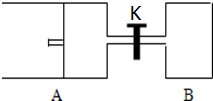 如图所示,向A中充入1mol X和1mol Y,向B中充入2mol X和2mol Y,起始时,V(A)=V(B)=a L.在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:X(g)+Y(g)?2Z(g)+W(g)△H<0达到平衡时,V(A)=1.2aL.试回答:
如图所示,向A中充入1mol X和1mol Y,向B中充入2mol X和2mol Y,起始时,V(A)=V(B)=a L.在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:X(g)+Y(g)?2Z(g)+W(g)△H<0达到平衡时,V(A)=1.2aL.试回答: