3.下列都是生活中常见的物质,其中属于纯净物的是( )
| A. | 葡萄酒 | B. | 冰水 | C. | 碘盐 | D. | 食醋 |
19.采用硫酸同槽浸出软锰矿(主要成分MnO2)和黄铜矿(主要成分CuFeS2)的新工艺方法提取锰、铜、铁元素获得成功,生产流程如图所示:
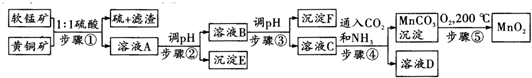
已知:(1)步骤?5MnO2+2CuFeS2+10H2SO4═5MnSO4+Fe2(SO4)3+2CuSO4+4S↓+10H2O
?部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
根据表中数据,回答相关问题:
(1)步骤?①中每生成64g硫,转移电子的数目为5NA;
(2)步骤?②中pH的范围是3.2≤pH<4.2或3.2<pH<4.2,沉淀E主要成分的化学式为Fe(OH)3;
(3)MnSO4溶液中c(MnSO4)=3×10-6mol/L,某碳酸盐溶液中c(CO32-)=3.3×10-5mol/L,若两溶液按体积比2:1混合,恰好达到溶解平衡,则MnCO3的Ksp=2.2×10-11;
(4)步骤④发生的离子反应方程式:Mn2++2NH3+CO2+H2O=MnCO3↓+2NH4+;
(5)称取0.58g软锰矿于烧杯中,再分别向烧杯中加入过量20.00mL0.1000mol/LNa2C2O4溶液和过量的硫酸,充分搅拌溶解,过滤,将滤液转移至锥形瓶中,用0.1000mol/L的KMnO4溶液滴定至终点,消耗了4.00mLKMnO4溶液.有关反应如下:
MnO2+Na2C2O4+2H2SO4═MnSO4+Na2SO4+2CO2↑+2H2O
5Na2C2O4+2KMnO4+8H2SO4═2MnSO4+K2SO4+5Na2SO4+10CO2↑+8H2O
①实验过程中,若在滴定前滴定管尖嘴部分无气泡,滴定后滴定管尖嘴部分产生了气泡,则会使滴定时消耗的KMnO4溶液体积偏大(填“偏大”、“偏小”或“不变”).
②计算软锰矿中MnO2 的百分含量:15.0%.

已知:(1)步骤?5MnO2+2CuFeS2+10H2SO4═5MnSO4+Fe2(SO4)3+2CuSO4+4S↓+10H2O
?部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Cu(OH)2 | Fe(OH)3 | Mn(OH)2 | Fe(OH)2 |
| 开始沉淀pH | 4.2 | 1.5 | 7.3 | 6.4 |
| 完全沉淀pH | 6.7 | 3.2 | 9.8 | 9.0 |
(1)步骤?①中每生成64g硫,转移电子的数目为5NA;
(2)步骤?②中pH的范围是3.2≤pH<4.2或3.2<pH<4.2,沉淀E主要成分的化学式为Fe(OH)3;
(3)MnSO4溶液中c(MnSO4)=3×10-6mol/L,某碳酸盐溶液中c(CO32-)=3.3×10-5mol/L,若两溶液按体积比2:1混合,恰好达到溶解平衡,则MnCO3的Ksp=2.2×10-11;
(4)步骤④发生的离子反应方程式:Mn2++2NH3+CO2+H2O=MnCO3↓+2NH4+;
(5)称取0.58g软锰矿于烧杯中,再分别向烧杯中加入过量20.00mL0.1000mol/LNa2C2O4溶液和过量的硫酸,充分搅拌溶解,过滤,将滤液转移至锥形瓶中,用0.1000mol/L的KMnO4溶液滴定至终点,消耗了4.00mLKMnO4溶液.有关反应如下:
MnO2+Na2C2O4+2H2SO4═MnSO4+Na2SO4+2CO2↑+2H2O
5Na2C2O4+2KMnO4+8H2SO4═2MnSO4+K2SO4+5Na2SO4+10CO2↑+8H2O
①实验过程中,若在滴定前滴定管尖嘴部分无气泡,滴定后滴定管尖嘴部分产生了气泡,则会使滴定时消耗的KMnO4溶液体积偏大(填“偏大”、“偏小”或“不变”).
②计算软锰矿中MnO2 的百分含量:15.0%.
18.设NA为阿伏伽德罗常数的数值,下列说法不正确的是( )
| A. | 两份均为18g的Al片分别与足量的盐酸和NaOH溶液充分转移电子总数均为2NA | |
| B. | 1 molCu和2 mol热浓硫酸充分反应,可生成NA个SO2分子 | |
| C. | 标准状况下,14g N2和C2H4混合气体的体积为11.2L | |
| D. | 3mol单质Fe完全转变为Fe3O4,失去8NA个电子 |
17.下列说法正确的是( )
| A. | 氧化还原反应中一定有电子得失 | B. | 凡是能电离出H+的化合物均属于酸 | ||
| C. | 离子反应不一定是氧化还原反应 | D. | 置换反应不一定是氧化还原反应 |
14.咖啡和茶叶中富含漂木酸,它具有抗癌作用,其结构简式如图.下列有关说法正确的是( )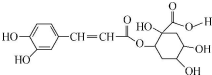
0 153635 153643 153649 153653 153659 153661 153665 153671 153673 153679 153685 153689 153691 153695 153701 153703 153709 153713 153715 153719 153721 153725 153727 153729 153730 153731 153733 153734 153735 153737 153739 153743 153745 153749 153751 153755 153761 153763 153769 153773 153775 153779 153785 153791 153793 153799 153803 153805 153811 153815 153821 153829 203614

| A. | 每个分子中含有4个手性碳原子 | |
| B. | 能与FeCl3溶液发生显色反应 | |
| C. | 1mol该有机物只能与1molBr2发生反应 | |
| D. | 1mol该有机物最多与8molNaOH反应 |
 有一无色透明溶液,可能含Al3+、Fe3+、Cu2+、Mg2+、K+、OH-、CO32-、Cl-离子中的若干种.现做如下实验:
有一无色透明溶液,可能含Al3+、Fe3+、Cu2+、Mg2+、K+、OH-、CO32-、Cl-离子中的若干种.现做如下实验: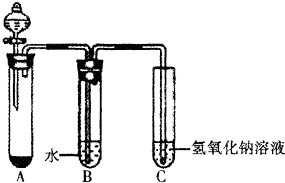 某课外小组同学用下图所示装置进行C12的制备及相关性质实验(加热及夹持装置已省略).
某课外小组同学用下图所示装置进行C12的制备及相关性质实验(加热及夹持装置已省略).